| روانگسیختگی | |
|---|---|

پارچهٔ سوزندوزیشده توسط بیمار مبتلا به اسکیزوفرنی
|
|
| آیسیدی-۱۰ | F20 |
| آیسیدی-۹ | 295 |
| اُمیم | 181500 |
| دادگان بیماریها | ۱۱۸۹۰ |
| مدلاین پلاس | 000928 |
| ایمدیسین | med/۲۰۷۲ emerg/520 |
| پیشنت پلاس | اسکیزوفرنی |
| سمپ | F03.700.750 |
روانگسیختگی یا اسکیزوفرنی یا شیزوفرنی(به انگلیسی: Schizophrenia) یک اختلال روانی است که مشخصهٔ آن ازکارافتادگی فرایندهای فکری و پاسخگویی عاطفی ضعیف است.[۱] این بیماری در بین همهٔ بیماریهای عمدهٔ روانشناختی از همه وخیمتر میباشد و معمولاً خود را به صورت توهم شنیداری، توهمهای جنون آمیز یا عجیب و غریب، یا تکلم و تفکر آشفته نشان میدهد، و با اختلال در عملکرد اجتماعی یا شغلی قابل توجهی همراه است. شروع علائم معمولاً در دوران نوجوانی رخ میدهد، با یک شیوع در طول زندگی جهانی در حدود ۰٫۳–۰٫۷٪.[۲] تشخیص بر اساس مشاهدهٔ رفتار و تجارب گزارششدهٔ بیمار است.
به نظر میرسد ژنتیک، محیط اولیه، نوروبیولوژی، و فرایندهای روانی و اجتماعی از عوامل مهم مؤثر باشند؛ ۴۰ درصد از بیماران مبتلا به اسکیزوفرنی چپ دست بودهاند.http://sara.jamejamonline.ir/NewsPreview/2056807644655767691 به نظر میرسد برخی از مواد مخدر تفریحی و داروها باعث ایجاد یا بدتر شدن علایم میشوند. پژوهش حاضر بر روی نقش نوروبیولوژی متمرکز شده است، اگر چه هیچ علت ارگانیک مجزایی یافت نشد. ترکیب بسیار محتمل علائم بحثهایی را در مورد اینکه آیا تشخیص نشان دهندهٔ یک اختلال واحد است یا تعدادی از سندرمهای گسسته، بر انگیخته شده است. با وجود اینکه ریشه لغت در یونانی skhizein (σχίζειν، «گسستن») و phrēn, phren- (φρήν, φρεν-؛ «ذهن») است، اسکیزوفرنی به معنی «ذهن گسیخته» نیست و همانند اختلال شخصیت تجزیهای نمیباشد- که به عنوان «اختلال شخصیت چندگانه» یا «هویت پریشی» نیز شناخته میشود - شرایطی که اغلب در ادراک عمومی با آن اشتباه گرفته میشود.[۳]
نقطه اتکای درمان، داروهای آنتی سایکوتیک (ضد جنون) است، که عمدتاً فعالیت گیرنده دوپامین (و گاهی اوقات سروتونین) را سرکوب میکنند. درمان روانی و توان بخشی حرفهای و اجتماعی نیز در درمان مهم هستند. در موارد جدیتر - که امکان ایجاد خطر برای شخص بیمار و دیگران وجود دارد - ممکن است به بستری اجباری نیاز باشد، اگر چه ماندن در بیمارستان در حال حاضر کوتاهتر و کمتر از آن چیزی است که زمانی مرسوم بود.[۴]
اختلال عمدتاً ادراک را تحت تأثیر قرار میدهد، اما معمولاً به مشکلات مزمن در رفتار و احساسات نیز میانجامد. افراد مبتلا به اسکیزوفرنی در معرض شرایط اضافی (همراه بیماری) هستند، از جمله افسردگی اساسی و اختلال اضطراب؛ احتمال سوء مصرف مواد مخدر در طول زندگی تقریباً ۵۰٪ است.[۵] مشکلات اجتماعی از قبیل بیکاری طولانی مدت، فقر و بیخانمانی، شایع هستند. امید به زندگی متوسط افراد مبتلا به این اختلال به دلیل افزایش مشکلات سلامت جسمی و نرخ خودکشی بالاتر (حدود ۵٪) ۱۲ تا ۱۵ سال کمتر از کسانی که مبتلا به آن نیستند.[۲]
محتویات
علائم
فرد مبتلا به اسکیزوفرنی ممکن است دچار توهمهایی شود (که اغلب به صورت شنیدن صداها گزارش شده است)، خیالات (اغلب عجیب و غریب یا سرکوب گرانه در طبیعت) و آشفتگی فکری و کلامی میباشند. مورد دوم ممکن است از از دست دادن قطار اندیشه، تا جملات با اتصال نامنظم در معنی، تا تناقض شناخته شده به عنوان آشفته گویی در موارد حاد متغیر باشد. گوشهگیری اجتماعی، نامرتبی لباس و بهداشت، و از دست دادن انگیزه و قضاوت تماماً موارد عادی موجود در اسکیزوفرنی میباشند.[۶] اغلب الگوی قابل مشاهدهای از مشکل عاطفی وجود دارد، برای مثال عدم پاسخگویی به محرکات.[۷] اختلال در شناخت اجتماعی با اسکیزوفرنی مرتبط است،[۸] همچنین علائم پارانویا؛ انزوای اجتماعی به طور معمول اتفاق میافتد.[۹] همچنین معمولاً مشکلات در کار و حافظهٔ بلند مدت، توجه، عملکرد اجرایی، و سرعت پردازش رخ میدهد.[۲] در یک زیرگروه غیر معمول، فرد ممکن است تا حد زیادی ساکت باشد، در وضعیتهای حرکتی عجیب و غریب، یا در جلوههای بیموردی از اضطراب قرار بگیرد، که همهٔ اینها نشانههایی از جنون جوانی میباشند.[۱۰]
اواخر نوجوانی و اوایل دوران بلوغ، دورههای اوج شروع بیماری اسکیزوفرنی میباشند،[۲] که سالهای بحرانی توسعهٔ اجتماعی و حرفهای یک نوجوان است.[۱۱] در ۴۰٪ از مردان و ۲۳٪ از زنان مبتلا به اسکیزوفرنی، این مهم قبل از سن ۱۹ سالگی خود را نمایان میکند.[۱۲] برای به حداقل رساندن گستردگی اختلال مرتبط با اسکیزوفرنی، به تازگی کار بسیاری برای شناسایی و درمان مرحلهٔ علائم اولیه (قبل از شروع) بیماری به انجام رسیده است، که تا ۳۰ ماه قبل از شروع علائم قابل تشخیص است.[۱۱] کسانی که بیماری اسکیزوفرنی آنها در حال پیشرفت است ممکن است علائم گذرا یا خود محدودگری روانی[۱۳] و علائم نامعین کنارهگیری از اجتماع، تحریک پذیری، بیقراری،[۱۴] و عدم مهارت حرکتی[۱۵] را در طول مرحلهٔ ابتدایی بیماری تجربه کنند.
طبقهبندی اشنایدری
در اوایل قرن بیستم، روانپزشک کورت اشنایدر علائم روانپریشی را که وی فکر میکرد اسکیزوفرنی از سایر اختلالات روانی مجزا میکند فهرستبندی کرد. اینها به نام «علائم درجه اول» یا علائم درجه اول اشنایدر معروفند. آنها عبارتند از: کنترل هذیان توسط نیروی خارجی، اعتقاد به این که افکار به درون ذهن شخص وارد میشوند یا برگرفته از ذهن شخص میباشند؛ اعتقاد به این که افکار شخص به افراد دیگر اشاعه مییابند، و شنیدن صداهای وهمآوری که منتقد افکار یا اعمال شخص یا آمیزشی از صداهای وهمآور دیگر باشند.[۱۶] اگر چه آنها به طور قابل توجهی به معیارهای تشخیصی کنونی کمک کردهاند، اما ویژگی علائم درجه اول بحثبرانگیز میباشند. از بررسی مطالعات تشخیصی انجام شده بین سالهای ۱۹۷۰ و ۲۰۰۵ درمییابیم که آنها مجاز به تأیید یا رد ادعای اشنایدر نمیباشند، و پیشنهاد شده است که علائم درجه اول باید، تأکیدی بر بازبینی سیستمهای شناختی آینده باشند.[۱۷]
علائم مثبت و منفی
اسکیزوفرنی اغلب با واژههای علائم مثبت و منفی (فقدان) شرح داده میشود.[۱۸] علائم مثبت، آنهایی هستند که اکثر افراد به طور عادی تجربه نمیکنند، اما در افراد مبتلا به اسکیزوفرنی موجود میباشند. آنها میتوانند شامل هذیان، اختلال افکاری و گفتاری، و توهم لمسی، شنوایی، بصری، بویایی و چشایی باشند، و معمولاً به عنوان جلوهای از جنون در نظر گرفته شوند.[۱۹] به طور معمول توهمات نیز مرتبط با محتوای مقولهٔ خیال میباشند.[۲۰] عموماً علائم مثبت خوب به دارو پاسخ میدهند.[۲۰] علائم منفی فقدانی از پاسخهای عاطفی طبیعی یا سایر فرایندهای فکری میباشند، و کمتر به دارو پاسخ میدهند.[۶] آنها معمولاً شامل یکنواختی عاطفی یا کمبود عاطفه و احساس، فقر بیان (عجز گویایی)، ناتوانی در تجربهٔ خوشی و لذت (فقدان لذت)، عدم تمایل به تشکیل روابط (بی تفاوتی اجتماعی)، و فقدان انگیزه (فقدان اراده) میشوند. تحقیقات نشان میدهد که نشانههای منفی نسبت به علائم مثبت بیشترین تأثیر را در کیفیت زندگی ضعیف، ناتوانی عملکردی، و بار مسئولیتی که بر دوش دیگران است دارند.[۲۱] اغلب افراد با علائم منفی برجسته دارای سابقهٔ ناموزونی قبل از شروع بیماری میباشند، و اغلب پاسخ به دارو محدود میباشد.[۶][۲۲]
علل
ترکیبی از ژنتیک و عوامل زیست محیطی در پیشرفت اسکیزوفرنی ایفای نقش میکنند.[۲][۳] افراد با سابقه خانوادگی اسکیزوفرنی که از جنون گذرا یا خود محدودگری رنج میبرند به احتمال ۲۰–۴۰٪ بیماریشان یک سال بعد مشخص میشود.[۲۳]
ژنتیک
برآورد قابلیت به ارث بردن به دلیل مشکل بودن جدا کردن اثرات ژنتیکی و زیست محیطی متفاوت است.[۲۴] بزرگترین خطر برای پیشرفت اسکیزوفرنی داشتن یک فامیل درجه اول مبتلا به این بیماری میباشد (درصد خطر ۶٫۵٪ است)؛ بیش از ۴۰٪ از دوقلوهای همسان کسانی که مبتلا به اسکیزوفرنی هستند نیز تحت تأثیر قرار میگیرند.[۳] این احتمال وجود دارد که بسیاری از ژنها، آمیزشی از هر یک از اثر کوچک و ناشناخته انتقالی و ظاهری ناشناخته باشند.[۳] کاندیداهای احتمالیی زیاد پیشنهاد شدهاند، از جمله تغییرات تعداد کپی خاص، NOTCH4 و مکان ژن پروتئین هیستون.[۲۵] تعداد ارتباط به وسعت ژنوم مانند پروتئین انگشتی روی ۸۰۴A نیز مرتبط شدهاند.[۲۶] به نظر میرسد همپوشانی قابل توجهی در ژنتیک اسکیزوفرنی وجود دارد و اختلال دوقطبی[۲۷] با فرض یک مبنای ارثی، یک سوال از روانشناسی تکاملی این است که چرا ژنهایی که احتمال جنون تکامل یافته را افزایش میدهند، با در نظر گرفتن شرایط، از نقطه نظر تکاملی ناسازگارانه میباشند. یک تئوری به نقش ژنهای دخیل در تکامل زبانی و طبیعت انسان اشاره دارد، اما تا به امروز چنین ایدههایی کمی بیش از ایدههای نظری موجود در طبیعت به قوت خود باقی هستند.[۲۸][۲۹]
در ژوئیهٔ ۲۰۱۴ دانشمندان موفق شدند هشتاد و سه ژن جدید را که در بیماری اسکیزوفرنی نقش دارند شناسایی کنند.[۳۰] بیشتر این ژنها در انتقال پیامهای شیمیایی در مغز نقش دارند و برخی دیگر نیز بر سیستم ایمنی بدن تأثیر میگذارند. این پژوهش ژنتیکی بودن این بیماری را ثابت کرد.[۳۱]
محیط زیست
عوامل زیست محیطی مرتبط با پیشرفت اسکیزوفرنی عبارتند از: محیط زندگی، مصرف مواد مخدر و عوامل استرس زای قبل از تولد.[۲] به نظر میرسد سبک و شیوه تربیتی والدین اثر عمدهای ندارد، گر چه افرادی که از حمایت والدین برخوردارند از موقعیت بهتری نسبت به افرادی که والدینی انتقادی یا خصمانه دارند برخوردار میباشند.[۳] زندگی در یک محیط شهری در دوران کودکی یا بلوغ به طور مداوم با افزایش خطر ابتلاء به اسکیزوفرنی توسط یکی از دو عامل ذکر شده،[۲][۳] حتی پس از در نظر گرفتن مصرف مواد مخدر، گروه قومی، و اندازه و وسعت گروه اجتماعی همراه میباشد.[۳۲] از عوامل دیگری که نقش مهمی را ایفا میکنند عبارتند از: انزوای اجتماعی و مهاجرت مرتبط با سختیهای اجتماعی، تبعیض نژادی، اختلال در خانواده، بیکاری، و کمبود شرایط مسکن.[۳][۳۳]
سوء مصرف مواد مخدر
شماری از مواد مخدر که باعث رشد و پیشرفت اسکیزوفرنی میشوند، عبارتند از: حشیش، کوکائین، و آمفتامین.[۳] حدود نیمی از کسانی که مبتلا به اسکیزوفرنی هستند بیش از حد مواد مخدر و / یا الکل مصرف میکنند.[۳۴] نقش حشیش میتواند علی باشد،[۳۵] اما داروها و مواد دیگر ممکن است تنها به عنوان مکانیسمهایی سازگار برای مقابله با افسردگی، اضطراب، خستگی، و تنهایی مصرف شوند.[۳۴][۳۶]
حشیش با افزایش تعلق میزان مصرف با خطر پیشرفت یک اختلال روانی مرتبط[۳۷] که استفاده مکرر با دو برابر خطر ابتلاء به جنون و اسکیزوفرنی مرتبط است.[۳۶][۳۸] حال آنکه برشمردن مصرف حشیش به عنوان عامل مؤثر بر ابتلاء به اسکیزوفرنی توسط خیلیها قابل قبول است،[۳۹] همچنان مورد بحث میباشد.[۲۵][۴۰] آمفتامین، کوکائین، و به میزان کمتر الکل، میتوانند منجر به جنونی که بسیار شبیه به اسکیزوفرنی است شوند.[۳][۴۱] اگر چه به طور کلی علت بیماری تصور نمیشود، اما افراد مبتلا به اسکیزوفرنی نیکوتین بسیار بیشتری نسبت به جمعیت عمومی مصرف میکنند.[۴۲]
عوامل رشد و پیشرفت
عواملی مانند فقدان اکسیژن خون و عفونت، یا استرس و سوء تغذیه مادر در دوران رشد جنین، ممکن است اندکی خطر ابتلاء به اسکیزوفرنی را در مراحل بعدی زندگی افزایش دهند.[۲] به احتمال زیاد افراد مبتلا به اسکیزوفرنی ممکن است در فصل زمستان یا فصل بهار (حداقل در نیمکره شمالی) متولد شده باشند، که ممکن است ناشی از قرار گرفتن زیاد در معرض ویروس در رحم باشد.[۳] این اختلاف حدود ۵ تا ۸٪ میباشد.[۴۳]
مکانیسمها
تلاشهای چندی برای توضیح ارتباط بین تغییر عملکرد مغز و اسکیزوفرنی به مرحله عمل رسیده است.[۲] یکی از شایعترین آنها فرضیه دوپامین میباشد، که نسبت خصیصههای جنون به تفسیر ذهن معیوب از احتراق ناقص نورونهای دوپامینرژیک میباشد.[۲]
روانی
بسیاری از مکانیسمهای روانی در توسعه و بقای اسکیزوفرنی درگیر میباشند. انحرافات شناختی در افرادی که مطلع از خطر هستند یا کسانی که در معرض خطر هستند، به ویژه هنگامی که تحت فشار یا در موقعیتهای گیج کنندهای هستند قابل تشخیص میباشد.[۴۴] برخی از ویژگیهای شناختی ممکن است منعکس کننده فقدانهای عصب شناسی عمومی از جمله از دست دادن حافظه باشند، حال آن که ویژگیهای دیگر ممکن است مربوط به مسائل خاص و تجربیات باشند.[۴۵][۴۶]
علی رغم نمایان شدن فقدان عاطفه، یافتههای اخیر نشان میدهد که بسیاری از افراد مبتلا به اسکیزوفرنی از لحاظ عاطفی، خصوصاً به محرکهای استرس زا یا منفی پاسخگو هستند، و این گونه است که حساسیت ممکن است سبب بروز آسیب پذیری نسبت به اختلال و علائم شود.[۴۷][۴۸] برخی از شواهد نشان میدهد که محتوای باورهای پنداری و تجارب روانی میتواند منعکس کننده علل عاطفی اختلال باشند، و همچنین نشان میدهد که چگونه تعبیر شخص از چنین تجربههایی میتواند در شناخت علائم تأثیر گذار باشد.[۴۹][۵۰][۵۱] استفاده از «رفتارهای مطمئن» برای جلوگیری از تهدیدات فرضی ممکن است کمکی برای توهم مزمن باشد.[۵۲] اکثر شواهد مرتبط با نقش مکانیسمهای روانی ناشی از اثرات روان درمانیها روی علائم اسکیزوفرنی میباشد.[۵۳]
عصبشناسی
اسکیزوفرنی بسته به تفاوتهای ظریف موجود در ساختار مغز میباشد، که در ۴۰ تا ۵۰٪ موارد و در شیمی مغز در حالات جنونی حاد یافت میشود.[۲] بررسیهای برگرفته از تست روانشناسی عصبی و تکنولوژیهای تصویربرداری از مغز مانند FMRI و PET برای بررسی تفاوتهای اجرایی در فعالیت مغز نشان دهنده تفاوتهایی هستند که به نظر میرسد اغلب در لب قدامی مغز هیپوکامپها و لب گیجگاهی رخ میدهند.[۵۴] کاهش حجم مغز، کوچکتر از آنچه در کسانی که مبتلا به بیماری آلزایمر هستند بافت میشود، در مناطقی از قشر پیشانی و لبهای گیجگاهی گزارش شدهاند. معلوم نیست که آیا این تغییرات حجمی تدریجی هستند یا قبل از شروع بیماری به وجود میآیند.[۵۵] این تفاوتها به فقدان شناخت عصبی مرتبط اند که اغلب ابتلاء به اسکیزوفرنی را به همراه دارند.[۵۶] از آنجا که مدارهای عصبی متغیرند، متناوباً پیشنهاد شده است که اسکیزوفرنی را باید به عنوان مجموعهای از اختلالات گسترده عصب تصور کرد.[۵۷]
توجه خاصی نسبت به عملکرد دوپامین در مسیر mesolimbic مغز شده است. توجهات بیش از حد منتج شده از یافتههای تصادفی است که phenothiazine مواد مخدر، که مسدودکننده عملکرد دوپامین است، میتواند علائم روان پریشی را کاهش دهد. این واقعیت وجود دارد که آمفتامینها، که منجر به آزاد شدن دوپامین میشوند، ممکن است علائم روان پریشی در اسکیزوفرنی را تشدید کنند.[۵۸] فرضیه مؤثر دوپامین اسکیزوفرنی پیشنهاد میکند که فعال سازی بیش از حد گیرندههای D۲ علت (علائم مثبت) اسکیزوفرنی بود. اگر چه حدود ۲۰ سال این فرضیه بر اساس اثر مسدود کننده D۲ مشترک در تمام داروهای ضد روان پریشی بنا شد، اما تا اواسط دهه نود که PET و بررسیهای تصویربرداری مقطعنگاری رایانهای تکفوتونی شواهد پشتیبان را تأمین میکردند اثری از آن نبود. فرضیه دوپامین در حال حاضر، تا حدودی تنها به دلیل اینکه تجویز داروهای ضد روان پریشی جدید (تجویز داروی داروهای ضد روان پریشی نامنظم) میتوانند مؤثر تر از تجویز داروهای قدیمی (تجویز دارو داروهای ضد روان پریشی معمولی) باشند ساده تصور میشود، اما عملکرد سروتونین نیز مؤثر واقع میشود و ممکن است اندکی کمتر از دوپامین اثر مسدود کننده داشته باشد.[۵۹]
انتقالدهندهٔ عصبی گلوتامات و کاهش عملکرد گیرنده گلوتامات NMDA در اسکیزوفرنی نیز مورد توجه قرار گرفته است، بیشتر به دلیل کاهش غیر طبیعی سطح گیرندههای گلوتامات یافت شده در مغزهای پس از مرگ کسانی که مبتلا به اسکیزوفرنی هستند،[۶۰] و کشف اینکه داروهای مسدود کننده گلوتامات مانند پنسیلین و کتامین میتوانند مقلد علائم و مسائل شناختی مرتبط با این حالت باشند.[۶۱] کاهش عملکرد گلوتامات به عملکرد ضعیف آزمون الزامی لپ قدامی مغز و عملکرد هیپوکامپ مرتبط میباشد، و گلوتامات میتواند در عملکرد دوپامین، که هر دو در اسکیزوفرنی دخیل شدهاند تأثیر گذار باشد، واسطه مهم (و احتمالاً عملی) نقش مسیرهای گلوتامات در این حالت پیشنهاد میشوند.[۶۲] اما علائم مثبت نسبت به تجویز داروی glutamatergic پاسخگو نیستند.[۶۳]
تشخیص
اسکیزوفرنی یا بر اساس دو معیارهای انجمن روان پزشکی آمریکا «راهنمای تشخیصی و آماری اختلالات روانی»، نسخه DSM-IV-TR، یا سازمان بهداشت جهانی طبقهبندی آماری بینالمللی از بیماریها و مشکلات مرتبط با سلامت، ICD-۱۰ تشخیص داده میشود.[۲] این معیارها از تجارب گزارش شده شخص، گزارش اختلال رفتاری، به دنبال یک ارزیابی بالینی توسط یک متخصص سلامت روانی استفاده میکنند. نشانههای مرتبط با اسکیزوفرنی به طور پی در پی در جامعه رخ میدهد و بسیار سخت میشود به اسکیزوفرنی پی برد.[۳] تا سال ۲۰۰۹ هیچ آزمون عینی وجود ندارد.[۲]
معیارها
معیارهای ICD-۱۰ به طور معمول در کشورهای اروپایی مورد استفاده قرار میگیرند، حال آنکه معیارهای DSM-IV-TR در ایالات متحده آمریکا و سایر نقاط جهان مورد استفاده قرار میگیرند، و در مطالعات پژوهشی متداول هستند. معیارهای ICD-۱۰ تأکید بیشتری بر علائم درجه اول اشنایدری دارند. در عمل، تشابه بین دو سیستم بالا است.[۶۴]
با توجه به نسخه تجدید نظر شده چهارم «راهنمای تشخیصی و آماری اختلالات روانی» (DSM-IV-TR)، برای تشخیص ابتلاء به اسکیزوفرنی، سه معیار مشخص باید در نظر گرفته شود:[۶۵]
-
علائم مشخصه: دو یا چند مورد زیر، که هر یک برای مدت طولانی در طول یک دوره یکماهه وجود دارند (یا کمتر، در صورتی که علائم صرفه نظر از درمان باشند).
- توهمات
- وهم و خیالات
- سخنان آشفته، که جلوهای از اختلال در تفکر رسمی میباشد.
- رفتار به شدت آشفته (مانند نامناسب لباس پوشیدن، اغلب گریه کردن) یا رفتار جنون جوانی
- علائم منفی: تحت تأثیر کم توجهی عاطفی (فقدان یا کمبود در پاسخ عاطفی) قرار گرفتن، عجز گویایی (فقدان و یا کمبود در گفتار)، و یا نداشتن اختیار و اراده (فقدان یا کمبود انگیزه).
- اگر توهمها عجیب و غریب تشخیص داده شوند، یا یک صدای آمیخته با صحبتهای بیمار همزمان با انجام گرفتن اعمال بیمار یا شنیدن دو یا چند صدا که درحال گفتگو با یکدیگر هستند را توهم شنیداری بحساب بیاوریم، تنها علائم بالا کاربرد دارند. ملاک اختلال در سخن زمانی قابل مشاهده است که به اندازه کافی بطور قابل ملاحظه اختلال در ارتباطات شدید باشد.
- اختلال در عملکرد اجتماعی یا شغلی: برای مدت قابل توجهی از زمان شروع اختلال، یک یا چند منطقه عمده از عملکرد مانند کار، روابط بین فردی، یا مراقبت از خود، به طور قابل توجهی پایینتر از سطح به دست آمده قبل از شروع اختلال میباشند.
- طول مدت قابل توجه: علائم مداوم اختلال به مدت حداقل شش ماه ماندگار میباشند. این دوره ششماهه، باید حداقل یک ماه از علائم (و یا کمتر، در صورتی که علائم صرفه نظر از درمان باشند) را کاهش دهد.
اگر نشانههای اختلال برای بیش از یک ماه ولی کمتر از شش ماه نمایان شوند، تشخیص اختلال حالت اسکیزوفرین عملی میباشد.[۶۵] علائم روان پریشی که کمتر از یک ماه به طول میانجامند ممکن است به عنواناختلال روانی کوتاه تشخیص داده شود، و در شرایط مختلف ممکن است به عنوان اختلال روانی غیرقابل تشخیص دستهبندی شود. در صورتی که نشانههای اختلال خلقی به طور قابل ملاحظهای نمایان شوند اسکیزوفرنی قابل تشخیص نمیباشد (گر چه اختلال schizoaffective قابل تشخیص است)، یا اگر نشانههای اختلال پیش رونده فراگیر نمایان شوند مگر این که هذیان یا توهم برجسته نیز وجود داشته باشند، یا اگر علائم مستقیماً نتیجه فیزیولوژیکی شرایط یا موارد یک پزشک عمومی، مانند سوء استفاده از مواد مخدر یا داروها باشند، اسکیزوفرنی قابل تشخیص نمیباشد.
زیر گروهها
DSM-IV-TR شامل پنج زیر گروه اسکیزوفرنی میباشد، گر چه توصیه میشود پیشرفتهترین آن یعنی DSM-5 را از طبقهبندی جدید مجزا کنیم:[۶۶][۶۷]
- نوع پارانویایی (هذیانی): توهمات یا توهمات شنیداری نمایان میشوند، اما اختلال در تفکر، رفتار آشفته، یا تملق عاطفی نمایان نمیشوند. توهمات سرکوب گرانه و / یا پر آب و تاب هستند، اما علاوه بر این، آیتمهای دیگری مانند حسادت، مذهب، و یا شکایت جسمانی نیز ممکن است وجود داشته باشند. (DSM code 295.۳/ICD code F20.0)
- نوع نامنظم: به نام «اسکیزوفرنی جنون جوانی» موجود در ICD معروفند. جایی که اختلال فکری و عاطفه یکنواخت با هم وجود دارند. (DSM code 295.۱/ICD code F20.1)
- نوعی از جنون جوانی: این موضوع ممکن است تقریباً ناشی از بی حرکتی و یا جلوهای از آشفتگی، حرکات بی هدف و بیمورد باشد. علائم میتوانند شامل نداشتن هوشیاری نسبی یا کامل جنون جوانی و انعطافپذیری مومی باشند. (DSM code 295.۲/ICD code F20.2)
- نوع نامشخص: علائم روانپریشی نمایانند، اما معیاری برای انواع پارانوئید، آشفتگی، یا جنون جوانی دیده نمیشود. (DSM code 295.۹/ICD code F20.3)
- نوع باقیمانده: که در آن علائم مثبت فقط در یک حساسیت پایین نمایانند. (DSM code 295.۶/ICD code F20.5)
ICD-۱۰ دو زیر گروه دیگر را معرفی میکند:[۶۷]
- افسردگی پس از اسکیزوفرنی: بروز افسردگی پس از یک بیماری اسکیزوفرنی که در آن سطح پایینی از علائم اسکیزوفرنی هنوز هم ممکن است وجود داشته باشند. (ICD code F20.4)
- اسکیزوفرنی ساده: گسترش بی سر و صدا و پیشرونده علائم شاخص منفی بدون هیچ سابقهای از حالات روانی (ICD code F20.6)
تفاوت
علائم روان پریشی ممکن است در بسیاری از اختلالات روانی دیگر موجود باشند، از جمله اختلال دوقطبی،[۶۸] اختلال شخصیت مرزی،[۶۹] مسمومیت با مواد مخدر و جنون ناشی از مواد مخدر. توهمات («غیر-عجیب و غریب») نیز اختلال توهم، و برداشتهای اجتماعی دراختلال اضطراب اجتماعی، اختلال شخصیت گریزی و اختلال شخصیت موجود هستند. اسکیزوفرنی با اختلال وسواس (OCD) همراه است، به طور قابل توجه بیشتر از آن است که بتوان به صورت شانسی در مورد آن بحث کرد، گر چه وسواسی که در OCD از توهمات اسکیزوفرنی رخ میدهد را به سختی میتوان تشخیص داد.[۷۰]
بیشتر پزشکان عمومی و اعصاب و روان ممکن است ملزم به رد کردن بیماریهای پزشکی شوند که ممکن است به ندرت حاصل از علائمی شبیه اسکیزوفرنی روانی،[۶۵] مانند: آشوب و اضطراب متابولیک، عفونت سیستماتیکی، سفلیس، HIV عفونت، صرع، و ضایعات مغز باشند. ممکن است رد کردنهذیان، که میتواند نشانه توهمات دیداری، شروع حاد و متغیر سطح هوشیاری، و نشانه بیماری زمینهای باشد لازم باشد. تحقیقات به طور کلی به منظور عود کردن تکرار نمیشوند مگر اینکه نشانه «طبی» خاصی باشد یا ممکن است عوارض جانبی از دارو ضد جنون وجود داشته باشد.
پیشگیری
در حال حاضر شواهد و مدارک مبتنی بر اثر بخشی مداخلات زودرس برای جلوگیری از اسکیزوفرنی بی نتیجه است.[۷۱] حال آنکه شواهدی وجود دارد که مداخلهٔ زودهنگام در آنهایی که با یک فقره بیماری روانی همراه هستند ممکن است در کوتاهمدت نتایج بهبودشان را مهیا سازند، پس از پنج سال بهرهمندی کمی از این اقدامات وجود دارد.[۲] تلاش برای جلوگیری از اسکیزوفرنی در مرحله علائم اولیه بیماری مطمئناً سودمند نمیباشد و به همین دلیل از سال ۲۰۰۹ توصیه نمیشود.[۷۲] پیشگیری در صورت نبودن نشانههای قابل اعتماد بعد از پیشرفت بیماری دشوار است.[۷۳] با این حال، برخی از موارد اسکیزوفرنی میتواند به تعویق بیفتد یا احتمالاً با تشویق به پرهیز کردن از مصرف حشیش، به ویژه در میان جوانان میتواند به تعویق بیفتد.[۷۳] افراد با سابقه خانوادگی اسکیزوفرنی ممکن است بیشتر در معرض خطر ابتلاء به جنون ناشی از حشیش باشند.[۳۹] و، یک پژوهش نشان داد که اختلالات روانی ناشی از حشیش در حدود نیمی از موارد پیشرفت شرایط روانی مداوم را به دنبال دارد.[۷۴]
تحقیقات نظری دنباله رو استراتژیهایی هستند که ممکن است بیماری اسکیزوفرنی را کاهش دهند. به دنبال یک روش برای درک آنچه در سطح ژنتیک و عصبی اتفاق میافتد تا یک بیماری به حساب بیاید، به طوری که مداخلات زیست پزشکی میتوانند گسترده شوند. با این حال، آثار متعدد و متنوع ژنتیکی به هر اندازه که کوچک باشند، تعامل با محیط زیست را با مشکل مواجه میکنند. متناوباً، استراتژیهای [بهداشت عمومی]] میتوانند عوامل انتخابی اقتصادی و اجتماعی باشند که در گروههای خاص به میزان بالایی از اسکیزوفرنی، به عنوان مثال در ارتباط با مهاجرت، قومیت یا فقر، به هم مرتبط هستند. گروه گستردهای از استراتژیها میتوانند از خدمات مربوط به اطمینان از حاملگی سالم و رشد سالم، از جمله در مناطق توسعه روانی مانند شناخت اجتماعی حمایت کنند. با این حال، به اندازه کافی شواهد و مدارکی دال بر اجرای ایدههایی که در زمان فعلی وجود دارند، و تعدادی از مسائل گستردهتری که مختص اسکیزوفرنی باشند موجود نیست[۷۵][۷۶]
مدیریت
درمان اولیه اسکیزوفرنی، مصادف با مصرف داروهای آنتی سایکوتیک میباشد، که اغلب با ترکیبی از حمایتهای روانی و اجتماعی همراه هستند.[۲] بستری شدن در بیمارستان ممکن است برای موارد وخیم یا به طور داوطلبانه یا (در صورتی که قانون سلامت روانی به آن اجازه دهد) اجباری صورت پذیرد. بستری شدن طولانی مدت از مان شروع غیر نهادینه کردن در سالهای دهه ۱۹۵۰ غیر طبیعی میباشد، هر چند هنوز هم اتفاق میافتد.[۴] ارتباطات خدمات پشتیبانی از جمله سر زدن به مراکز، بازدید توسط اعضای جامعه بهداشت روانی، حامیان اشتغال[۷۷] و پشتیبانی از گروهها، عادی میباشد. برخی از شواهد نشان میدهد که ورزش منظم دارای اثرات مثبتی بر سلامت جسمی و روانی افراد مبتلا به اسکیزوفرنی میباشد.[۷۸]
درمان های تکنولوژیک
درمان با TMS تقريباً بيش از هشت سال است كه محققين درمان اختلال اسكيزوفرنيا با TMS بكارمي برند. اين روش بيشتر در مواردي آزمايش شده است كه بيماران داراي توهمات مقاوم بوده اند ويا به درمان هاي دارويي پاسخ نمي دادند. خاستگاه به كارگيري اين روش به مطالعاتي برمي گردد كه نشان مي دهند اين نوع مداخله جديد در اختلالات خلقي موثر است. چندين مطالعه نشان داده اند كه TMS در قشر پيش پيشاني نيمكره چپ همان اثراتي را توليد مي كندكه داروهاي ضدافسردگي ايجاد مي كنند. افزون بر اين، طبق شواهد مختلف، اثربخشي اين رويكرد درماني در اختلالاتي نظيروسواس فكري- عملي و اختلال استرس پس از سانحه و شيدايي نيز نشان داده شده است. TMS براي نشانگان منفي اسكيزوفرنيا نشانگان منفي اسكيزوفرنيا مرتبط با نقص در عمل رد اجرايي است و جزء آن دسته از علايمي است كه به داروهاي نورولپتيك بسيار كند جواب مي دهد. همچنين علائم منفي به داروهاي ضد روان پريشي نسل اول )نظير هالوپردول، تريفلوپرازين،كاربافازپن و...( جواب نمي دهند عليرغم اينكه داروهاي ضدروانپريشي غير كلاسيك نيز تا حدي مي تواند اين علائم را كنترل كند ولي اثر واقعي آنها بر چنين علايمي هنوز مبهم و ناشناخته است. به هر ترتيب با استفاده از (TMS) مي توان آن نواحي از قشر پيشاني را كه در به وجودآمدن اين علايم نقش داشته اند تحريك مغناطسي نمود. تصاوير به دست آمده از مغز بيماران اسكيزوفرنيا نشان داده است كه در ايجاد علايم منفي، كاهش فعاليت در منطقه قشر مخ نيمكره چپ به چشم مي خورد. در واقع منطق زيربنايي درمان از طريقTMS براي علايم منفي اسكيزوفرنيا به اين مي پردازدكه چون در اين منطقه ازكرتكس يك فعاليت پايين را شاهد هستيم لذا تحريك از طريق فركانس بالا سبب فعاليت نوروني مي شود. TMS براي نشانگان مثبت اسكيزوفرنيا توهم، هذيان، گفتار عجيب و غريب، اختلال در فكر، در زمره علايم مثبت اسكيزوفرنيا محسوب مي شود. در ميان علايم مثبت اين بيماري بيش ترين مطالعات بر روي توهم به خصوص )شنيداري(انجام شده است. توهم شنيداري در ميان 50-70 درصد از بيماران اسكيزوفرنيا ديده مي شود. معمولاً درمان هايي مبتني بر دارو به صورت كامل انجام نمي شود ويا علي رغم مصرف دارو بيمار همچنان اين توهمات را دارد. اين توهمات مي تواند سبب پريشاني، ناتواني كاركرد يا عدم كنترل بر رفتار شود. اسكيزوفرنيا در خصوص اثر بخشي rTMS بر علايم اسكيزوفرنيا نيز شواهدي وجود داردكه نشان مي دهد اين شيوه بر علايم منفي و توهمات شنيداري در افراد مبتلا موثر است. به طور مثال در مقاله اي كه در سال 2004 ارايه شده، نشان داده شده قريب به اثر مطالعات حاكي از تاثير rTMS بر بهبود علايم فوق بوده اند.[۷۹]
دارو
راه اول برای درمان اختلال روانی مرتبط با اسکیزوفرنی تجویز داروی ضد روان پریشی است،[۸۰] که میتواند علائم مثبت روان پریشی را در حدود ۷–۱۴ روز کاهش دهد. داروهای ضد روان پریشی، به هر حال، به میزان قابل توجهی نسبت به بهبود علائم منفی و اختلال در شناخت ضعیف میباشند.[۲۲][۸۱] استفاده دراز مدت از این دارو، خطر عود را کاهش میدهد.[۸۲]
انتخاب داروی ضد روان پریشی برای مصرف بر اساس منافع، خطرات و هزینهها میباشد.[۲] جای بحث دارد که کدام دسته بهتر هستند، معمولی یا داروهای ضد روان پریشی نامنظم.[۸۳] در زمانی که داروهای ضد روان پریشی معمولی به مقدار کم نسبت به متوسط دفعات و مقدار دوزهای مصرف دارو مورد استفاده قرار میگیرند، هر دو دارو به یک اندازه علائم افت یا عود را نشان میدهند.[۸۴] در ۴۰ - ۵۰٪ از افراد خوب جواب میدهد، در ۳۰ - ۴۰٪ از افراد نسبتاً جوابگو میباشد، و در ۲۰٪ از افراد باعث مقاومت در برابر درمان شده است (از بین رفتن علائم، بعد از شش هفته با توجه به دو یا سه داروی ضد روان پریشی مختلف به طور رضایت بخشی پاسخگو میباشد).[۲۲] Clozapine (کلوزاپین) برای کسانی که پاسخ ضعیفی نسبت به داروهای دیگر دارند درمان مؤثری است، اما احتمال عوارضجانبی وخیمی نسبت به agranulocytosis (آگرانولوسیتوز) دارد (کاهش تعداد سلولهای سفید خون در ۱–۴٪).[۲][۳][۸۵]
توجه داشته باشید که عوارض جانبی داروهای ضد روان پریشی معمولی میزان بیشتری ازعوارض جانبی اکستراپیرامیدال را به دنبال دارند در حالی که داروهای ضد روان پریشی نامنظم افزایش قابل توجه وزن، دیابت و خطر ابتلاء به سندرم متابولیک را به دنبال دارند.[۸۴]حال آن که داروهای ضد روان پریشی نامنظم عوارض جانبی اکستراپیرامیدال کمتری دارند که این اختلافات نسبتاً کم میباشند.[۸۶]برخی از داروهای ضد روان پریشی نامنظم از قبیل quetiapine (کویتاپین) و risperidone (ریسپریدون) نسبت به داروهای روان پریشی معمولی perphenazine (پرفنازین) با خطر جدی مرگ همراه هستند، در حالی که clozapine (کلوزاپین) با کمترین خطر مرگ همراه است.[۸۷] هنوز مشخص نیست که آیا داروهای ضد روان پریشی جدید شانس ابتلاء به سندرم نورولپتیک بدخیم، که یک اختلال عصبی نادر ولی جدی است را کاهش میدهند یا خیر.[۸۸]
برای افرادی که مایل یا قادر به اخذ دارو به طور منظم، نیستند، انبار پی در پی تدارکات داروهای ضد روان پریشی ممکن است به منظور کنترل نظارت مورد استفاده قرار بگیرند.[۸۹] آنها به نسبت زیادی خطر مربوط به داروهای خوراکی را کاهش میدهند.[۸۲] هنگامی که در ترکیب با اختلالات روانی استفاده میشوند، ممکن است پیوسته در دراز مدت درمان را بهبود دهد.[۸۹]
روانی اجتماعی
شماری از مداخلات روانی اجتماعی ممکن است در درمان اسکیزوفرنی مفید باشند که عبارتند از: خانواده درمانی،[۹۰] ارتباط درمانی مثبت، اشتغال، بازسازی شناخت،[۹۱] آموزش مهارت درمان شناخت رفتاری (CBT)، مداخلات اقتصادی اعتباری، و مداخلات روانی اجتماعی به منظور مواد مصرفی و کنترل وزن.[۹۱] خانواده درمانی یا آموزشی، که کل سیستم خانواده را نسبت به یک فرد، مخاطب قرار دهد، ممکن است عود شدن بیماری و بستری شدن در بیمارستان را کاهش دهد.[۹۲] شواهد و مدارک مؤثر CBT در مورد کاهش علائم یا جلوگیری از عود کردن بیماری اندک میباشد.[۹۳][۹۴] هنر یا درام درمانی به خوبی مورد تحقیق قرار نگرفته است.[۹۵][۹۶]
پیشبینی
اسکیزوفرنی هزینههای جانی و مالی بسیاری دارد.[۲] اسکیزوفرنی به کاهش امید به زندگی از ۱۲ - ۱۵ سال منتج میشود، در درجه اول به دلیل به همراه داشتن چاقی، بی حرکتی در طول زندگی روزمره، و سیگار کشیدن، افزایش میزان خودکشی نقش کمتری را ایفا میکند.[۲] این تفاوتها در امید به زندگی بین سالهای s۱۹۷۰ و s۱۹۹۰ افزایش یافته است،[۹۷] و بین سال۱۹۹۰s و دهه اول قرن ۲۱st تغییر قابل ملاحظهای در نظام سلامت با در دسترس بودن مراقبتهای گسترده نداشته است (فنلاند).[۸۷]
اسکیزوفرنی یکی از علل عمده ناتوانی است، با فعال شدن جنون به سه دسته بیشترین ناتوانی پس از quadriplegia و جنون و در صدر آن paraplegia و کوری تقسیم بندی میشود.[۹۸] حدود سه چهارم از افراد مبتلا به اسکیزوفرنی همراه با عود کردن بیماری از ناتوانی مداومی برخوردارند.[۲۲] برخی از مردم به طور کامل بهبود مییابند و دیگران برخوردهای خوب و مناسبی در جامعه دارند.[۹۹] بسیاری از افراد مبتلا به اسکیزوفرنی، به طور مستقل با پشتیبانی جامعه زندگی میکنند.[۲] در افراد مبتلا به جنون با توجه به قسمت اول در ۴۲٪ موارد از نتیجه خوبی در دراز مدت، نتیجه متوسط در ۳۵٪ و یک نتیجه ضعیف در ۲۷٪ برخوردارند.[۱۰۰] به نظر میرسد نتایج بدست آمده مرتبط با اسکیزوفرنی در در حال توسعه نسبت به کشورهای توسعه یافته بهتر است.[۱۰۱] با این حال، این نتیجهگیریها، زیر سؤال رفتهاند.[۱۰۲][۱۰۳]
یک نرخ خودکشی بیش از حد متوسط در افراد مبتلا به اسکیزوفرنی موجود میباشد. این مهم ۱۰٪ ذکر شده است، اما اکثر تحلیلهای اخیر مطالعاتی و آماری در یک تجدید نظر ۴٫۹٪ برآورد کردهاند، که اغلب در دوران پس از شروع یا اولین زمان بستری شدن در بیمارستان اتفاق میافتد.[۱۰۴] در اکثر مواقع بیش از (۲۰ تا ۴۰ درصد) حداقل یک بار اقدام به خودکشی میکنند.[۱۰۵][۱۰۶] انواع مختلفی از عوامل خطر وجود دارد، از جمله جنس مذکر، افسردگی، و بهره هوشی بالا.[۱۰۵]
اسکیزوفرنی و سیگار کشیدن یک ارتباط تنگاتنگ در مطالعات سراسر جهان از خود نشان دادهاند.[۱۰۷][۱۰۸] مصرف سیگار در افراد مبتلا به اسکیزوفرنی بسیار شایعتر از سایر افراد است. ۸۰٪ تا ۹۰٪ این بیماران سیگار میکشند در حالیکه تنها ۲۰٪ از جمعیت عمومی سیگاری هستند.[۱۰۸] همچنین اسیکزوفرنهای سیگاری علاقه بیشتری به سیگار کشیدن دارند و از سیگارهای با نیکوتین بالا را ترجیح میدهند.[۱۰۶]
نظریه قابل قبولی در مورد دلیل شیوع مصرف سیگار در این بیماران وجود ندارد. برخی فرضیات مصرف سیگار در این افراد را نوعی خوددرمانی برای کاهش استرس و تنظیم تفکر و یا کاهش عوارض جانبی داروهای ضد اسکیزوفرنی میدانند اما از سوی دیگر اثرات منفی سیگار میتواند در مجموع نتیجه بدتری برای این بیماران داشته باشد. با توجه به اینکه مدارک موجود در مورد آسیبها و منافع سیگار کشیدن ضدونقیض است در مورد نحوه برخورد با سیگار کشیدن این بیماران اختلاف نظر است. به طور تاریخی روانپزشکان این بیماران را از سیگار کشیدن منع نمیکنند و معتقدند افرادی که به مشکلات جدی ذهنی مبتلا هسنند و استرس و فشارهای شدید را تحمل میکنند حق سیگار کشیدن را به عنوان یک فعالیت لذتبخش هرچند مخرب دارند. در برخی موارد نیز در بیمارستانهای روانی سیگار به عنوان یک جایزه و محرومیت از سیگار به عنوان یک تنبیه در نظر گرفته میشود. اما تحقیقات جدیدی که منفعت ترک سیگار در طولانی مدت را نشان میدهد موجب شده تا اکنون ایده مخالفت با مصرف سیگار نظریه غالبتری باشد. با این حال هرچند در حال حاضر در بیشتر کلینیکهای سلامت روانی قطع سیگار یک هدف است اما در مورد شیوه موفق رسیدن به این هدف تحقیقات قابل قبولی انجام نشده است. همجنین در تحقیقاتی که بعد از قطع سیگار انجام شده نشانهای حاکی از تاثیر قطع سیگار بر بهتر شدن یا بدتر شدن این بیماران دیده نشدهاست.[۱۰۹]
برخی از شواهد نشان میدهد که احتمالاً اسکیزوفرنی پارانویید نسبت به انواع دیگر اسکیزوفرنی به منظور زندگی مستقل و عملکرد شغلی چشم انداز بهتری دارد.[۱۱۰]
اپیدمیولوژی (همهگیرشناسی)
|
no data ≤ 185 185–197 197–207 207–218 218–229 229–240
|
240–251 251–262 262–273 273–284 284–295 ≥ ۲۹۵
|
حدود ۰٫۳–۰٫۷٪ از افراد در برخی از مراحل زندگی خود[۲] یا ۲۴ میلیون نفر در سراسر جهان تا سال ۲۰۱۱ تحت تأثیر اسکیزوفرنی قرار میگیرند،[۱۱۱] اسکیزوفرنی غالباً در مردان ۱٫۴ برابر بیشتر از زنان و به طور معمول در مردان زودتر رخ میدهد[۳]- اوج سن شروع، ۲۰ - ۲۸ سال برای مردان و ۲۶ - ۳۲ سال برای زنان است.[۱۱۲] در بدو دوران کودکی بسیار نادرتر از،[۱۱۳] بدو میان سالی – کهنسالی میباشد.[۱۱۴] علیرغم دانش دریافت شده مبنی بر اینکه اسکیزوفرنی با نرخ مشابهی در سراسر جهان رخ میدهد، شیوع آن در سراسر جهان متفاوت است.
بیماران مشهور
۱.جان فوربز نش. ۲.ریچارد براتیگان. ۳.اد گین. ۴.بادی بولدن. ۵.سید برت. ۶.کرت کوبین
پیشینه
علایم این بیماری در گذشتههای دور نیز شناخته شده بود؛ ولی پیشینیان تعبیرهای اسطورهای برای آن داشتند.در گذشته ها مردمان قدیم عقاید اسطوره ای نسبت به این بیماری داشتند که امروزه این عقاید تغییرات زیادی کرده است. در گذشته به روانگسیختگی ((جنون جوانی)) میگفتند که امروزه چندان مورد پسند روانپزشکان و روانشناسان نیست.[۱۱۵][۱۱۶] پیشینیان میگفتند دیوانه کسی است که دیو را میبیند و مجنون کسی است که جن را میبیند. این همان روانگسیختگی است. روانگسیختگی نوعی از بیماری است که بیمار موجودی را میبیند که دیگران نمیبینند و مردم به این دلیل که آن موجود مورد ادعا را نمیبینند به فردی که آن موجود را میبیند مجنون یا دیوانه میگویند. به این بیماری در قدیم دیوانگی یا جن زدگی یا آل زدگی میگفتند.
در قرن نوزدهم پزشکان این بیماری را به عنوان جنون و دیوانگی محض میانگاشتند و در اوسط همین قرن بندیکت اوگوستن مورل برای اولین بار به توصیف این بیماری در کتاب خود پرداخت و از آن به عنوان «توقف ناگهانی تمام قوای روحی» یاد کرد. این بیماری در آن زمان اغلب در دسته هیستری به شمار میرفت و به آن هیستری گیج و منگ میگفتند.[۱۱۷]
در اواخر قرن نونزدهم امیل کرپلین، روانپزشک آلمانی، این بیماری را جنون زودرس نامید که به فراگیری این بیماری نزد جوانان و نوجوانان باز میگشت. در نهایت اُیگِن بلویلر، روانپزشک سوئیسی، کلمه اسکیزوفرنی را در جهت دفاع از روانکاوی فروید ابداع کرد و به تعریف عوارض این بیماری پرداخت. فروید لفظ پارافرنی را برای این بیماری مناسب تر میدانست.
ادامه مطلب
| کژپشتی | |
|---|---|

رادیوگرافی از یک کژپشتی
|
|
| آیسیدی-۱۰ | M41 |
اگر در یک فرد سالم ستون مهرهها را از روبرو یا پشت نگاه کنید به صورت یک خط راست دیده میشود. بیماری کَژپُشتی یا اسکولیوز (به انگلیسی: Scoliosis) انحراف جانبی ستون مهرهها (به راست یا چپ) میتواند به علت ناهنجاری مادرزادی (مثلاً نوروفیبروماتوز) یا اسکولیوز اکتسابی (مثلاً بیماری راشیتیسم) ایجاد شود.
اختلال در عملکرد عضلات که ماهیچهآسیبی (میوپاتی) خوانده میشود به نوع خاصی از کژپشتی منجر میشود که به آن کژپشتی ماهیچهآسیبی Myopathic میگویند. دیستروفیهای عضلانی جزو این گروه قرار میگیرند.
ممکن است کژپشتی به علت اختلال عملکرد عصب ایجاد شود که بنام کژپشتی عصبآسیبی Neuropathic شناخته میشود.
مسئله مهمی که باید در انحراف جانبی ستون فقرات توجه داشته باشیم این است که جهت حرکت زوائد خاری spinous processes به سمت تقعر میباشد درحالیکه دندهها و جسم مهرهها برخلاف زواید خاری چرخشی به طرف تحدب دارند. این پدیده (چرخش دندهها به سمت تحدب) باعث ایجاد برجستگی در سمت تحدب میگردد که به آن کوهان خلفی posterior hump گفته میشود.
محتویات
انواع
به هرگونه انحراف ستون فقرات کژپشتی میگویند که به دو صورت C و S وجود دارد. در نوع C یک قوس و در نوع S دو قوس غیرنرمال ایجاد میشود. میزان قوس در افراد مبتلا به این بیماری متفاوت میباشد که خود این مسئله نوعی از درجهبندی را ایجاد میکند. در کژپشتی به دلیل عدم قرینگی و غیرطبیعی بودن ستون فقرات، نیروهای وارده به آن حتی درصورت طبیعی بودن باعث فشار به عضلات، رباطها، دیسکهای بین مهرهای و مفاصل بین مهرهای پشتی Facet Joints میگردد و درنتیجه منجر به تشدید درد در ستون فقرات بهویژه ناحیه کمر میشود.
البته طبقهبندی کژپشتی به دو صورت غیرساختمانی Mobile و ساختمانی Fixed نیز ممکن است که جهت نوع درمان مهم است. در نوع غیرساختمانی که برگشتپذیر نیز خوانده میشود درصورت خم کردن تنه به جلو و یا دراز کشیدن اصلاح میشود. وضعیتهای نادرست، کمردردها ی شدید به خصوص فتق دیسک، برخی از تومورها و اختلاف طول اندامها میتوانند این حالت را ایجاد کنند. در نوع ساختمانی برخلاف نوع غیرساختمانی در حالت خم شدن به جلو انحراف و قوس ازبین نمیرود. اسکولیوز ساختمانی به دلیل نقص عضو، برخی از بیماریهای عضلانی، بعضی از ناهنجاریها ی مادرزادی، بیماریهای عصبی (فلج مغزی، پولیومیلبت، سیرنگومیلی و...) و گهگاه به دلایل ناشناخته[۱] در کودکان، نوجوانان و جوانان به وجود میآید.
کژپشتی با توجه به نوع آن، میزان انحراف، سن بیمار و... نیاز به وسایل کمکی، فیزیوتراپی و یا عمل جراحی دارد. این بیماری که بیشتر در دختران نوجوان پدید میآید علل مختلفی دارد که شایعترین آن کژپشتی ناشناختهعلت Idiopathic میباشد.
درمان
درمان این بیماری به دو روش میباشد: درمان جراحی و درمان غیر جراحیکه درمان غیر جراحی شامل فیزیوتراپی و بریس میباشد.
بیمارانی که نیاز به عمل جراحی دارند شامل:
-اگر در سن رشد میزان انحراف بیشتر از ۴۰ درجه باشد
-اگر انحراف جانبی در سنین رشدی به صورت پیشرونده ادامه یابد
-اگر بیشتر از ۵۰ درجه پس از پایان رشد باشد
جستارهای وابسته
پانویس
- Idiopathic
منابع
- واژههای مصوب فرهنگستان زبان وادب فارسی
- ناصری، نسرین، فیزیوتراپی در ضایعات ارتوپدیک، انتشارات صبح سعادت، چاپ اول، شابک:۴–۷–۹۳۴۰۸–۹۶۴
- اعلمی هرندی، بهادر، اصول ارتوپدی و شکسته بندی، چاپ ششم، نشر فروغ اندیشه
ادامه مطلب
| اسکوروی | |
|---|---|
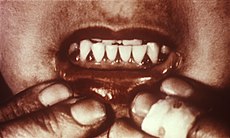
زخم و اسفنجی شدن لثهها از علایم اسکوروی است.
|
|
| آیسیدی-۱۰ | E54 |
| آیسیدی-۹ | 267 |
| اُمیم | 240400 |
| دادگان بیماریها | 13930 |
| مدلاین پلاس | 000355 |
| ایمدیسین | med/2086 derm/521 ped/2073 radio/628 |
| سمپ | D012614 |
اسکوروی (به انگلیسی: Scurvy) یک بیماری است که در اثر کمبود ویتامین ث، که در سنتز و ساخت کلاژن نقش دارد، به وجود میآید. نام شیمیایی این ویتامین، اسید اسکوربیک، از ریشهٔ لاتین واژهٔ اسکوروی، اسکوربوتوس (Scorbutus) گرفته شده است. در گذشته، در زبان فارسی، به این بیماری اسقربوط نیز گفته میشد، که از زبان عربی گرفته شده است.
اسکوروی موجب ظاهر شدن لکههایی بر روی پوست، اسفنجی شدن لثهها و خونریزی غشاهای مخاطی میشود. لکهها بر روی رانها و پاها بیشتر ظاهر میشوند. افراد مبتلا به اسکوروی رنگپریده و افسرده هستند، و ممکن است دچار فلجی یک یا چند عضو شوند. در اسکوروی پیشرفته، زخمها باز شده، چرک میکنند، دندانها میافتند، و سرانجام، در صورت عدم درمان، فرد میمیرد.
در گذشته اسکوروی در میان ملوانان و دزدان دریایی که مدتهایی طولانی در سفر بودند و به میوه و سبزیجات دسترسی نداشتند بسیار شایع بود.
اغلب جانوران دچار اسکوروی نمیشوند، چرا که بدن آنها قادر به ساخت ویتامین ث است. انسان و سایر نخستیها، خوکچههای هندی، و چند گونهٔ دیگر فاقد آنزیمی هستند که ساخت این ویتامین را ممکن میسازد، و باید آن را از طریق رژیم غذایی خود دریافت کنند. ویتامین ث در بسیاری از بافتهای گیاهی یافت میشود. مرکبات، گوجه، سیبزمینی، کلم و فلفل سبز منابعی سرشار از ویتامین ث هستند.
محتویات
تاریخچه
به نظر میرسد که بقراط (۴۶۰ پ.م.-۳۸۰ پ.م.) نخستین کسی بوده است که این بیماری را توصیف کرده است. با این وجود توصیفاتی از یک بیماری در پاپیروس ابرس (حدود ۱۶۰۰ پ.م.) وجود دارد که بسیار به اسکوروی شباهت دارد[۱]. در دوران پیشاتاریخی درمانهای گیاهی برای این بیماری در میان برخی تمدنها شناخته شده بود.
در قرن سیزدهم اسکوروی در میان جنگجویان اروپایی شایع بود. این بیماری یکی از عوامل محدودکنندهٔ سفرهای دریایی بود، چرا که تعداد زیادی از سرنشینان و کارکنان کشتی در سفرهای دراز مدت تلف میشدند. این موضوع حتی در جنگ جهانی اول نیز تأثیر داشت.
در سال ۱۵۳۶، ژاک کارتیه، مکتشف فرانسوی که در حال اکتشاف رودخانهٔ سن لوران بود، با استفاده از دانش بومی آن منطقه مردان خود را که به اسکوروی دچار بودند از مرگ نجات داد. او با استفاده از برگهای سوزنی یک نوع درخت، چایی درست کرد که بعدها ثابت شد دارای ۵۰ میلیگرم ویتامین ث در هر ۱۰۰ گرم است.
در سال ۱۶۱۴، جان وودال، جراح کمپانی هند شرقی بریتانیا، در کتابی که برای شاگردان خود نوشته بود، اسکوروی را یک مشخصهٔ کمبود توصیف کرد و درمان آن را غذای تازه در صورت امکان، و در غیر این صورت پرتقال، لیموترش، لیمو سبز، تمر هندی و حتی در مواقع ضروری اسید سولفوریک دانست.
در دهه ۱۷۴۰، دریادار آنسون ناخدای ناوگان دریایی که در اقیانوس آرام درگیر جنگ با اسپانیا بود، طی سفر دریایی ۶۲۶ نفر از ۹۶۱ نفر از افراد خود را بر اثر بیماری اسکوروی از دست داد. در سال ۱۷۴۷، جیمز لیند، پزشک نیروی دریایی سلطنتی بریتانیا، طی آزمایشی ثابت کرد که اسکوروی با مصرف مرکبات در رژیم غذایی درمان میشود.
جیمز کوک (۱۷۶۸-۱۷۷۱) توانست دور دنیا را با کشتی بزند، بدون آن که حتی یک نفر از کارکنان کشتی او از اسکوروی تلف شوند. البته رژیم غذایی آنان فاقد مرکبات بود، چرا که نگاه داشتن این میوهها در سفرهای طولانی ناممکن بود. به علاوه، پختن غذاها موجب از بین رفتن بیشتر ویتامین ث میشد. بازپُرسازی کشتی از غذاهای تازه و عدم مصرف چربیها برای تمیز کردن ظروف مسی (زیرا چربیها در مجاورت مس داغ دارای ترکیبی میشوند که موجب اختلال در جذب ویتامینها میشود.) مؤثرترین اقدامات کوک در این رابطه بود.
در سال ۱۹۲۷، آلبرت سنت گیورگیی، بیوشیمیست مجارستانی که در سال ۱۹۳۷ برندهٔ جایزه نوبل فیزیولوژی و پزشکی شد، مولکول اسید اسکوربیک را از کلم، پرتقال و فلفل سبز مجزا کرد. سرانجام در سال ۱۹۳۲، چارلز گلن کینگ، محقق آمریکایی، ارتباط میان اسید اسکوربیک (ویتامین ث) و بیماری اسکوروی را کشف کرد.
علت
|
|
این نوشتار نیازمند بررسی متخصص است. |
مولکول اسید اسکوربیک در بسیاری از واکنشهای بیوسنتز، از جمله واکنشهای هیدروکسیلاسیون و آمیداسیون نقش دارد. در سنتز کلاژن، اسید اسکوربیک برای ایجاد ۳ رشتهٔ مارپیچی کلاژن که موجب حفظ ساختار بافتها است لازم میباشد. این مولکول به عنوان یک آنتیاکسیدان عمل میکند. به این ترتیب، گروههای پرولین و لیزین کلاژن توسط یک مولکول دیاکسیژن دچار هیدروکسیلاسیون میشوند، و باعث حفظ ساختار رگها میشوند. در واقع، تنها یک اتم اکسیژن در واکنش هیدروکسیلاسیون یک اسید آمینه شرکت میکند، و اتم دیگر به صورت یک رادیکالهای آزاد باقی میماند. این اتم یک اکسیدکنندهٔ (اکسیدان) قوی است، و موجب سست شدن مویرگهای لثه میشود. دو اتم هیدروژن آزاد شده توسط مولکول اسید اسکوربیک با این اتم اکسیژن واکنش داده و مولکول آب تولید میکنند. به این ترتیب، از بروز اسکوروی جلوگیری میشود.
در صورت کمبود ویتامین ث، تکاتم اکسیژن موجب سست شدن بافت لثه و خونریزی آن میشود.[۱]
همهگیری
امروزه اسکوروی بیشتر در کشورهای دچار فقر و قحطی شایع است. طبق گزارش سازمان بهداشت جهانی در سال ۲۰۰۰، اسکوروی یکی از شایعترین بیماریهای سوءتغذیه در جهان است.
در سایر کشورها، اسکوروی در بزرگسالان نادر است و بیشتر در کودکان و افراد مسن دیده میشود. نوزادانی که شیر پاستوریزه مصرف میکنند، در صورتی که ویتامین ث را به صورت مکمل دریافت نکنند، ممکن است دچار اسکوروی شوند، چرا که ویتامین ث شیر طی عمل پاستوریزه شدن از بین میرود. شیر مادر، در صورتی که تغذیهٔ سالم داشته باشد، حاوی ویتامین ث مورد نیاز نوزاد است.
همچنین، پختن غذا موجب از بین رفتن ویتامین ث میشود.
علایم
ورمهایی در بازوها و پاها و خستگی از علایم ابتدایی بیماری هستند. پس از مدتی، بافت غشاهای مخاطی بینی و لثه سست و اسفنجی شده و دچار خونریزی میشود. همچنین، لکههایی بر روی پوست ظاهر میشوند. در اسکوروی پیشرفته، زخمها باز شده، چرک میکنند، دندانها شل شده و سپس میافتند. بیمار دیگر قادر به ایستادن نخواهد بود و سرانجام، از شدت خستگی یا عفونت میمیرد. [۱]
جلوگیری و درمان
اسکوروی به کمک رژیم غذایی حاوی ویتامین ث درمان میشود، و جلوگیری از آن نیز از همین طریق صورت میگیرد. مرکبات، کیوی، پاپایا، گوجه و توت فرنگی میوههایی سرشار از ویتامین ث هستند. هویج، فلفل دلمهای، بروکلی، سیبزمینی، کلم، اسفناج و پاپریکا نیز منابعی از این ویتامین هستند.
همچنین، جگر گوساله و صدف خوراکی دارای ویتامین ث هستند. علاوه بر این غذاها، ویتامین ث به صورت مکمل (مثلاً به شکل قرص) نیز وجود دارد.
پانویس
- «ویکیپدیای فرانسه» (فرانسوی). بازبینیشده در ۲ مه ۲۰۰۹.
منابع
- «ویکیپدیای انگلیسی». بازبینیشده در ۲ مه ۲۰۰۹.
ادامه مطلب
| اسکلروز جانبی آمیوتروفیک | |
|---|---|
| اُمیم | ۱۰۵۴۰۰ |
| دادگان بیماریها | ۲۹۱۴۸ |
| مدلاین پلاس | 000688 |
| ایمدیسین | neuro/۱۴ |
| پیشنت پلاس | اسکلروز جانبی آمیوتروفیک |
| سمپ | D۰۰۰۶۹۰ |
بیماری اسکلروز جانبی آمیوتروفیک (به انگلیسی: Amyotrophic lateral sclerosis) (به صورت مخفف: ALS) یا بیماری لو گهریگ (به انگلیسی: Lou Gehrig's Disease) یک بیماری نورونهای حرکتی یا (MND یا Motor Neuron Disease) است که موجب تخریب پیشرونده و غیرقابل ترمیم در دستگاه عصبی مرکزی (مغز و نخاع) و دستگاه عصبی محیطی میشود. اسکلروز جانبی آمیوتروفیک شایعترین بیماری نورونهای حرکتی (MND) میباشد؛ بنابراین این بیماری هم علایم نورون محرکه فوقانی و هم نشانههای نورون محرکه تحتانی را ایجاد میکند. در حقیقت در ALS نشانههای فلج مرکزی و محیطی تواماً ایجاد میشود.
این بیماری منجر به از دست رفتن تدریجی عملکرد عضلات (به ویژه عضلات مخطط) میگردد و با تضعیف ماهیچهها بتدریج فرد به فلج عمومی مبتلا میشود. به طوری که توانایی هرگونه حرکتی از شخص سلب خواهد شد. معمولاً مبتلایان به این بیماری مدت زمان زیادی زنده نمیمانند. اگر چه این مدت برای استیون هاوکینگ بین ۲ تا ۳ سال پیشبینی شده بود، اما او علیرغم همه مشکلات و ناراحتیها همچنان به زندگی خود ادامه میدهد و برای فرارسیدن مرگ لحظهشماری نمیکند. بیماران مبتلا به این بیماری معمولاً دچار ناتوانیهای حرکتی شده و ۳ تا ۵ سال پس از ابتلا به این بیماری جان خود را از دست میدهند. اگر چه ۲۰ درصد این بیماران تا ۵ سال و ۱۰ درصد آنها تا ۱۰ سال زنده خواهند ماند. در این بیماری دستگاه عصبی مرکزی و ماهیچهها بویژه ماهیچههای دست، پا، ساعد، سر و گردن به شدت صدمه میبینند.
محتویات
بیماریزایی
علت این بیماری نامشخص است[۱] (برخی بیماران زمینه ارثی دارند) اما به نظر میرسد فرایندهای التهابی که در این موتور نورونها اتفاق میافتد، دلیل بروز آن باشد.
این بیماری در اثر معیوب بودن ژن SOD۱ ممکن است بوجود آمده باشد. اما تاکنون علت دقیق ابتلا به ALS شناخته نشدهاست. ناتوانی حرکتی در این افراد سبب ایجاد زخمهایی ناشی از فشارهای طولانی مدت روی نقاط خاصی از بدن میشود. ابتلا به ذاتالریه در اثر مشکلات موجود در بلع این افراد و همچنین تجمع ترشحات در مسیرهای هوایی از دیگر عوارض جانبی احتمالی در افراد مبتلا به ALS است. این در حالی است که تحلیل نیروی جسمانی فرد میتواند جنبههای مختلف زندگی او مانند کار، روابط اجتماعی و… را تحت تاثیر پیامدهای نامطلوب خود قرار دهد. پژوهشگران برای بررسی منشاء ایجاد این بیماری نظریههای گوناگونی مانند عوامل عفونی، اختلال در دستگاه ایمنی بدن، علل وراثتی، مواد سمی، عدم تعادل مواد شیمیایی در بدن و همچنین سوءتغذیه را بررسی کردهاند. اگرچه پژوهشگران تاکنون به عامل ایجادکننده این بیماری در بیماران مختلف پی نبردهاند، اما در سال ۱۹۹۳ با شناسایی عامل ژنتیکی موثر در انتقال بیماری ALS براساس عوامل وراثتی توسط گروهی از کارشناسان علوم ژنتیک و روانپزشکان بالینی یک قدم به شناسایی عامل ایجاد بیماری نزدیکتر شدند. این عامل ژنتیکی در به رمز درآوردن آنزیمی که از سلولها در برابر آسیبهای ایجاد شده توسط رادیکالهای آزاد محافظت میکند، نقش دارد.
علایم بالینی، سیر و بروز
از جمله نشانههای شایع این بیماری دشواری در گفتار و گرفتگی ماهیچه، پرش و ضعف ماهیچهها که اغلب از اندامها (دست، بازوها و پاها) آغاز شده و گسترش مییابد و سرانجام ماهیچههای تنفسی و بلع را نیز درگیر میکند. ضعف و ناتوانی ناشی از این بیماری، راه رفتن و استفاده از دستها برای انجام فعالیتهای روزانه مانند شستن دست و صورت و لباس پوشیدن را غیرممکن میسازد. با گسترش ناتوانی حرکتی و ضعف ماهیچهها در بدن فرد، بیمار در بلع، جویدن و تنفس نیز با مشکل روبهرو میشود. هنگامی که ماهیچههای تنفسی مورد حمله قرار میگیرند فرد برای ادامه زندگی خود به ناچار باید از دستگاههای تنفس مصنوعی استفاده کند.
بروز بیماری دونفر در هر صد هزار نفر میباشد و اغلب افراد بین چهل تا شصت سال را درگیر میسازد. بیماری ماهیت پیشرونده داردو اغلب بیماران بعد از دو تا پنج سال فوت میکنند ولی گاه دورههای توقف بیماری وجود دارد؛ که باعث میشود ۱۰ درصد از بیماران تا ۱۰ سال زنده بمانند. از آنجایی که این بیماری تنها به اعصاب حرکتی آسیب میرساند، بنابراین هیچ اختلالی در بینایی، بساوایی، شنوایی، چشایی و بویایی فرد به وجود نخواهد آمد و جالب این که اعصاب حرکتی موثر در حرکت چشمها و مثانه برای مدتهای طولانی از حمله عامل بیماری مصون خواهند ماند.
بررسی یک نوع امضا یا اثر انگشت مولکولی مشترک با استفاده از فناوری نانو، تشخیص بیماری ALS را در دو حالت ارثی و غیرارثی امکانپذیر میسازد. بررسیهای انجام شده توسط پژوهشگران نشان میدهد که نوعی پپتید در مایع نخاعی همه بیماران مبتلا وجود دارد.
درمان این بیماری
بیماری ALS درمان خاصی به جز درمان علائم ندارد ولی به تازگی نیز استفاده از سلولهای بنیادی پیشنهاد شدهاست.
دانشمندان هم اکنون در تلاش هستند با انجام آزمایشهای بالینی تأثیر این روشهای درمانی در بیماران مبتلا به ALS را مورد بررسی قرار دهند. آنها امیدوارند با استفاده از نتایج این تحقیقات بتوانند به روشی برای درمان دیگر بیماریهای دستگاه عصبی مانند پارکینسون، آلزایمر و زوال عقل دست یابند.
برخی از پروتئینها مانند عوامل رشد به آسانی جذب بافت عصبی میشوند و بهنظر میرسد میتوانند از اعصاب حرکتی بدن نیز محافظت کنند. از آنجا که نمیتوان مولکولهای بزرگ را بهآسانی از طریق جریان خونی به دستگاه عصبی بدن منتقل کرد، برای استفاده از این مولکولها در فرایندهای درمانی باید آنها را بهطور مستقیم به عضلات تزریق کرد. علاوه بر این برخی از مولکولهای کوچک نیز نقش مهمی در تحریک دستگاه عصبی بدن دارند که میتوان آنها را براحتی به رگهای خونی منتهی به مغز منتقل کرد. استفاده از سلولهای بنیادی نیز روش دیگری است که مانع از پیشرفت بیماری خواهد شد. سلولهای بنیادی همانند پمپهای زیستی عمل کرده و عوامل حیاتی مؤثر در رشد را به سلولهای عصبی آسیب دیده انتقال میدهند.
آزمایشهای انجام شده در افراد مبتلا به این بیماری نشان میدهد که سلولهای بنیادی میتوانند بهطور دقیق خود را به محل سلولهای عصبی آسیب دیده انتقال دهند. همچنین ایجاد رشتههای RNA مصنوعی نیز میتواند نقش موثری در توقف تولید پروتئینهای سمی داشته باشد. این نوع RNA خود را به RNA پیک که انتقال اطلاعات ژنتیکی را بهعهده دارد متصل کرده و از ساخت پروتئینهایی که به سلولهای عصبی آسیب میرساند جلوگیری میکند. گروهی دیگر از پژوهندگان نیز در تلاش برای دستیابی به روش درمانی مؤثر برای این بیماری دریافتهاند که انجام فعالیتهای ورزشی مانع از گسترش بیماریهای اعصاب حرکتی بدن خواهد شد. در موشهای تحت بررسی آزمایشهای انجام شده، حرکت روی چرخهای گردان مانع از روند پیشرفت سریع بیماری شدهاست.
براین اساس درمانهای ترکیبی میتواند تأثیر درمان انتخاب شده در بهبود وضعیت بیمار را به نحو چشمگیری تحت تأثیر خود قرار دهد. اگر چه بهترین روش این است که در مراحل اولیه بیماری از توسعه بیماری جلوگیری کنیم. دستیابی به این هدف نیز بیش از اینکه تحت تأثیر عوامل ژنتیکی باشد مستلزم دستیابی به راهکارهایی برای ایجاد تغییرات مناسب در زندگی افراد است که با انجام تمرینات ورزشی و انتخاب برنامه غذایی مناسب میتوان به اصلاح شیوه زندگی بیماران و ایجاد شرایط مناسب برای زندگی آنها امیدوار بود.
اخیراً استفاده از دارویی به نام ریلوزول یا ریلوتک با بلوک گیرنده های گلوتامات میتواند روند بیماری را کند نماید و طول عمر بیماران را افزایش دهد.
نگهداری و مراقبت
به علت شرایط فیزیکی بیمار و عدم تحرک او نگه داری از این بیماران بسیار دشوار است و خانواده و پرستار بایستی نسبت به موارد پیش رو کاملاً توجیه باشند و با پزشک و انجمنهای محلی و خانواده سایر بیماران مشورت نمایند. به عنوان مثال حمام رفتن که کاری ساده و روزمره برای بیشتر انسان هاست در این بیماران بایستی به دقت انجام گیرد تا مانع از اسیب دیدن پرستار یا بیمار شود.
همچنین مهمترین مانع پیش رو بیماران عدم توانایی تکلم یا برقراری ارتباط با محیط بیرون است. ساده ترین روش استفاده از یک جدول حروف جلو تخت بیمار و گرفتن علامت چشم از او هنگام اشاره به حرف مورد نظر است. (مثلاً ایا در این ستون است؟ ایا در این سطر است؟) سپس باتوجه تجربه، پرستار باید حدس بزند که بیمار چه میخواهد. البته این روش بیشتر برای کارهای ابتدایی پاسخ گو میباشد. سالهاست دستگاههایی برای حل این مشکل به بازار امده که میتوانند با ردیابی حرکت چشم آنرا تبدیل به مختصات نموده و به کاربر اجازه تعامل ساده با رایانه را فراهم کنند. این گونه دستگاهها فعلاً قیمتی بین ۶ تا ۱۰ هزار دلار دارند و در ایران با توجه به موانع مالی و زبانی کاربردی نیافتهاند. البته چند پروژه برای کمک به بیماران ایرانی در دست اجرا است که از آن جمله پروژه دستگاه ارتباط با بیمار «زیگورات» است.
شیوع
براساس آمار در مقیاس جهانی دور و بر ۳۵۰ هزار نفر از بیماری ای.ال.اس رنج می برند. در هلند یک هزار و ۵۰۰ نفر به این بیماری دچار هستند. سالانه حدود ۶۵۰ بیمار به علت ای.ال.اس مورد آزمایش و تحقیق قرار می گیرند . همچنین هر سال حدود ۳۵۰ نفر در اثر این بیماری در کشور هلند میمیرند. [۲]
پیوند به بیرون
منابع
- “Amyotrophic Lateral Sclerosis (ALS) Fact Sheet”. National Institute of Neurological Disorders and Stroke. Retrieved 4 December 2015.
- مشارکتکنندگان ویکیپدیا، «ALS»، ویکیپدیای انگلیسی و www.pezeshk.us/?p=۱۳۱۸۷، دانشنامهٔ آزاد (بازیابی در ۲۸ نوامبر ۲۰۰۹).
ادامه مطلب
| اسکلرودرمی | |
|---|---|
 |
|
| آیسیدی-۱۰ | L94.0-L94.1, M34 |
| آیسیدی-۹ | 701.0 710.1 |
| مدلاین پلاس | 000429 |
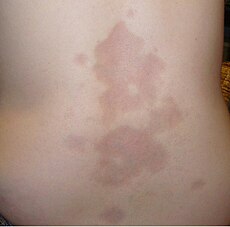
بیماری «اسکلرودرمی» (Scleroderma) نوعی بیماری نادر و پیشرونده روماتیسمی است که پوست بیماران ضخیم، سفت و خشک شده و گاه در انتهاهای اندامها زخم ایجاد میشود. تجمع کلاژن وسایر فیبرها در این بیماری پوست صورت و اندامها، مفاصل دست و پا، ریه، کلیه و دستگاه گوارش به خصوص مری را گرفتار و فرد را ناتوان میکند. این بیماری میتواند به صورت موضعی (Limited) یا عمومی (Systemic scleroderma) بروز کند.
محتویات
عوارض بیماری
زخمها گاهی چنان پیشرفت میکنند که باعث قطع شدن انگشتان فرد میشود، حرکت انگشتان دست در این بیماری محدود شده و همچنین فرد قادر به بازکردن کامل دهان خود نیست. سایر عوارض احتمالی این بیماری اختلال در ترمیم زخمها، افزایش خونریزی، اختلال در ریتم قلب، نارسایی احتقانی قلب، نارسایی کلیه، اختلال در بلع، فشارخون بالا، تخریب بافتهای ریوی و درگیری عروق کوچک (به ویژه آرتریولها)است. تشخیص با آزمایشهای خون جهت شناسایی کمخونی و اندازهگیری پادتن ها؛ آزمایش ادرار برای شناسایی گلبولهای قرمز در ادرار؛ نوار قلب؛ رادیوگرافی دستها، مری و قفسه سینه تایید میشود.
بیماریزایی
هنوز علت قطعی ابتلا به اسکلرودرمی روشن نشدهاست، خودایمنی، زمینه ژنتیک، برخی عوامل میکروبی و... از علل موثر در ایجاد این بیماری میباشند. ابتلا به این بیماری در سنین زیر پنج سال و بالای ۷۰ سال نادر است و شیوع آن در سنین ۳۵ تا ۵۰ سالگی مشاهده میشود. امید به زندگی ده ساله ۵۵٪ است.
درمان
درمان قطعی اسکلرودرمی تا به امروز نامشخص میباشد. معمولاً درمان عوارض و ورزش توصیه میشود.گاه از داروهای سرکوبگر ایمنی مانند متوتروکسات و آزاتیوپرین، داروهای شیمی درمانی مانند کلشی سین و سیکلوسپورین، کورتیکواستروئیدها در درمان استفاده میشود. اکسیژن درمانی در محل زخمها و بلوککنندههای کانال کلسیم در پدیده رینود (تنگی عروق انتهایی انگشتان) به کار میروند.
منابع
- ویکیپدیای انگلیسی اسکلرودرمی
ادامه مطلب
اسفروسیتوز ارثی (به انگلیسی: Hereditary spherocytosis) یک آسیب ارثی است که به سبب نقص در سنتز یک پروتئین غشایی آسیب دیدگی غشاء گلبولهای قرمز روی میدهد، گلبولهای قرمز شکل کروی مییابند. گلبولهای قرمز کروی شکل به دلیل شکل غیرمعمول خود از خون جدا شده و بدست طحال نابود میشوند. این امر موجب کاهش شمار گلبولهای قرمز درگردش خون شده و درنتیجه کمخونی ایجاد میشود.
محتویات
علائم
علائم این بیماری کم خونی، زردی، بزرگ شدن طحال وسنگ صفراوی است. در اسمیر خون محیطی اجسام هاول ژلی (Howell-Jolly bodies) دیده میشود. گویچههای سرخ معمولاً نرموسیتیک هستند و تعداد رتیکولوسیتها تا بیست درصد افزایش مییابد. افزایش شکنندگی اسموتیک گویچههای سرخ، آزمایش کومبس منفی سایر علائم بیماری هستند.
بیماریزایی
بیماری عمدتاً به صورت اتوزومال غالب (75%) و در 25% موارد به شکل اتوزومال مغلوب (که شکل شدیدتری از بیماریست) به فرزندان منتقل میشود. بیماری ظاهراً در اثر نقصی در آنکیرین – که پروتئینی ضروری برای اتصال پروتئین ساختاری اسپکترین به غشاء گویچهٔ سرخ است – رخ میدهد.
اسفروسیتوز غیر ارثی
اسفروسیتوز غیر ارثی یک آنمی همولیتیک اتوایمیون (خودایمنی) است. اسفروسیتها همچنین در بیماری هموگلوبین C و بعضی سوختگیهای شدید دیده میشوند.
درمان
تنها درمان موثر برداشتن کامل طحال (اسپلنکتومی) است. باید احتمال وجود طحالهای فرعی را درنظر گرفت. اسپلنکتومی موجب رفع آنمی میشود. این کار باید بعد از شش سالگی انجام شود تا خطر سپسیس و مرگ کودک کمتر شده باشد. همچنین مصرف اسیدفولیک و تزریق واکسنهای پنوموکوک، مننگوکوک و هموفیلوس آنفلوآنزا قبل از اسپلنکتومی توصیه میشود.
جستارهای وابسته
منابع
- مشارکتکنندگان ویکیپدیا، «Hereditary spherocytosis»، ویکیپدیای انگلیسی، دانشنامهٔ آزاد (بازیابی در ۱۸ اردیبهشت ۱۳۹۲).
ادامه مطلب
Leukocytosis
-
استئومیلیت  کورک استخوان درشتنی یک نوجوان. آبسههای فراوان در استخوان به صورت روشنتر نشان داده شدهاند.
کورک استخوان درشتنی یک نوجوان. آبسههای فراوان در استخوان به صورت روشنتر نشان داده شدهاند.آیسیدی-۱۰ M86 آیسیدی-۹ 730 دادگان بیماریها ۹۳۶۷ مدلاین پلاس 000437 ایمدیسین ped/۱۶۷۷ پیشنت پلاس استئومیلیت سمپ D010019 ورم استخوان (نامهای دیگر: کورک استخوان، التهاب مغز استخوان، استئومیلیت (به انگلیسی: Osteomyelitis)) به معنی عفونت استخوان و مغز استخوان میباشد. تمام استخوانهای بدن ممکن است دچار عفونت شوند.
محتویات
بیماریزایی
باکتری به سه طریق ممکن است به استخوان برسد: از راه جریان خون به خصوص در حضور عفونت سایر بافتها مثلاً سلولیت پوست، از راه ترومای نافذ مثلاً شکستگی باز و راه آخر از راه مداخلهٔ پزشکی برای نمونه به دنبال تثبیت شکستگی با جراحی و گذاشتن پروتز، عصبکشی در دندانپزشکی و دیگر اقدامات درمانی.
شایعترین عامل ورم استخوان، میکرب استافیلوکوک میباشد. در سایر موارد اغلب باکتریهایی مانند استرپتوکوک، انتروباکترها و مایکوباکتریوم و گاه قارچها عامل بیماری میباشند. در کمخونی سلول داسیشکل اغلب عامل بیماریزا سالمونلا است. استئومیلیت مزمن ممکن است به علت وجود باکتریهای داخل سلولی (داخل سلولهای استخوان) باشد. این باکتریها قادر به هجوم به سلولهای دیگر استخوانی هستند، علاوه بر این، باکتریهای بین استخوانی در مقابل آنتی بیوتیکها مقاومت پیدا میکنند. این موارد استئومیلیت مزمن را توجیه میکنند. استئومیلیت به خصوص نوع مزمن آن میتواند به فلج شدن، قطع عضو و حتی مرگ نیز بینجامد.
در کودکان استئومیلیت میتوانند به مفصلها منتقل شود و به التهاب مفصل منجر شود. استخوانهایی که در کودکان معمولاً درگیر میشوند عبارتند از استخوانهای بلند مانند استخوان ران، درشتنی و استخوان بازو. در بزرگسالان معمولاً استخوانهای لگن، ستون فقرات و گاه فک درگیر میشوند. این بیماری در کودکان در دوره رشد سریع (۱۴–۵ سال)، به خصوص در جنس مذکر شایعتر است. ورم استخوان مزمن در افراد بالغ به ویژه معتادان تزریقی، افراد با ضعف ایمنی، افراد ناتوان و بیماران مرض قند شایعتر است.
علل
در کودکان مبتلا به این بیماری، اغلب استخوانهای بلند تحت تأثیر قرار میگیرند و در افراد بزرگسال، مهرهها و لگن مورد تأثیر واقع میشوند. استئومیلیت بحرانی و حاد، همواره میتواند در کودکان رخ دهد. وقتی افراد بزرگسال تحت تأثیر قرار میگیرند، میتواند به علت مقاومت ضعیف شدهٔ میزبان باشد. سوء مصرف دارو به صورت درون وریدی، دندان روت کانال(عصبکشی) شده که منجر به عفونت آن میشود.
استئومیلیت در ۱ تا ۳ درصد بیماران به صورت یک بیماری درآمیخته با توبرکلوسیس ریوی در میآید، در این حالت، باکتری از راه سیستم گردش خونی به استخوان نفوذ میکند و اول از همه به علت غلظت بالای اکسیژن، مایع داخل مفصلی را آلوده میکند و سپس به استخوان مجاور نفوذ کرده و آن را آلوده میکند واستئومیلیتی که بر پایهٔ انتقال از راه گردش خونی است، را میتوان در کودکان مشاهده کرد و بالغ بر ۹۰ درصد این نوع از استئومیلیت را استافیلو کوکوس ارئوس عامل میشود. در کودکان کمتر از هفت سال، عوامل این بیماری عبارتند از :S.Aureus، استرپتوکوکی نوع B(رایجترین نوع)، E.Coli.
در افراد بزرگسال رایجترین عامل استئومیولیت، بیپناه بودن استخوان آسیب دیده در برابر عفونت میباشد. استافیلو کوکوس ارئوس رایجترین نوع باکتری در استئومیلیتهایی است که از سرایت کردن عفونت از محل آسیب دیدگی به وجود میآید، اما باکتری بیهوازی و ارگانیسمهای گرم منفی از جمله سودوموناس آئروژینوزا و سراشیا و نیز E.Coli، رایج هستند. میوکوتیک سیستمیک (هنگامی که ارگانیسم قارچ بر دستگاه دفاعی بدن غلبه کرده و موجب عفونت میشود) نیز از عوامل استئومیلیت میباشد.
تشخیص
تشخیص این بیماری بیشتر بر مبنای رادیولوژی صورت میگیرد و در گرافی نتایج به صورت یک چرخهٔ لیتیک با یک حلقهٔ اسکلروزیس همراه است. دقیقترین و حساسترین روش تشخیص این بیماری ام آر آی است که در موارد خاصی همچون زخم پای دیابتی و عفونتهای ستون فقرات از آن استفاده میشود.
علایم بیماری
در ورم حاد استخوان تب، درد، تورم، قرمزی، گرمی و احساس درد با لمس برروی استخوان مبتلا، به خصوص هنگام حرکت دادن مفصل مجاور آن. مفاصل مجاور ناحیه مبتلا نیز ممکن است دچار التهاب (قرمزی، گرمی و تورم) باشند، احساس ناخوشی عمومی. در کودکانی که هنوز قادر به تکلم نیستند، وجود درد به صورت امتناع از حرکت دادن اندام، خودداری از راه رفتن، لنگیدن هنگام راه رفتن یا جیغزدن هنگام لمس یا حرکت دادن عضو مبتلا، نشان داده میشود.
در ورم استخوان مزمن ما خروج چرک از طریق آبسه پوستی، بدون تب یا درد شدید را ممکن است داشته باشیم (گاه همراه با علائم ورم استخوان حاد). همچنین در ورم استخوان مزمن بخشهایی از استخوان بافتمرده میشوند. بدن در اطراف این بخشهای بافتمرده شروع به استخوانسازی میکند و گریبانهای[۱] از استخوان پدید میآورد. این نما از نکات متمایزکننده اصلی بین ورم استخوان مزمن و حاد است.
در آزمایشگاه لکوسیتوز[۲] (افزایش گلبولهای سفید خون)، افزایش سطح آنزیمهای لیز استخوانی و... داریم. گاه کشت مغز استخوان مثبت است.
در رادیولوژی ورم استخوان مزمن ما کانونهای تخریب شده استخوان همراه با حلقههای سفتشده (اسکلروز) را داریم.
درمان
این بیماری یک اورژانس ارتوپدی-پزشکی است. اصول درمان بر تجویز طولانی آنتی بیوتیک قوی (گاه ماهها) و دبریدمان استوار است. درمان استئومیلیت مزمن دشوار است. آنتیبیوتیکهایی مانند وانکومایسین، سفالوسپورینهای نسل سوم و چهارم و... مفیدند.
منابع
- ویکیپدیای انگلیسی استئومیلیت
- involucrum
ادامه مطلب
| نرماستخوانی | |
|---|---|
| آیسیدی-۱۰ | M83 |
| آیسیدی-۹ | 268.2 |
| دادگان بیماریها | 9351 |
| ایمدیسین | ped/2014 radio/610 |
| پیشنت پلاس | نرماستخوانی |
| سمپ | D010018 |
مینرالیزاسیون تأخیری و ناکافیِ استخوان در افراد بالغ را استئومالاسی (به انگلیسی: Osteomalacia) یا نرماستخوانی مینامند.
محتویات
بیماریزایی
علت اصلی آن کمبود ویتامین D (عدم استفاده از اشعهٔ آفتاب در ایران) است. سوء تغذیه و کمبود کلسیم یا فسفر، اختلالات آنزیمیِ ارثی (بیماران مقاوم به ویتامین دی)، و یا بیماریهایی نظیر امراض متابولیکی کبد، نارسایی مزمن کلیه، مصرف بعضی داروها ازجمله داروهای ضد صرع، سندرمهای سوءجذب مانند سلیاک و سرطانها سایر علل نرمی استخوان هستند.
در این بیماری، بهعلت عدم کلسیفیه شدن صحیح بافت استخوان، شکل و استحکام استخوان طبیعی نیست. «استئومالاسی»، مشابه بیماری راشیتیسم کودکان است. البته در سنین بالا، صفحه رشد استخوانها بسته میشود لذا استئومالاسی برخلاف راشیتیسم بر روی صفحه رشد استخوان و رشد طولی استخوانهای دراز اثری ندارد.
بیماری در خانمها نسبت به آقایان و در زمستان و اوایل بهار شایعتر است.
علائم بالینی
شروع بیماری با کمردرد و دردهای اندامهاست. سپس شکستگی کاذب، پوکشدگی استخوانها، ضعف عضلانی و دردهای عضلانی و مفصلی در بلندمدت ممکن است در ستون فقرات انحراف و قوز (کیفوز) و یا لوردوز و در استخوانهای دراز کمانی شدن مشاهده شود.
علائم رادیولوژیک نرمی استخوان بهصورت تغییر شکل مهرههای ستون فقرات، استخوان لگن، استخوان ران و کتف و شکستگیهای کاذب مشخص میشود. این علائم معمولاً در مراحل پیشرفته بیماری دیده میشوند. کاهش معنیدار در میزان کلسیم (Ca)، فسفر (P)، افزایش آلکالن فسفاتاز (ALKP)، پاراتورمون سرم (PTH) نسبت به دامنه طبیعی.
درمان استئومالاسی مصرف خوراکی کلسی تریول و کلسیم و یا تزریق عضلانی ویتامین D است. مصرف لبنیات و سبزیجات (حاوی کلسیم و ویتامین دی) و ورزش توصیه میشود.
جستارهای وابسته
منابع
- مشارکتکنندگان ویکیپدیا، «Osteomalacia»، ویکیپدیای انگلیسی، دانشنامهٔ آزاد (بازیابی در ۲۳ سپتامبر ۲۰۰۹).
- فرهنگ واژههای مصوب فرهنگستان زبان وادب فارسی
ادامه مطلب
| استئوژنز ایمپرفکتا | |
|---|---|

The classic blue sclerae of a person with osteogenesis imperfecta
|
|
| آیسیدی-۱۰ | Q78.0 |
| آیسیدی-۹ | 756.51 |
| دادگان بیماریها | 9342 |
| مدلاین پلاس | 001573 |
| ایمدیسین | ped/1674 |
| پیشنت پلاس | استئوژنز ایمپرفکتا |
| سمپ | D010013 |
استئوژنز ایمپرفکتا (Osteogenesis imperfecta) یا استخوان سازی ناقص بیماری ژنتیکی و مادرزادی است که در آن استخوان بسیار ترد و شکننده میشود.افراد مبتلا به این بیماری در طول عمر خود دچار شکستگی های متعدد میشوند. صلبیه اغلب بیماران آبی رنگ است.
محتویات
بیماریزایی
در استئوژنز ایمپرفکتا ژن خاصی در بدن کار خود را به خوبی انجام نداده و پروتئین خاصی به نام کلاژن تیپ یک به درستی ساخته نمیشود. هفتاد درصد بیماران به شکل توارث (اتوزومال غالب و گاه مغلوب) از والدین بیماری را به ارث میبرند ولی سی درصد بصورت اسپورادیک (جهش) مبتلا میشوند.
انواع
شدت بیماری استئوژنز ایمپرفکتا در بیماران متفاوت است.افراد مبتلا به نوع یک این بیماری ،تغییر شکل استخوانی کم ،صلبیه آبی رنگ دائمی،قد نزدیک به نرمال در بزرگسالی، احتمال کاهش شنوایی بیشتر ار 50درصد در سنین بزرگسالی دارند. بیماران مبتلا به نوع دو استئوژنز ایمپرفکتا شدت بیشتری از این بیماری نشان میدهند و شکستگی های متعدد در لگن و زمان وضع حمل دارند. این نوزادان معمولاً مرده متولد میشوند و یا به زودی می میرند. به طور کلی دارای وزن کم هنگام تولد و میکروملیا (استخوان های کوچک غیر عادی) با خمیدگی هستند. در نوع سه آن چند ژن درگیر هستند.
| Type | Description | Gene | OMIM | Mode of Inheritance |
| I | mild | Null COL1A1 allele | 166240 (IA), 166200 (IB) | autosomal dominant, 60% de novo [۱] |
| II | severe and usually lethal in the perinatal period | COL1A1, COL1A2, | 166210 (IIA), 610854 (IIB) | autosomal dominant, ~100% de novo [۱] |
| III | considered progressive and deforming | COL1A1, COL1A2 | 259420 | autosomal dominant, ~100% de novo [۱] |
| IV | deforming, but with normal scleras | COL1A1, COL1A2 | 166220 | autosomal dominant, 60% de novo [۱] |
| V | shares the same clinical features of IV, but has unique histologic findings ("mesh-like") | IFITM5 | 610967 | autosomal dominant [۱][۲] |
| VI | shares the same clinical features of IV, but has unique histologic findings ("fish scale") | unknown | 610968 | unknown [۱] |
| VII | associated with cartilage associated protein | CRTAP | 610682 | autosomal recessive [۱] |
| VIII | severe to lethal, associated with the protein leprecan | LEPRE1 | 610915 | autosomal recessive |
تظاهرات بالینی
اصلیترین تظاهر استخوان نرم وشکننده است. پوست ممکن است نازک و آتروفیک شود و حتی نور را عبور دهد و دندان ها مستعد پوسیدگی و شکستن شوند و یک رنگ غیر عادی از زرد کهربایی تا خاکستری مایل به آبی دارند. وقتی ملتحمه آبی رنگ بروز میکند، یک خصوصیت ویژه و تمییز دهنده بیماریست ودر 90درصد بیماران دیده میشود.رنگ دانه های مشیمیه از خلال صلبیه نازک مشاهده می شوند و چندین نمای آبی توصف شده اند. سایر ویژگیها شامل اوتواسکلروز(سخت شدن گوش) همراه با کاهش شنوایی که مکن است در طی دومین تا سومین دهه زندگی شروع شوند و ضایعات قلبی عروقی شامل اتساع دریچه میترال همراه با نارسایی ،سندرم دریچه میترال سست و نکروز کیستیک مدیای آئورت هستند.
منابع
- Steiner, RD; Pepin, MG, Byers, PH, Pagon, RA, Bird, TD, Dolan, CR, Stephens, K, Adam, MP (January 28, 2005). "Osteogenesis Imperfecta". PMID 20301472. Retrieved 26 March 2012.
- Shapiro JR, Lietman C, Grover M, Lu JT, Nagamani SC, Dawson BC, Baldridge DM, Bainbridge MN, Cohn DH, Blazo M, Roberts TT, Brennen FS, Wu Y, Gibbs RA, Melvin P, Campeau PM, Lee BH (2013) Phenotypic variability of osteogenesis imperfecta type V caused by an IFITM5 mutation. J Bone Miner Res doi: 10.1002/jbmr.1891
ایران ارتوپد Osteogenesis_imperfecta
ادامه مطلب
| استئوآرتریت | |
|---|---|

کاهش فاصله مفصل و ایجاد استئوفیت در آرتروز زانو
|
|
| آیسیدی-۱۰ | M15-M19, M47 |
| آیسیدی-۹ | 715 |
| اُمیم | 165720 |
| دادگان بیماریها | 9313 |
| مدلاین پلاس | 000423 |
| ایمدیسین | med/1682 |
| پیشنت پلاس | آرتروز |
| سمپ | D010003 |
استئوآرتریت (به انگلیسی: Osteoarthritis) بیماری بسیار شایعی است که در تمام مناطق جغرافیایی دیده میشود. نام دیگر این بیماری آرتروز است و بعضی دیگر معتقدند که استئوآرتروز نام بهتری برای این بیماری است. استئوآرتریت یک بیماری تخریبی در مفصل است (تخریب غضروف مفصل) که پیشرونده بوده ولی علیرغم نامگذاری آن، یک بیماری التهابی نیست (بر خلاف آرتریت روماتویید). چون التهاب در این بیماری یک عارضه ثانویه است.
در استئوآرتریت تحلیل غضروف مفصلی و درگیری استخوان زیر غضروفی داریم که باعث التهاب بافتهای اطراف میگردد. این عارضه ممکن است هر یک از مفاصل را درگیر سازد ولی شایعترین مفاصل درگیر عبارتند از مفاصل دست ،پا، زانو، ران و ستون فقرات. این بیماری بسیار شایع است و در ۲۵٪ ویزیتهای پزشکان عمومی و ۸۰٪ رادیوگرافی افراد بالای ۶۵ سال دیده میشود (البته فقط ۶۰٪ آنان علامت دارند).
محتویات
بیماریزایی
استئوآرتریت بیماریی مفصلی است که ابتدا غضروف مفصل را درگیر مینماید. غضروف بافتی لغزندهاست که انتهاهای استخوانها را در یک مفصل میپوشاند. استخوانها داشتن حرکتی آسان بر روی یکدیگر را مدیون غضروفهای سالم هستند. وظیفه دیگر غضروفها جذب شوک در طی حرکات فیزیکی میباشد (Shock Absorption). در بیماری استئوآرتریت غضروفها نازک شده و بتدریج در برخی نواحی از بین میرود که باعث میشود استخوانهای زیر غضروفها به همدیگر ساییده شوند. نهایتاً درد، التهاب و کاهش حرکت در مفصل به وجود آید. به مرور زمان مفصل شکل طبیعی خودش را از دست میدهد. همچنین استئوفیتها (زوائدی استخوانی که در لبههای مفصل رشد میکنند)تشکیل میشوند که خود باعث درد و ناراحتی بیشتر میشوند. برعکس سایر آرتریتها مانند آرتریت روماتوئید استئوآرتریت تنها مفاصل را درگیر مینماید و به سایر اندامها کاری ندارد. آرتریت روماتوئید افراد جوانتر را مبتلا میکند و ممکن است علاوه بر درگیری مفصل فرد احساس مریضی، خستگی و یا تب نماید.
علایم شایع
درد مفاصل، محدودیت حرکت و کاهش انعطاف پذیری مفاصل، التهاب و تورم مفصل، معمولاً بدون گرما یا تب همراه درگیری مفاصل، افیوژن مفصل و صدای ترق و تروق یا صدای ساییده شدن با حرکت مفصل مبتلا (گاهی)
درد ممکن است در آغاز خفیف باشد، ولی میتواند به قدری شدید گردد که زندگی و خواب بیمار را دچار اختلال کند.درد مفاصل موجب عدم تحرک کافی بیمار میشود که این خود باعث لنگیدن، تحلیل رفتن و ضعیف شدن عضلات اطراف مفصل مبتلا و شل شدن لیگامانها میگردد. تغییرات مفصلی دایمی هستند و بیماری ماهیت پیشرونده دارد.
در درگیری مفاصل انگشتان دست ما تورم استخوان را داریم که در مفاصل انتهایی انگشتان گره های هبردن (Heberden's nodes) و در مفاصل میانی گره های بوچارد(Bouchard's nodes) نامیده میشوند.
علل
علت دقیق این اختلال ناشناختهاست. به نظر میرسد نتیجه ترکیب یا تعامل عوامل مکانیکی با سایر عوامل در افرادی با زمینه ارثی باشد. عوامل افزایش دهنده خطر چاقی، بالارفتن سن و فعالیتهایی که با فشار به مفاصل (میکروتروما) همراهند نظیر رقص، فوتبال، موسیقی یا قالی بافی، دیابت، سندرم مارفان، بیماری ویلسون و آلکاپتونوری میباشند. تقریباً اغلب افراد بالای ۵۰ سال به درجاتی به استئوآرتریت مبتلا هستند.آرتروز در خانمها بیشتر از آقایان بروز میكند ولی دلیل آن هنوز به درستی مشخص نشده است.[۱]
پیشگیری و تشخیص
حفظ وزن در حد مناسب، داشتن فعالیت فیزیکی مناسب، تغذیه مناسب باعث پیشگیری بیماری می شود. تشخیص اصولاً بالینی است. بررسیهای تشخیصی ممکن است شامل بررسی آزمایشگاهی مایع مفصل (برای ردکردن احتمال آرتریت التهابی) باشد. رادیوگرافی مفاصل درگیر، میزان کاهش فاصله مفصلی، اسکلروز و گاه کیست زیر غضروفی را نشان میدهد.
درمان دارویی
استامینوفن یا داروهای ضد التهاب غیر استروئیدی (NSAIDs) مانند آسپیرین و بروفن جهت کاهش درد و تخفیف التهاب به کار میروند. اینفیلتراسیون یا تزریق کورتون به داخل مفاصل شدیداً درگیر ممکن است به طور موقت باعث تخفیف درد و ناراحتی گردد. NSAIDs موضعی، مسکنهای مخدر، تزریق اسید هیالورونیک نیز تجویز شدهاند. سایر داروهایی که برحسب نیاز ممکن است تجویز شوند شامل گلوکوزآمین کندروئیتین، آنتی اکسیدانهایی مانند ویتامین C و ویتامین E، سلنیوم، فولات یا ویتامین B۹ و ویتامین B۱۲، ویتامین دی، (SAMe)، شل کنندههای عضلانی و مسکنهای قوی تر هستند.
سایر اقدامات درمانی
برای تخفیف درد، مفاصل مبتلا را گرم کنید و عضلات اطراف مفاصل درگیر را ماساژ دهید. برای استئوآرتریت گردن از یک گردن بند بی حرکت کننده گردن استفاده کنید. در استئوآرتریت ستون فقرات، هنگام خواب به پشت بخوابید و از یک تشک سفت استفاده کنید. جراحیهای توصیه شده برای استئوآرتریت شدید (مقاوم به درمان) شامل آرتروپلاستی (تعویض مفصل) و آرترودز (بی حرکت کردن مفصل)، برداشتن تکههای استخوانی با آرتروسکوپ می باشد.
فعالیت ورزشی متوسط برای آرتروز مفید است.استراحت تنها در مرحله حاد بیماری که مفاصل خیلی دردناکند ضروری است.
درمان فیزیکی برای توانبخشی عضلات و مفاصل (تنها برای موارد شدید).
ممکن است جلوگیری از حرکت زیاد مفصل لازم باشد (با استفاده از چوبهای زیربغل، عصا، واکر و زانوبند کشی)
- تحقیقات نشان می دهد که مصرف هندوانه در کاهش علائم آرتروز زانو (استئوآرتریت) و رماتیسم و تقویت سیستم ایمنی و دفاعی بدن علیه عفونت ها نقش موثری دارد.[۲]
جستارهای وابسته
منابع
- هندوانه در تقویت سیستم ایمنی بدن و کاهش علائم رماتیسم موثر است . [خبرگزاری جمهوری اسلامی(ایرنا) http://www.irna.ir]
- مشارکتکنندگان ویکیپدیا، «Osteoarthritis»، ویکیپدیای انگلیسی، دانشنامهٔ آزاد (بازیابی در ۲۳ سپتامبر ۲۰۰۹).
پیوند به بیرون
استئوآرتریت
ادامه مطلب







