. Genetics Home Reference. U.S. National Library of Medicine. Retrieved 4 March 2013.
-
سندرم آلاژیل آیسیدی-۱۰ Q44.7 آیسیدی-۹ 759.89 اُمیم ۱۱۸۴۵۰ دادگان بیماریها ۲۹۰۸۵ ایمدیسین ped/۶۰ سمپ D016738 سندرم آلاژیل (به انگلیسی: Alagille syndrome) یا دیسپلازی آرتریوهپاتیک، نوعی بیماری وراثتی است که دستگاههای چندی از بدن در آن درگیر میباشند.[۱] علاوه بر هیپوپلازی (تشکیل نشدن کامل) مجاری صفراوی داخل کبدی که منجر به کلستاز میشود، نوزادان مبتلا به این نشانگان (سندرم)، ممکن است دچار آنومالیهای صورت، قلب (بصورت تنگی دریچه ریوی یا تنگی محیطی عروق ریوی و تترالوژی فالوت[۲])، ستون فقرات (مهره پروانهای)، چشم (امبریوتوکسین خلفی) و کلیه (دیسپلازی کلیه) باشند. بیماران در نتیجه دچار سطح کلسترول خونی بالا و گزانتمهای پوستی همراه آن هستند. رشد ناکافی و عقب ماندگیذهنی خفیف هم گاهی وجود دارد.
درمان
درمان این سندرم شامل رژیم غذایی برای هیپرکلسترولمی و کلستیرامین است. برای درمان عوارض کمبود ویتامین ای مانند آتاکسی، از دست دادن رفلکسها و از دست دادن حس ارتعاش و موقعیت و فلج عضلات خارج چشمی؛ درمان با مقادیر زیادی از ویتامین E انجام میشود. درمان با فنوباربیتال و اورسودوکسی کولیک اسید در پایین آوردن بیلیروبین و اسیدهای صفراوی کمک کننده است. از نظر توارثی، الگوی انتقال این بیماری، اتوزوم غالب میباشد.[۳]
منابع
- Kliegman, [edited by] Richard E. Behrman, Robert M. (1994). Nelson essentials of pediatrics (2nd ed. ed.). Philadelphia: W.B. Saunders. p. 429. ISBN 0721637752 (help).
- مشارکتکنندگان ویکیپدیا، «Alagille syndrome»، ویکیپدیای انگلیسی، دانشنامهٔ آزاد (بازیابی در ۱۴ اسفند ۱۳۹۱).
ادامه مطلب
| نشانگان آگلوتینین سرد | |
|---|---|

|
|
| آیسیدی-۱۰ | D59.1 |
| آیسیدی-۹ | 283.0 |
| دادگان بیماریها | 2949 |
| ایمدیسین | med/408 |
| سمپ | D000744 |
نشانگان آگلوتینین سرد نوعی کمخونی همولیتیک خودایمن (اتو ایمیون) است. و مانند هر کمخونی همولیتیک خودایمن دیگری به انواع اولیه و ثانویه تقسیم میشود. در این نشانگان نیز مانند بقیه کمخونیهای همولیتیک اتو ایمن پادتنهایی در بدن ایجاد میشوند که به غشا گویچههای سرخ متصل میشوند و باعث تخریب گویچههای سرخ میشوند. در نشانگان آگلوتینین سرد به طور خاص این پادتنها در دمای پایین تری واکنش نشان میدهند و به پروتئینهای غشا گویچههای سرخ متصل میشوند.
محتویات
نوع اولیه
نوع اولیه نشانگان آگلوتینین سرد در نوع اولیه پادتنها به صورت تکدودمانی (مونو کلونال-monoclonal) هستند و علت خاصی برای بروز بیماری شناخته نشده است. این فرم از بیماری معمولاً مزمن است و بعد از دهه پنج زندگی بروز میکند.
نوع ثانویه
نوع ثانویه نشانگان آگلوتینین سرد میتواند ثانویه به بیماریهای مختلفی بروز کند. در انواع تک دودمانی معمولاً بیماری مزمن است و در بزرگسالانی مبتلا به بیماریهای زیر دیده میشود: نیوپلاسم سلولهای B - ماکروگلوبلولینمی والدنشتروم - لنفوم - لوسمی انفویید مزمن - میلوم
تغییر رفتاری
افزون بر مراقبتهای پزشکی به دلیل فعال شدن این نوع کمخونی در هوای سرد، نکات زیر توصیه می شود:[۱]
- دوری کردن از هوای سرد با پوشیدن لباس گرم
- پوشیدن دست کش هنگام کار با یخچال فریزر
- گرم کردن خودرو در هوای سرد پیش از سوار شدن
ادامه مطلب
بیماریهای متابولیک مادرزادی علائم بالینی، تشخیص و درمان، دکتر پریچهر توتونچی-امیر ساسان توتونچی
-
سندرم ایمرسلاند-گراس Imerslund-Grasbeck syndrome بک که با نامهای سندرم ایمرسلاند-نجمان-گراس بک Imerslund-Najman-Grasbeck syndrome و همچنین بیماری ایمرسلاند-گراس بک, سندرم ایمرسلاند, سوء جذب مادرزادی کوبالامین یا کم خونی مگالوبلاستیک اتوزوم مغلوب نیز خوانده میشود، شکل خانوادگی کمبود ویتامین ب ۱۲ و با الگوی توارث اتوزوم مغلوب است که به دنبال اختلال کارکرد نوعی گیرنده که در ایلئوم ترمینال قرار دارد بروز میکند.
محتویات
علائم و نشانه ها
- کم خونی
- گلوسیت (التهاب زبان)
- استوماتیت(التهاب گوشه لبها و مخاط دهان)
- تابس دورسالیس
- نوروپاتی محیطی
- پان سیتوپنی
- افزایش سطح متیل مالونیل کوآ در خون
- در بررسی خون محیطی، کم خونی مگالوبلاستیک دیده میشود.
- پروتئینوری
- با تزریق ویتامین ب ۱۲ , همه علائم به جز علائم عصبی رفع میشوند.
الگوی توارث
درمان
تزریق وریدی ویتامین ب ۱۲.
منابع
- Grasbeck R (2006). "Imerslund-Gräsbeck syndrome (selective vitamin B12 malabsorption with proteinuria". Orphanet Journal of Rare Diseases 1: 17
ادامه مطلب
| سندرم آشرمن | |
|---|---|

تصویر اولتراسونیک
|
|
| آیسیدی-۱۰ | N85.6 |
| آیسیدی-۹ | 621.5 |
| دادگان بیماریها | 946 |
| مدلاین پلاس | 001483 |
| سمپ | D006175 |
سندرم آشرمن وضعیتی است که با چسبندگی یا فیبروز آندومتر رحم مشخص میشود که اغلب بدنبال کورتاژ رحم ایجاد میشود .
محتویات
علل
اصولاً سندرم آشرمن بیماری نادری است و اغلب در افرادی رخ می دهد که سابقه چندین بار کورتاژ و سقط داشته اند.همچنین ممکن است ناشی از جراحی های داخل رحمی دیگر باشد.
درمان
تشخیص با هیستروسکوپی و یا هیستروسالپنگوگرافی است. اگر موجب آمنوره سقط و ناباروری شود درمان با جراحی و برداشتن چسبندگی است.
جستارهای وابسته
منابع
ادامه مطلب
| سندرم استیونز–جانسون | |
|---|---|

شخصی مبتلا به سندرم استیونز–جانسون
|
|
| آیسیدی-۱۰ | L51.1 |
| آیسیدی-۹ | 695.13 |
| اُمیم | 608579 |
| دادگان بیماریها | 4450 |
| مدلاین پلاس | 000851 |
| ایمدیسین | emerg/555 derm/405 |
| پیشنت پلاس | نشانگان استیونز–جانسون |
| سمپ | D013262 |
سندرم استیونز–جانسون (به انگلیسی: Stevens–Johnson Syndrom) یک بیماری نادر در پوست و مخاط بدن است که بر اثر عفونت یا داروهای آلرژیزا ایجاد میشود.
محتویات
ابتلا
علت اصلی ابتلا به این سندم (نزدیک به ۵۰٪) واکنشهای آلرژیک به داروها (مانند سولوفنامید، هیدانتوئین، آلوپورینول و ...) است.[۱]. دلیلهای فرعی میتواند عفونتهای لنفاوی، مایکوپلاسمایی یا باکتریهای دیگر باشد.
پاتومکانیزم
این سندرم به واکنش دفاعی لنفوسیت تی در بدن انسان بر میگردد. بر اثر آپوپتوز سلولهای کراتینوسیت از بین میروند. اما دلیل پاتولوژی دیگر تاکنون کشف نشدهاست.
نشانهها
به صورتی کلینیکی، این بیماری خود را به صورت یک بیماری عمومی با تب، و رینیت نشان میدهد. پس از آن پوست شروع به التهاب میکند. مرکز التهاب سیاه رنگ است و در داخل دهان، لبها و آلت تناسلی جوشهای دردناکی ایجاد میشوند. بعضی اوقات تعداد این جوشها چنان در دهان زیاد است که بیمار از درد دهان خود را نمیتواند باز کند و مشکلاتی برای غذا خوردن وی ایجاد میشود.
تشخیص
با وجود اعلایم کلینکی روشن بیماری، برای تشحیص نمونهبرداری و آزمایش باید صورت گیرد. پارمترهای آزمایشگاهی یا تستهای مناسب برای یافتن این بیماری موجود است. سلولهای مرده در محل التهاب و سوراخهای موجود در غشای پایهای میتواند راهی برای تشخیص این سندرم باشد.
درمان
بهترین کار کنار گذاشتن داروهایی است، که بیمار در طول ۲-۳ هفتهٔ قبل از بروز بیماری مصرف میکردهاست. عفونتهای مایکوپلاسمایی باید با تتراسایکلین درمان شوند، البته برای کودکان بهتر است از آنتیبیوتیکهای مایکوپلاسمایی پرهیز شود.
پیشبینی
مرگ در اثر این بیماری در ۶٪ درصد موارد اتفاق افتادهاست. البته اگر بیمار به حالت نکروز سمی اپیدرم برسد تا ۵۰٪ امکان مرگ برای بیمار وجود دارد.
منابع
- blitz-a-t vom 20. November ۲۰۰۷: «Vorsicht! Schwerwiegende Überempfindlichkeitsreaktionen unter Strontiumranelat (Protelos)» [۱]
مشارکتکنندگان ویکیپدیا، «Stevens-Johnson-Syndrom»، ویکیپدیای آلمانی، دانشنامهٔ آزاد (بازیابی در ۱۲ اوت ۲۰۱۱).
ادامه مطلب
| سلولیت (عفونت بافت) | |
|---|---|

Infected left shin
|
|
| آیسیدی-۱۰ | L03 |
| آیسیدی-۹ | 682.9 |
| دادگان بیماریها | ۲۹۸۰۶ |
| مدلاین پلاس | 000855 |
| ایمدیسین | med/۳۱۰ emerg/88 derm/۴۶۴ |
| سمپ | D002481 |
سلولیت (به انگلیسی: Cellulitis) نوعی عفونت باکتریایی است که پوست را درگیر میکند. این بیماری مخصوصاً غشاء میانپوستی و چربی زیرجلدی را تحت تأثیر قرار میدهد. علائم و نشانههای این بیماری شامل یک ناحیهٔ قرمز رنگ است که ظرف چند روز وسیعتر میشود. اطراف این محدودهٔ قرمز رنگ عموماً دارای لبه نیست و ممکن است پوست ورم کند. در حالی که امکان دارد با فشار دادن قسمت قرمز، رنگ آن سفید شود، اما این امر همیشه صدق نمیکند. محدودهٔ عفونت کرده معمولاً دردناک است.[۱] گاه و بیگاه عروق لنفاوی هم ممکن است درگیر این بیماری شوند[۱][۲] و شخص مبتلا ممکن است تب کند و یا احساس خستگی نماید.[۳]
پاها و صورت معمولاً اعضایی از بدن هستند که درگیر این بیماری میشوند، هرچند که سلولیت ممکن است در هر قسمتی از بدن اتفاق بیفتد. پاها معمولاً بعد از بریده شدن و شکافت پوست عفونی میشوند. از دیگر عوامل خطر میتوان به مرض چاقی، تورم پا و کهنسالی اشاره کرد. در مورد عفونت صورت، مواردی مانند بریده شدن و شکافت پوست از قبل، الزاماً باعث این بیماری نمیشوند. باکتریهایی که معمولاً این بیماری را به وجود میآورند شامل استرپتوکوک و استافیلوکوکوس اورئوس هستند. بر خلاف سلولیت، باد سرخ نوعی عفونت باکتریایی است که بیشتر لایههای سطحی پوست را درگیر مینماید و شامل قسمتی قرمز رنگ با لبههای کاملاً مشخص میشود و بیشتر با تب همراه است.[۱] عفونتهای جدیتری همچون کورک استخوان| عفونت استخوان یا التهاب غلاف نکروزان را باید غیرمحتمل انگاشت.[۲]
تشخیص این بیماری معمولاً با کشت سلولی صورت میگیرد که علائم و نشانههای آن در این روش مشخص میشود، البته این روش به ندرت امکانپذیر است.[۱] این بیماری اغلب با آنتیبیوتیکهای خوراکی از قبیل سفالکسین، آموکسیسیلین و یا کلوگزاسیلین درمان میشود.[۱][۴] برای افرادی که شدیداً به پنیسیلین حساسیت دارند، اریترومایسین یا کلیندامایسین میتواند مورد استفاده قرار گیرد.[۴] هرگاه استافیلوکوک اورئوس مقاوم به متیسیلین یا (MRSA) عاملی برای نگرانی باشد، توصیه میشود که از داکسیسایکلین یا تری متوپریم / سولفامتوکسازول نیز به صورت اضافه استفاده شود.[۱] این نگرانی در مورد وجود چرک یا عفونتهای پیشین به MRSA است.[۱][۳] استروئیدها میتوانند سرعت بهبودی در بیماران تحت درمان با آنتیبیوتیک را تسریع بخشند.[۱] بالا آوردن منطقهٔ عفونت کرده میتواند مفید باشد.[۲] داروی مسکن نیز تأثیرگذار است.[۴]
حدود ۹۵ درصد از بیماران بعد از هفت تا ده روز درمان حالشان رو به بهبود میرود.[۳] عوارض بالقوهٔ این بیماری شامل تشکیل ورم چرکی است. عفونتهای پوستی هر ساله، از هر هزار نفر دو نفر را مبتلا میسازد.[۱] سلولیت در سال ۲۰۱۰ باعث مرگ ۲۷ هزار نفر در سراسر دنیا شد.[۵] در بریتانیا، سلولیت دلیل ۱٫۶ پذیرش بیمارستانها بوده است.[۴]
نگارخانه
ادامه مطلب
| سل | |
|---|---|

رادیوگرافی قفسه سینه شخص مبتلا به بیماری سل پیشرفته. عفونت در هر دو سمت ریه با پیکانهای سفید نمایش داده شده و تشکیل حفره سلی با پیکانهای مشکی مشخص شده است.
|
|
| آیسیدی-۱۰ | A15–A19 |
| آیسیدی-۹ | 010–018 |
| اُمیم | ۶۰۷۹۴۸ |
| دادگان بیماریها | ۸۵۱۵ |
| مدلاین پلاس | 000077 ۰۰۰۶۲۴ |
| ایمدیسین | med/۲۳۲۴ emerg/618 radio/۴۱۱ |
| پیشنت پلاس | سل |
| سمپ | D014376 |
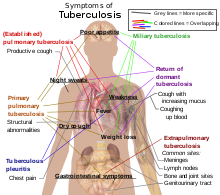
سل یک بیماری عفونی شایع، و در بسیاری از موارد مرگبار است. این بیماری توسط گونههای مختلف میکوباکتریا، به طور معمول «مایکوباکتریوم توبرکلوزیس» ایجاد میشود.[۱] سل به طور معمول به ریهها حمله میکند، اما بر قسمتهای دیگر بدن نیز میتواند تأثیر گذار باشد. وقتی افرادی که عفونت سلی فعال دارند سرفه، عطسه، و یا بزاق خود را از طریق هوا منتقل میکنند سل از طریق هوا پخش میشود.[۲] اغلب عفونتها بدون علامت و پنهان هستند. اما معمولاً از هر ده عفونت نهفته یک عفونت در نهایت پیشرفت کرده و به بیماری فعال تبدیل میشود. اگر سل درمان نشود، بیش از ۵۰٪ از افرادی که به آن آلوده میشوند را به کام مرگ میکشد.
علائم کلاسیک عفونت سل فعال عبارتند از سرفه مزمن با خلط آغشته به خون، تب، تعریق شبانه، و کاهش وزن. (سل قبلاً به دلیل کاهش وزن افراد به «زوال» مبتلا معروف بود) عفونت اندامهای دیگر باعث طیف وسیعی از علائم میشود. تشخیص سل فعال به رادیولوژی (معمولاً عکس از قفسه سینه با X-ray) و همچنین آزمایشهای میکروسکوپی و کشت میکروبیولوژیک مایعات بدن متکی است. تشخیص سل نهفته متکی بر تست پوستی توبرکولین (TST) و آزمایش خون میباشد. درمان دشوار است و مستلزم آن است که آنتی بیوتیکهای متعددی در یک مدت زمان طولانی استفاده شوند. ارتباطات اجتماعی نیز غربالگری و در صورت لزوم مورد درمان قرار میگیرند. مقاومت در برابر آنتی بیوتیکها یک مشکل رو به رشد در عفونتهای سل مقاوم در برابر داروهای چندگانه (MDR-TB) میباشد. برای جلوگیری از سل، مردم باید برای این بیماری غربالگری و با واکسن bacillus Calmette-Guérin واکسینه شوند.
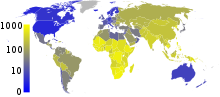
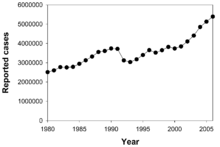
کارشناسان معتقدند که یک سوم از جمعیت جهان مبتلا به «M. tuberculosis» هستند،[۳] و در هر ثانیه یک نفر به این تعداد افزوده میشود.[۳] در سال ۲۰۰۷، ۱۳٫۷ میلیون مورد مزمن در سطح جهان فعال بودند.[۴] در سال ۲۰۱۰، حدود ۸٫۸ میلیون مورد جدید به وجود آمده و ۱٫۵ میلیون مورد به مرگ انجامید، که عمدتاً در کشورهای در حال توسعه رخ داده است.[۵] تعداد مطلق موارد ابتلا به سل از سال ۲۰۰۶ رو به کاهش بوده است، و موارد جدید از سال ۲۰۰۲ کاهش یافته است.[۵] سل به طور یکنواخت در سراسر جهان توزیع نشده است. تست توبرکولین حدود ۸۰٪ از جمعیت حاضر در بسیاری از کشورهای آسیایی و آفریقایی مثبت بوده است، اما تنها تست ۵–۱۰٪ از جمعیت ایالات متحده مثبت بوده است.[۱] مردم کشورهای در حال توسعه به دلیل کمبود ایمنی، بیشتر در معرض خطر سل قرار دارند. به طور معمول، این افراد به دلیل آلوده بودن به HIV و ابتلا به ایدز گرفتار سل میشوند.[۶] بیش از ۹۰٪ موارد بیماری و مرگ ناشی از سل در کشورهای در حال توسعه رخ میدهد، کشورهایی که%۷۵ موارد بیماری در آنها به فعالترین گروه سنی به لحاظ اقتصادی (یعنی ۱۵ تا ۵۴ سالگی) تعلق دارد. در این کشورها یک فرد بزرگسال مبتلا به سل بطور متوسط ۳ الی ۴ ماه قادر به کار کردن نبوده و لذا۲۰تا ۳۰٪ درآمد سالانه خانواده وی از دست میرود. با مرگ چنین فردی بطور متوسط۱۵ سال درآمد خانواده بطور یکجا از بین خواهد رفت. بیماری سل که بزرگترین علت مرگ ناشی از بیماریهای عفونی تک عاملی است (حتی بیشتر از ایدز، مالاریا و سرخک)، دارای مرتبه دهم در بار جهانی بیماری هاست و پیش بینی میشود تا سال ۲۰۲۰ همچنان جایگاه کنونی خود را حفظ کند و یا تا رتبه هفتم بالا رود.[۷]
محتویات
علائم و نشانهها
حدود ۵–۱۰٪ از افرادی که HIV ندارند، اما آلوده به سل هستند در طول عمر خود دچار بیماری فعال میشوند.[۹] در مقابل، ۳۰٪ از افرادی که آلوده به HIV و سل هستند دچار بیماری فعال میگردند.[۹] سل میتواند هر قسمتی از بدن را آلوده کند، اما معمولاً در ریهها رخ میدهد (شناخته شده به عنوان سل ریوی).[۱۰] سل خارج ریوی زمانی رخ میدهد که سل به خارج از ریهها نفوذ میکند. سل خارج ریوی همچنین میتواند همزمان با سل ریوی وجود داشته باشد.[۱۰] علائم و نشانههای عمومی عبارتند از تب، لرز، تعریق شبانه، از دست دادن اشتها، کاهش وزن، و خستگی.[۱۰] همچنین پدیده انگشت چماقی قابل توجهی نیز میتواند رخ دهد.[۹]
ریوی
اگر یک عفونت سل فعال شود، در حدود ۹۰٪ از مردم در ریهها بروز میکند.[۶][۱۱] علائم میتواند شامل درد قفسه سینه و سرفههای طولانی باشد که تولید خلط میکنند. در حدود ۲۵٪ از افراد هیچ علائمی ندارند (یعنی آنها «بدون علامت» باقی میمانند).[۶] گاهی اوقات، افراد دچار سرفههای خونین در مقادیر کم میشوند. در موارد نادر، عفونت میتواند به تضعیف شریان ریوی بینجامد، که منجر به خونریزی شدید به نام آنوریسم راسموسن میشود. سل میتواند تبدیل به یک بیماری مزمن شده و باعث زخمهای گسترده در نرمه فوقانی ریهها شود. قسمت فوقانی ریهها بیشتر تحت تأثیر قرار میگریند.[۱۰] دلیل آن به طور کامل روشن نیست.[۱] شاید قسمت فوقانی ریهها به دلیل جریان هوای بهتر[۱] یا خروجی ضعیف غدد لنفاوی بیشتر تحت تأثیر قرار میگیرند.[۱۰]
خارج ریوی
در ۱۵–۲۰٪ از موارد فعال، عفونت به خارج از اندامهای تنفسی گسترش مییابد که باعث بروز انواع دیگر سل میشود[۱۲] به سلی که خارج از اندامهای تنفسی رخ میدهد، «سل خارج ریوی» گفته میشود.[۱۳] سل خارج ریوی به طور معمول در افرادی که دچار نقص سیستم ایمنی هستند و کودکان رخ میدهد. سل خارج ریوی در بیش از ۵۰٪ از افرادی که HIV دارند دیده میشود.[۱۳] مکانهای عفونت قابل توجه خارج ریوی عبارتند از: شش شامه (در پلورزی (آماس شامه ریه) سلی)، سیستم عصبی مرکزی (در مننژیت سلی)، و سیستم لنفاوی (در سل غدد لنفاوی گردن). از میان مکانهای دیگر سل خارج ریوی در دستگاه ادراری تناسلی (در سل ادراری تناسلی) و در استخوانها و مفاصل (در سل ستون فقرات) نیز اتفاق میافتد. هنگامی که این بیماری در استخوان هم گسترش مییابد، آن را به عنوان «سل استخوانی» نیز میشناسند،[۱۴] که نوعی از استئومیلیت (کورک استخوانی) میباشد.[۱] یک نوع بالقوه جدی تر و شایع سل، سل «منتشر» نام دارد، که معمولاً به عنوان سل ارزنی یا میلیاری شناخته شده است.[۱۰] سل ارزنی در حدود ۱۰٪ از موارد سل خارج ریوی را تشکیل میدهد.[۱۵]
علل
مایکوباکتری
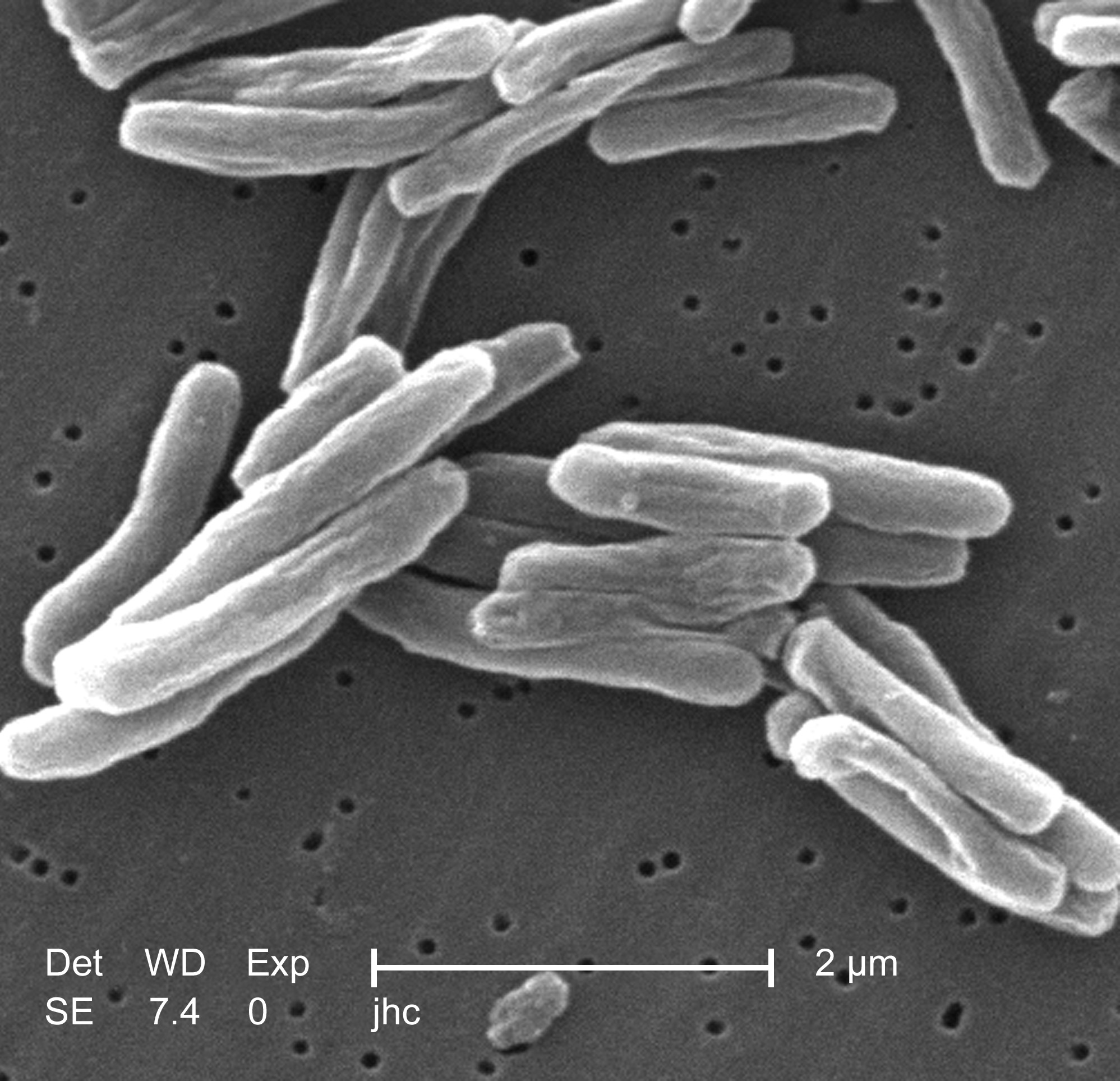
علت اصلی سل «مایکوباکتریوم توبرکلوزیس»، یک باسیل بی حرکت هوازی کوچک است.[۱۰] بسیاری از ویژگیهای بالینی منحصربهفرد این پاتوژن به دلیل محتوای چربی بالای آن ایجاد میشود.[۱۶] این باسیل هر ۱۶ –۲۰ ساعت یک بار تقسیم میشود. سرعت آن در مقایسه با دیگر باکتریها که معمولاً در کمتر از یک ساعت تقسیم میشوند آهسته است.[۱۷] غشای بیرونی میکوباکتریا از دولایه لیپیدی تشکیل شده است.[۱۸] اگر یک رنگ آمیزی گرم انجام شود، MTB یا رنگ بسیار کم «گرم مثبت» دارد یا اصلاً رنگی به خود نمیگیرد چرا که دیواره سلولی آن دارای محتوای چربی و اسید مایکولیک بالا میباشد.[۱۹] MTB میتواند در برابر مواد ضد عفونی کننده ضعیف مقاومت کند و میتواند در یک شرایط خشک هفتهها زنده بماند. در طبیعت، باکتری تنها میتواند در داخل سلول یک ارگانیسم میزبان رشد کند، اما «M. tuberculosis» میتوان در آزمایشگاه کشت شود.[۲۰]
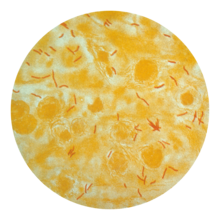
با استفاده از رنگهای بافتی بر روی نمونههای بلغم به دست آمده از سینه، دانشمندان میتوانند MTB را در زیر یک میکروسکوپ معمولی (نوری) تشخیص دهند. (بلغم، «خلط» نیز نامیده میشود) MTB رنگهای خاصی را حتی بعد از واکنش با محلول اسیدی حفظ میکند، بنابراین به عنوان باسیل اسید-فاست (مقاوم در برابر رنگ بری اسید) (AFB) طبقهبندی شده است.[۱][۱۹] دو تکنیک رنگ آمیزی اسید فاست شایع تر هستند: رنگ آمیزی Ziehl–Neelsen، که AFBها را به رنگ قرمز روشن در میآورد که به وضوح در برابر یک پس زمینه آبی رنگ دیده میشوند،[۲۱] و رنگ آمیزی auramine-rhodamine و پس از آن میکروسکوپ فلورسانس.[۲۲]
مجموعه «M. tuberculosis»(MTBC) شامل چهار میکوباکتری سل زای دیگر میشود: “M. bovis,” “M. africanum,” “M. canetti,” و “M. microti”.[۲۳] «M. africanum» شایع نیست، اما علت قابل توجه ایجاد سل در بخشهایی از آفریقا میباشد.[۲۴][۲۵] «M. bovis» یک علت شایع سل بود، اما با ظهور شیر پاستوریزه تا حد زیادی این میکوباکتریوم را به عنوان یک مشکل بهداشت عمومی در کشورهای توسعه یافته از بین برد.[۱][۲۶] «M. canetti» نادر است و به نظر میرسد به شاخ آفریقا محدود باشد، اگر چه چند مورد در مهاجران آفریقایی دیده شده است.[۲۷][۲۸] «M. microti» نیز نادر بوده و اغلب در افراد دارای نقص ایمنی دیده میشود، اما این پاتوژن میتوانست شایع تر از آن باشد که ما فکر میکنیم.[۲۹]
دیگر میکوباکتریهای بیماری زای شناخته شده عبارتند از “M. leprae,” “M. avium,” و “M. kansasii”. دو گونه آخر به عنوان «میکوباکتریهای غیر سلی» (NTM) طبقهبندی شدهاند. NTM باعث ایجاد سل یا جذام نمیشود، اما آنها منجر به بیماریهای ریوی میشوند که شبیه سل است.[۳۰]
عوامل خطر ساز
عوامل متعددی مردم را بیشتر مستعد ابتلا به عفونت سل مینمایند. مهمترین عامل خطر ساز در سراسر جهان HIV است؛ ۱۳٪ درصد از تمام موارد ابتلا به سل آلوده به ویروس HIV هستند.[۵] این مشکل در کشورهای جنوب صحرای آفریقا، که در آن نرخ HIV بالاست شایع است.[۳۱][۳۲] سل به ازدحام بیش از حد و تغذیه نامناسب بسیار مرتبط است. این ارتباط باعث میشود سل یکی از بیماریهای فقر اصلی باشد.[۶] این دسته از افراد در معرض خطر بالایی برای عفونت سل قرار دارند: افرادی که مواد مخدر ممنوع تزریق میکنند، ساکنان و کارگران و کارمندان مکانهایی که در آن افراد آسیب پذیر تجمع میکنند (به عنوان مثال، زندانها و پناهگاههای مخصوص بی خانمانها)، افرادی که فقیر هستند و به مراقبتهای پزشکی مناسب دسترسی ندارند، اقلیتهای قومی با خطر بالا، بچهها در تماس نزدیک با افراد با خطر بالا، و ارائه دهندگان مراقبتهای بهداشتی که در خدمت این افراد میباشد.[۳۳] بیماری ریوی مزمن، یکی دیگر از عوامل خطر ساز قابل توجه است. بیماری سیلیکوز خطر را حدوداً ۳۰ برابر میکند.[۳۴] افرادی که سیگار میکشند نسبت به غیر سیگاریها تقریباً دو برابر در معرض خطر ابتلا به سل هستند.[۳۵] بیماریهای دیگر نیز میتوانند خطر ابتلا به سل را افزایش دهند، از جمله اعتیاد به الکل[۶] و دیابت قندی (خطر را سه برابر میکند).[۳۶] برخی داروها، مانند کورتیکواستروئیدها و اینفیلیکسیماب (یک آنتی بادی مونوکلونال ضد αTNF)، به خصوص در جوامع توسعه یافته از عوامل خطر ساز بسیار مهم هستند.[۶]همچنین، یک استعداد ژنتیکی[۳۷] نیز وجود دارد، اما دانشمندان مشخص نکردهاند که چقدر مهم است.[۶]
مکانیسم
انتقال
هنگامی که افراد مبتلا به سل فعال آواز بخوانند، سرفه، عطسه، صحبت، یا تف کند، آنها قطرات عفونی معلق در هوا به قطر ۰٫۵ تا ۵ میکرومتر را پخش میکنند. تنها یک عطسه میتواند تا ۴۰٬۰۰۰ قطره را منتشر کند.[۳۸] هر قطره میتواند بیماری را منتقل کند زیرا دوز عفونی سل بسیار پایین است. (کسی که کمتر از ۱۰ باکتری را استنشاق کند میتواند آلوده شود).[۳۹]
مردمی که در تماسهای طولانی مدت، مکرر، یا نزدیک با افراد مبتلا به سل هستند در معرض خطر آلوده شدن به عفونت، با نرخ عفونت حدود ۲۲ درصد میباشند.[۴۰] یک فرد مبتلا به سل فعال، اما درمان نشده میتواند ۱۰–۱۵ نفر (یا بیشتر) را در هر سال آلوده کند.[۳] به طور معمول، تنها افراد دارای سل فعال این بیماری را انتقال میدهند. تصور نمیشود که افراد مبتلا به عفونت نهفته مسری باشند.[۱] احتمال انتقال از فردی به فرد دیگر به عوامل متعددی بستگی دارد. این عوامل عبارتند از تعداد قطرات عفونی که حامل منتشر میکند، کارآمدی تهویه محیط زیست افراد، مدت زمان در معرض قرار گرفتن، میزان واگیردار بودن گونه «M. tuberculosis»، و سطح ایمنی در فرد غیرآلوده.[۴۱] برای جلوگیری از آبشار شیوع فرد به فرد، افراد مبتلا به سل فعال («آشکار») را جدا کنید و آنها را تحت رژیمهای داروی ضد سل قرار دهید. پس از حدود دو هفته درمان مؤثر، به طور کلی افراد مبتلا به عفونت فعال غیر مقاوم برای دیگران مسری نخواهند بود.[۴۰] اگر کسی آلوده شود، به طور معمول سه تا چهار هفته طول میکشد تا شخص به تازگی آلوده شده به اندازه کافی برای انتقال بیماری به دیگران مسری شود.[۴۲]
بیماری زایی
در حدود ۹۰٪ درصد از افرادی که مبتلا به «M. tuberculosis» هستند عفونت سل نهفته بدون علامت دارند (که گاهی اوقات LTBI نامیده میشود).[۴۳] این افراد در طول عمر خود تنها ۱۰٪ شانس پیشرفت عفونت نهفته به بیماری سل فعال آشکار را دارند.[۴۴] برای افراد مبتلا به HIV، خطر اینکه آنها به سل فعال مبتلا شوند به نزدیک ۱۰٪ در سال میرسد.[۴۴] اگر درمان مؤثر داده نشود، میزان مرگ و میر در موارد سل فعال تا ۶۶٪ میباشد.[۳]
عفونت سل وقتی که میکوباکتریها به حبابچههای ریوی میرسد شروع میشود، جایی که آنها به endosomes از ماکروفاژهای آلوئولی حمله کرده و در داخل آن تکثیر میشوند.[۱][۴۵] محل اولیه عفونت در ریهها، معروف به «کانون گان»، یا در قسمت فوقانی لوب تحتانی، یا در قسمت تحتانی لوب فوقانی واقع شده است.[۱] سل ریهها میتواند از طریق عفونت از جریان خون نیز ایجاد شود، که به عنوان کانون سیمون شناخته شده است. یک عفونت کانون سیمون به طور معمول در بالای ریه دیده میشود.[۴۶] این انتقال خونی میتواند بیماری را به محلهای دور تر از جمله غدد لنفاوی محیطی، کلیهها، مغز، و استخوانها نیز گسترش دهد.[۱][۴۷] سل بر تمام قسمتهای بدن تأثیر میگذارد، هر چند به دلایل نامعلوم به ندرت قلب، عضلات اسکلتی، لوزالمعده، یا تیروئید را تحت تأثیر قرار میدهد.[۴۸]
سل به عنوان یکی از بیماریهای التهابی گرانولومــاتوز دستهبندی میشود. ماکروفاژها، T لنفوسیتها، B لنفوسیتها، و فیبروبلاستها از جمله سلولهایی هستند که جمع میشوند تا گرانولومها را تشکیل دهند. لنفوسیتها ماکروفاژهای آلوده را احاطه میکنند. گرانولوم از انتشار میکوباکتریها جلوگیری کرده و یک محیط محلی را برای تعامل سلولهای سیستم ایمنی بدن فراهم مینماید. باکتریها در داخل گرانولوم میتوانند ساکت بمانند، که منجر به عفونت نهفته میشود. یکی دیگر از ویژگیهای گرانولومها توسعه مرگ سلولی غیرطبیعی (نکروز) در مرکز برآمدگیها است. برای چشم غیر مسلح، این نکروز، بافتی نرم، شبیه پنیر سفید دارد و نکروز پنیری نامیده میشوند.[۴۹]
باکتریهای سل میتوانند از یک منطقه آسیب دیده بافت وارد جریان خون شود. آنها میتوانند در سراسر بدن گسترش یافته و کانونهای متعدد عفونت را ایجاد کنند، که مانند برآمدگیهای کوچک سفید در بافتها دیده میشوند.[۵۰] این نوع شدید از بیماری سل سل ارزنی نامیده میشود. این شکل از سل بیشتر در کودکان و افراد مبتلا به HIV شایع است.[۵۱] افراد مبتلا به سل منتشر، حتی با درمان هم میزان مرگ و میر بالایی دارند (حدود ۳۰٪).[۱۵][۵۲]
در بسیاری از مردم، عفونت ظهور و افول دارد. تخریب و نکروز بافت اغلب با بهبود و فیبروز متعادل میشود.[۴۹] بافت متأثر، با جای زخم و حفرههای پر شده با مواد نکروز پنیری جایگزین میشود. در بیماری فعال، برخی از این حفرهها به راههای هوایی نایژهها پیوسته و این مواد میتوانند با سرفه کردن بیرون بریزند. این مواد حاوی باکتری زنده هستند و میتوانند عفونت را پخش کنند. درمان با آنتی بیوتیکهای مناسب، باکتریها را میکشد و امکان بهبودی را فراهم میکند. هنگامی که بیماری درمان شد، مناطق آسیب دیده توسط بافتهای همبند جای زخم جایگزین میشوند.[۴۹]
تشخیص
سل فعال
تشخیص سل فعال صرفاً بر اساس علائم و نشانهها دشوار است.[۵۳] همچنین تشخیص بیماری در افرادی که دچار دپرسیون ایمنی هستند نیز مشکل است.[۵۴] با این حال، افرادی که دارای علائم بیماری ریوی یا علائم مزاجی هستند که بیش از دو هفته ادامه مییابند ممکن است سل داشته باشند.[۵۴] یک عکس از قفسه سینه با پرتو ایکس و چند کشت خلط برای باسیلهای اسید فاست به طور معمول بخشی از ارزیابی اولیه میباشند.[۵۴] آزمونهای اینترفرون گاما ترشح شده (IGRAها) و آزمونهای پوستی توبرکولین در جوامع در حال توسعه مفید نیستند.[۵۵][۵۶] IGRAها در افراد مبتلا به HIV نیز محدودیتهای مشابهی دارند.[۵۷][۵۸]
یک تشخیص قطعی سل زمانی انجام میشود که «M. tuberculosis» در یک نمونه بالینی شناسایی شود (برای مثال، خلط چرک، یا یک بیوپسی از بافت). با این حال، روند دشوار کشت برای این ارگانیسم دارای رشد آهسته میتواند دو تا شش هفته برای کشت خون یا خلط طول بکشد.[۵۹] از این رو، درمان اغلب قبل از تأیید کشتها آغاز میشود.[۶۰]
آزمونهای تقویت اسید نوکلئیک و آزمایش آدنوزین آمیناز میتوانند سل را به سرعت تشخیص دهند.[۵۳] با این حال، این آزمایشها به طور مداوم توصیه نمیشوند چرا که آنها به ندرت چگونگی درمان یک فرد را تغییر میدهند.[۶۰] آزمایش خون برای تشخیص آنتی بادیها دقیق یا حساس نیستند، بنابراین توصیه نمیشوند.[۶۱]
سل نهفته
تست پوستی توبرکولین مانتو اغلب برای غربالگری افراد در معرض خطر بالای بیماری سل استفاده میشود.[۶۲] این تست میتواند در افراد مبتلا به سارکوئیدوز، لنفوم هوچکین، و سوء تغذیه به صورت کاذب منفی باشد. مهمتر از همه، این تست میتواند در افرادی که سل فعال دارند به صورت کاذب منفی باشد.[۱] سنجش اینترفرون گامای آزاد (IGRAها) در یک نمونه خون برای افرادی که تست مانتو مثبت دارند توصیه میشود.[۶۰] IGRAها تحت تأثیر ایمنسازی یا اکثر میکوباکتریهای زیستمحیطی قرار نمیگیرند، بنابراین آنها نتایج مثبت کاذب کمتری ارائه میکنند.[۶۳] با این حال آنها تحت تأثیر «M. szulgai»، «M. marinum» و «M. kansasii» قرار میگیرند.[۶۴] IGRAها زمانی که همراه با تست پوستی استفاده میشوند میتوانند حساسیت بیشتری داشته باشند. اما وقتی IGRAها به تنهایی استفاده میشوند میتوانند حساسیت کمتری نسبت به تست پوستی داشته باشند.[۶۵]
پیشگیری
تلاش برای جلوگیری و کنترل سل بر واکسیناسیون نوزادان و تشخیص و درمان مناسب موارد فعال متکی میباشد.[۶] سازمان بهداشت جهانی (WHO) موفقیتهایی را در رژیمهای درمانی بهبود یافته به دست آورده است. کاهش کوچکی در تعداد موارد دیده شده است.[۶]
واکسنها
تا سال ۲۰۱۱، تنها واکسن سل موجود(Bacillus Calmette-Guérin یا ب.ث. ژ) میباشد. BCG در برابر بیماریهای منتشر شده در دوران کودکی مؤثر است، اما حفاظت متناقضی را در برابر ابتلا به سل ریوی ایجاد میکند.[۶۶] با این حال، این گستردهترین واکسن مورد استفاده در سراسر جهان است، که بیش از ۹۰٪ از همه کودکان را واکسینه میکند.[۶] با این حال، ایمنی ایجاد شده توسط آن بعد از حدود ده سال کاهش مییابد.[۶] سل در اکثر نقاط کانادا، بریتانیا، و ایالات متحده شایع نیست، بنابراین BCG فقط برای افرادی که در معرض خطر بالا قرار دارند استفاده میشود.[۶۷][۶۸][۶۹] یکی از دلایل عدم استفاده از واکسن این است که باعث میشود تست پوستی توبرکولین مثبت کاذب شود، که این آزمون را برای غربالگری این بیماری بی فایده مینماید.[۶۹] واکسنهای جدید در دست تهیه هستند.[۶]
بهداشت عمومی
سازمان جهانی بهداشت در سال ۱۹۹۳ سل را «وضعیت اضطراری برای بهداشت جهانی» اعلام کرد.[۶] در سال ۲۰۰۶، مشارکت توقف سل، طرح جهانی برای متوقف کردن سل را مطرح کرد که قرار است تا سال ۲۰۱۵ جان ۱۴ میلیون نفر را حفظ کند.[۷۰] تعدادی از اهداف تعیین شده به احتمال زیاد تا سال ۲۰۱۵ حاصل نمیشوند، این امر بیشتر به دلیل افزایش سل مرتبط با HIV و ظهور سل مقاوم در برابر چند دارو (MDR-TB) میباشد.[۶] سیستم طبقهبندی سل که جامعه بیماریهای صدری آمریکا آن را تهیه کرده است در برنامههای بهداشت عمومی استفاده میشود.[۷۱]
مدیریت
درمان سل از آنتی بیوتیکها برای از بین بردن باکتریها استفاده میکند. درمان مؤثر سل مشکل است که به دلیل ساختار غیر معمول و ترکیب شیمیایی دیواره سلولی میکوباکتریومی میباشد. دیواره سلولی داروها را بیرون نگه میدارد و باعث میشود که بسیاری از آنتی بیوتیکها بی اثر شوند.[۷۲] دو آنتی بیوتیکی که بیشترین استفاده را دارند ایزونیازید و ریفامپیسین هستند و درمان میتواند ماهها ادامه یابد.[۴۱] در درمان سل نهفته معمولاً تنها از یک آنتی بیوتیک استفاده میشود.[۷۳] بیماری سل فعال، به منظور کاهش خطر ایجاد مقاومت در برابر آنتی بیوتیک در باکتری، با ترکیبی از چند آنتی بیوتیک بهتر درمان میشود.[۶] افراد مبتلا به عفونت نهفته نیز درمان میشوند تا از ابتلای آنها به بیماری سل فعال در آینده جلوگیری شود.[۷۳] WHO درمان با مشاهده مستقیم را توصیه میکند. در این روش درمانی، ارائه دهنده مراقبتهای بهداشتی مصرف دارو توسط فرد را مشاهده مینماید. هدف کاهش تعداد افرادی است که آنتی بیوتیکها را به طور مناسب مصرف نمیکنند.[۷۴] با این حال، شواهد برای حمایت از درمان با مشاهده مستقیم ضعیف است.[۷۵] روشهایی که به مردم یادآوری میکند که درمان بسیار مهم است مؤثر میباشند.[۷۶]
شروع جدید
در سال ۲۰۱۰، درمان توصیه شده برای سل ریوی تازه بروز کرده، ترکیبی از آنتی بیوتیکها به مدت شش ماه میباشد. برای دو ماه اول، ریفامپیسین، ایزونیازید، پیرازینامید و اتامبوتول تجویز شود. در چهار ماه بعد، تنها ریفامپیسین و ایزونیازید تجویز شود.[۶] در صورتی که مقاومت به ایزونیازید بالا باشد، میتوان به جای آن از اتامبوتول در چهار ماه پایانی استفاده کرد.[۶]
بیماری عود کننده
اگر سل عود کند، قبل از شروع درمان برای تعیین آنتی بیوتیکهایی که به آن حساس است آزمایش انجام دهید.[۶] اگر سل مقاوم به چند دارو (MDR-TB) تشخیص داده شود، درمان با حداقل چهار آنتی بیوتیک مؤثر برای ۱۸–۲۴ ماه توصیه میشود.[۶]
مقاومت به دارو
مقاومت اولیه هنگامی رخ میدهد که فرد به یک گونه مقاوم سل مبتلا میشود. فرد مبتلا به سل کاملاً حساس (مستعد) ممکن است در طول درمان دچار مقاومت ثانویه (اکتسابی) شود. یک فرد در صورتی که از رژیم تجویز شده به طور مناسب پیروی نکند (عدم تطابق)، یا اگر از داروهایی با کیفیت پایین استفاده کند، ممکن است به دلیل درمان نامناسب دچار مقاومت ثانویه شود.[۷۷] سل مقاوم در برابر دارو، یک مسئله جدی در بهداشت عمومی بسیاری از کشورهای در حال توسعه است. درمان سل مقاوم در برابر دارو طولانیتر است و به داروهای گرانتر نیاز دارد. MDR-TB به عنوان مقاومت در برابر دو داروی مؤثر رده اول سل: ریفامپیسین و ایزونیازید، تعریف شده است. سل بسیار مقاوم در برابر دارو در برابر سه یا بیشتر از سه مورد از شش کلاس داروهای رده دوم مقاوم است.[۷۸] سل کاملاً مقاوم در برابر دارو نسبت به تمام داروهایی که در حال حاضر استفاده میشود مقاوم است. سل کاملاً مقاوم در برابر دارو برای اولین بار در سال ۲۰۰۳ در ایتالیا مشاهده شد، اما از آن به بعد تا سال ۲۰۱۲ به طور گسترده گزارش نشده است.[۷۹] موارد multidrug-resistant TB) MDR-TB) در سال ۲۰۱۳ حدود ۳٫۵٪ در موارد جدید و ۲۰٫۵٪در موارد قدیمی و قبلی بوده است. پیش بینی میشد حدود۳۰۰/۰۰۰ مورد MDR-TB در سال ۲۰۱۳ وجود داشته باشند که ۱۳۶۰۰۰ نفر شناسایی و گزارش شدندیعنی در حدود ۴۵٪ موارد.[۸۰]
پیش شناخت
پیشرفت عفونت سل به بیماری سل آشکار زمانی رخ میدهد که باسیل بر دفاعهای سیستم ایمنی غلبه و شروع به تکثیر کند. در بیماری سل اولیه (حدود ۱–۵٪ از موارد)، این پیشرفت به سرعت پس از عفونت اولیه رخ میدهد.[۱] با این حال، در اکثر موارد، یک عفونت نهفته بدون هیچ نشانه آشکاری رخ میدهد.[۱] این باسیلهای خفته باعث ایجاد سل فعال در ۵–۱۰٪ از این موارد نهفته میشوند، و اغلب این امر سالها پس از عفونت اتفاق میافتد.[۹]
خطر فعال شدن مجدد با سرکوب سیستم ایمنی افزایش مییابد، مانند آنچه که از آلودگی به HIV ناشی میشود. در افراد مبتلا به «M. tuberculosis» و HIV، خطر فعال شدن مجدد به ۱۰٪ در سال افزایش مییابد.[۱] مطالعاتی که از طرحهای DNA نژادهای «M. tuberculosis» استفاده میکنند، نشان میدهند که عفونت مجدد باعث عود سل بیشتر از آنچه قبلاً تصور میشد میشود.[۸۱] عفونت مجدد ممکن است موجب بیش از ۵۰٪ از موارد فعال شده مجدد در مناطقی که در آن سل شایع است بشود.[۸۲] احتمال مرگ و میر ناشی از سل در حدود ۴٪ در سال ۲۰۰۸ بود، که کمتر از ۸٪ در سال ۱۹۹۵ است.
شیوع
حدود یک سوم از جمعیت جهان با «M. tuberculosis» آلوده شده است. در هر ثانیه یک عفونت جدید در مقیاس جهانی رخ میدهد.[۳] با این حال، بسیاری از عفونتها به «M. tuberculosis» منجر به بیماریهای سل نمیشود،[۸۴] و ۹۰–۹۵٪ از عفونتها بدون علامت باقی میمانند.[۴۳] در سال ۲۰۰۷، حدود ۱۳٫۷ میلیون مورد مزمن فعال وجود داشت.[۴] در سال ۲۰۱۰، ۸٫۸ میلیون مورد جدید سل، و ۱٫۴۵ میلیون مرگ و میر شناسایی شد، که بیشتر اینها در کشورهای در حال توسعه اتفاق میافتد.[۵] از این ۱٫۴۵ میلیون مرگ و میر، در حدود ۰٫۳۵ میلیون نفر در افراد آلوده به HIV رخ داد.[۸۵]
سل دومین علت شایع مرگ ناشی از بیماریهای عفونی (پس از مرگ به علت HIV/AIDS) است.[۱۰] تعداد مطلق موارد ابتلا به سل («شیوع») از سال ۲۰۰۵ رو به کاهش بوده است. موارد جدید سل («بروز») از سال ۲۰۰۲ کاهش یافته است.[۵] چین به خصوص پیشرفت چشمگیری داشته است. چین میزان مرگ و میر ناشی از سل خود را بین سالهای ۱۹۹۰ و ۲۰۱۰ حدود ۸۰٪ کاهش داده است.[۸۵] سل در کشورهای در حال توسعه شایع تر است. حدود ۸۰٪ از جمعیت بسیاری از کشورهای آسیایی و آفریقایی در آزمون توبرکولین تست مثبت داشتهاند، اما تنها ۵–۱۰٪ از جمعیت ایالات متحده آزمون مثبت داشتهاند.[۱] کارشناسان امیدوار بودند که سل را به طور کامل کنترل کنند. با این حال، عوامل متعددی کنترل کامل سل را بعید میکند. تهیه یک واکسن مؤثر دشوار بوده است. تشخیص بیماری گران است و زمان زیادی میبرد. درمان چندین ماه طول میکشد. افراد مبتلا به HIV بیشتری گرفتار سل میشوند. سل مقاوم در برابر دارو در دهه ۸۰ مشاهده شد.[۶]
در سال ۲۰۰۷، کشور دارای بیشترین میزان شیوع تخمینی سل، سوازیلند، با ۱٬۲۰۰ مورد در هر ۱۰۰٬۰۰۰ نفر بود. هند بیشترین شیوع در کل را با ۲٫۰ میلیون مورد جدید داشت.[۴] در کشورهای توسعه یافته، سل کمتر شایع است و به طور عمده در مناطق برون شهری یافت میشود. در سال ۲۰۱۰، نرخ TB در هر ۱۰۰٬۰۰۰ نفر در مناطق مختلف جهان بدین شرح بود: در سطح جهانی ۱۷۸، آفریقا ۳۳۲، آمریکا ۳۶، شرق مدیترانه ۱۷۳، اروپا ۶۳، جنوب شرق آسیا ۲۷۸، و غرب اقیانوس آرام ۱۳۹.[۸۵] در کانادا و استرالیا، سل در میان مردم بومی بسیار رایج است، به ویژه در مناطق دور افتاده.[۸۷][۸۸] در ایالات متحده، مرگ و میر ناشی از سل سکنه بومی پنج برابر بیشتر است.[۸۹]
شیوع سل در سنین مختلف متفاوت است. در آفریقا، سل به طور عمده افراد بین ۱۲ و ۱۸ سال و نوجوانان را تحت تأثیر قرار میدهد.[۹۰] با این حال، در کشورهایی که در آن نرخ بروز سل به طور چشمگیری کاهش یافته است (مانند ایالات متحده)، سل عمدتاً بیماری افراد پیر و افراد دارای سیستم ایمنی در معرض خطر است.[۱][۹۱] میزان بروز سل در مردان بیشتر از زنان است. در سال ۲۰۱۳ حدود ۵۱۰۰۰۰زن در نتیجه سل از بین رفته اندو حدود ۱۸۰۰۰۰ نفر از آنان همزمان آلودگی به HIVداشتهاند. در سال ۲۰۰۷، ۱۳٫۷ میلیون مورد مزمن سل در سطح جهان فعال بودند. در سال ۲۰۱۰، حدود ۸٫۸ میلیون مورد جدید به وجود آمده است. با حدود ۱٫۵ میلیون مرگ. در سال ۲۰۱۳ ۹میلیون مورد مزمن در سطح جهان فعال بودند با ۱٫۵ میلیون مرگ (۱٫۱ میلیون بدون آلودگی به HIV و ۳۶۰/۰۰۰ نفر با آلودگی بهHIV) از تمام موارد موجود ۵۶٪ موارد در جنوب شرق آسیا و غرب اقیانوس کبیر بودهاند و ۳۶۰/۰۰۰ نفر آلودگی همزمان سل و HIV داشتهاند. بین سالهای ۲۰۰۰ تا ۲۰۱۳، ۳۷ میلیون تشخیص ودرمان مؤثر سل انجام شده است. در سرتاسر جهان *میزان بروز سل بین سالهای ۲۰۰۰ تا ۲۰۱۳ حدود ۱٫۵٪ در هر سال کاهش داشته است. در همین بازه زمانی *میزان شیوع سل ۴۱٪ کاهش داشته است. بین سالهای ۱۹۹۰تا ۲۰۱۳میزان مرگ و میر سل حدود ۴۵٪ کاهش داشته است. میزان درمان موفقیت آمیز در سال ۲۰۱۳ حدود ۸۶٪ موارد کشف شده بود. هدف جهان تا سال ۲۰۳۵ کاهش ۹۵٪ مرگ ومیرهای ناشی از سل و کاهش ۹۰٪ بروز موارد جدید میباشد.[۹۲]
تاریخچه
سل از دوران باستان همراه انسان بوده است.[۶] قدیمیترین تشخیص بدون ابهام «M. tuberculosis» شامل شواهد این بیماری در بقایای گاومیش کوهان دار آمریکایی است که به ۱۷٬۰۰۰ سال پیش باز میگردد.[۹۳] با این حال، مشخص نیست که آیا سل، در گاومیش به وجود آمده و پس از آن به انسان منتقل شده است، یا اینکه از یک جد مشترک انشعاب یافته است.[۹۴] دانشمندان زمانی اعتقاد داشتند که انسان MTBC را از حیوانات هنگام اهلی کردن آنها گرفته است. با این حال، ژنهای مجموعه «M. tuberculosis» (MTBC) در انسان با MTBC در حیوانات مقایسه شدهاند، و ثابت شده است که این تئوری نادرست است. هر دو گونه باکتری سل یک جد مشترک دارند، که میتوانسته است انسان را در اوایل انقلاب نوسنگی آلوده کرده باشد.[۹۵] باقیماندههای اسکلتی نشان میدهد که انسانهای ماقبل تاریخ (۴۰۰۰ سال قبل از میلاد مسیح) سل داشتهاند. پژوهشگران پوسیدگی مسلول را در ستون فقرات مومیایی مصری یافتهاند که به ۳۰۰۰–۲۴۰۰ سال قبل از میلاد باز میگردد.[۹۶] «Phthisis» یک کلمه یونانی به معنی «مصرف» است که اصطلاح قدیمی برای بیماری سل ریوی میباشد.[۹۷] در حدود ۴۶۰ سال قبل از میلاد، بقراط سل ریوی را به عنوان گستردهترین بیماری در آن زمان شناسایی کرد. افراد مبتلا به سل ریوی تب و سرفه خونین داشتند. سل ریوی تقریباً همیشه کشنده بود.[۹۸] مطالعات ژنتیکی نشان میدهد که سل از حدود سال ۱۰۰ میلادی در میان آمریکاییها وجود داشته است.[۹۹]
قبل از انقلاب صنعتی، فرهنگ عامه اغلب سل را با خون آشامها مرتبط میدانسته است. هنگامی که یکی از اعضای خانواده به دلیل سل فوت میکرد، دیگر اعضای آلوده، سلامت خود را به آرامی از دست میدادند. مردم بر این باور بودند که فرد اصلی مبتلا به سل زندگی را از دیگر اعضای خانواده میربوده است.[۱۰۰]
نوع ریوی مرتبط با برآمدگیها به عنوان یک آسیبشناسی توسط دکتر ریچارد مورتون در سال ۱۶۸۹ تعیین شد.[۱۰۱][۱۰۲]با این حال، سل انواع مختلفی از علائم را داراست، از این رو، سل تا دهه ۲۰ قرن نوزدهم به عنوان یک بیماری واحد شناسایی نشده بود. این بیماری در سال ۱۸۳۹ توسط جی.ال. شوئن سل نامیده شد.[۱۰۳] طی سالهای ۱۸۳۸–۱۸۴۵، دکتر جان کروگان (John Croghan)، صاحب غار ماموت، افراد مبتلا به سل را به داخل غار میبرد به این امید که این بیماری را با درجه حرارت ثابت و خلوص هوای غار درمان کند: آنها ظرف یک سال درگذشتند.[۱۰۴] هرمان برمر (Hermann Brehmer) اولین آسایشگاه سل را در سال ۱۸۵۹ در Sokołowsko، لهستان باز کرد.[۱۰۵]
باسیلی که باعث بیماری سل میشود، «میکوباکتریوم توبرکلوسیس»، در ۲۴ مارس ۱۸۸۲ توسط رابرت کخ (Robert Koch) شناخته و توصیف شد. او موفق به دریافت جایزه نوبل در فیزیولوژی یا پزشکی در سال ۱۹۰۵ برای این کشف شد.[۱۰۶] کخ (Koch) معتقد نبود که بیماری سل گاومیشی (گاوی) و سل انسانی مشابه باشند. این باور درک اینکه که شیر آلوده هم یک منبع عفونت بود را به تعویق انداخت. پس از آن، خطر انتقال از این منبع با اختراع روند پاستوریزاسیون به طور قابل توجهی کاهش یافت. کخ (Koch) در سال ۱۸۹۰ یک عصاره گلیسیرین از باسیل سل را به عنوان «درمان» سل اعلام کرد. او آن را «توبرکولین» نامید. اگرچه «توبرکولین» مؤثر نبود اما از آن به عنوان یک تست غربالگری برای وجود سل پیش بالینی استفاده شد.[۱۰۷]
آلبرت کالمیت (Albert Calmette) و کامیل گوئرین (Camille Guérin) در سال ۱۹۰۶ اولین موفقیت را در ایمنسازی علیه سل به دست آوردند. آنها از گونه ضعیف شده سل گاوی استفاده کردند، و آن واکسن را BCG نامیدند (باسیل کلمنت و گوئرین). واکسن BCG برای اولین بار در سال ۱۹۲۱ در فرانسه بر روی انسانها مورد استفاده قرار گرفت.[۱۰۸] با این حال این واکسن BCG پس از جنگ جهانی دوم تنها در USA بریتانیا، و آلمان به صورت گسترده پذیرفته شد.[۱۰۹]
سل به عنوان گستردهترین بیماری همه گیر فقرای شهری، باعث بزرگترین نگرانی عمومی در قرن ۱۹ و اوایل قرن ۲۰ شد. در سال ۱۸۱۵، یکی از هر چهار مرگ در انگلستان به دلیل «مصرف» بود. در سال ۱۹۱۸، سل دلیل یکی از هر شش مرگ در فرانسه بود. پس از اینکه دانشمندان دهه ۸۰ قرن ۱۹ فهمیدند که بیماری مسری است، سل در فهرست بیماریهای قابل اخطار رسمی در بریتانیا قرار گرفت. کمپینهایی برای جلوگیری از تف کردن مردم در مکانهای عمومی شروع شد و فقرای آلوده به رفتن آسایشگاههایی «تشویق» میشدند که شبیه زندان بود. (آسایشگاهها برای طبقات متوسط و بالا، مراقبتهای عالی و مراقبتهای پزشکی ثابت ارائه میکردند)[۱۰۵] آسایشگاه ظاهراً مزایای «هوای تازه» و کار ارائه میکردند. اما حتی تحت بهترین شرایط، ۵۰٪ از افرادی که وارد آنجا میشدند ظرف پنج سال فوت میکردند (“ca. ” ۱۹۱۶)[۱۰۵]
نرخ سل در اروپا، در اوایل قرن ۱۷ شروع به افزایش کرد. سل در اروپا در قرن ۱۸ به اوج خود رسید، زمانی که عامل نزدیک به ۲۵٪ از تمام مرگ و میرها بود.[۱۱۰] مرگ و میر پس از آن در دهه ۵۰ قرن بیستم نزدیک به ۹۰٪ کاهش یافت.[۱۱۱] بهبود سلامت عمومی به طور قابل توجهی میزان سل را حتی قبل از استفاده از استرپتومایسین و آنتی بیوتیکهای دیگر کاهش داد. با این حال، این بیماری یک تهدید قابل توجه برای بهداشت عمومی باقیماند. هنگامی که شورای تحقیقات پزشکی در انگلستان در سال ۱۹۱۳ تشکیل شد، تمرکز اولیه آن تحقیقات سل بود.[۱۱۲]
در سال ۱۹۴۶، تولید آنتی بیوتیک استرپتومایسین درمان مؤثر و درمان سل را به یک واقعیت تبدیل کرد. قبل از اینکه این دارو معرفی شود، تنها درمان (به جز آسایشگاهها) مداخله جراحی بود. «روش پنوموتوراکس» ریه آلوده را کلاپس و بیحرکت میکرد تا به آن «استراحت» دهد و امکان درمان ضایعات سلی را فراهم نماید.[۱۱۳] پیدایش MDR-TB، دوباره جراحی را به عنوان گزینهای از استانداردهای قابل قبول مراقبت در درمان عفونت سل معرفی کرد. مداخلات جراحی کنونی شامل حذف پاتولوژیک حفرههای قفسه سینه («تاول») در ریهها برای کاهش تعداد باکتریها و برای افزایش در معرض دارو قرار گرفتن باکتریهای باقیمانده در جریان خون میباشد. این مداخله به طور همزمان بار باکتریایی را کاهش میدهد و باعث افزایش اثربخشی درمان آنتی بیوتیک سیستمیک میشود.[۱۱۴] اگرچه کارشناسان امیدوار بودند سل را به طور کامل حذف کنند (آبله)، پیدایش گونههای مقاوم در برابر دارو در دهه ۸۰ قرن بیستم حذف سل را غیر محتمل تر کرد. تجدید حیات متعاقب سل موجب اعلام یک وضعیت اضطراری برای بهداشت جهانی توسط WHO در سال ۱۹۹۳ شد.[۱۱۵]
جامعه و فرهنگ
سازمان بهداشت جهانی و بنیاد بیل و ملیندا گیتس (Bill and Melinda Gates) در حال ارائه کمکهای مالی به تهیه یک آزمون تشخیصی سریع برای استفاده در کشورهایی با درآمد پایین و متوسط هستند.[۱۱۶][۱۱۷] در سال ۲۰۱۱، بسیاری از مکانهای فقیر هنوز هم تنها به میکروسکوپی خلط دسترسی دارند.[۱۱۸]
در سال ۲۰۱۰، هند بالاترین تعداد کل موارد ابتلا به سل در سراسر جهان را داشت. یکی از دلایل، مدیریت ضعیف این بیماری توسط بخش مراقبتهای بهداشتی خصوصی بود. برنامههایی مانند برنامه کنترل سل ملی اصلاح شده به کاهش میزان سل در میان افرادی که مراقبتهای بهداشتی عمومی دریافت میکنند، کمک میکند.[۱۱۹][۱۲۰]
تحقیقات
واکسن BCG دارای محدودیتهایی است، و تحقیق برای تهیه واکسن سل جدید در حال انجام است.[۱۲۱] چند کاندیدای احتمالی در حال حاضر در فاز I و II کارآزمایی بالینی هستند.[۱۲۱] دو رویکرد اصلی در حال تلاش برای بهبود اثر بخشی واکسن موجود هستند. یک رویکرد شامل اضافه کردن یک واکسن زیرواحد به BCG است. استراتژی دیگر در تلاش برای ایجاد واکسنهای جدید و بهتر است.[۱۲۱] MVA85A نمونهای از یک واکسن زیرواحد است که در حال حاضر در آفریقای جنوبی در دست آزمایش میباشد. MVA85A مبتنی بر یک ویروس آبله گاوی با اصلاح ژنتیک میباشد.[۱۲۲] امید است که واکسنها نقش مهمی را در درمان بیماری نهفته و فعال داشته باشند.[۱۲۳]
برای تشویق کشف بیشتر، محققان و سیاست گذاران، مدلهای جدید اقتصادی توسعه واکسن را ترویج میدهند، از جمله جوایز، مشوقهای مالیاتی، و تعهدات بازار پیشرفته.[۱۲۴][۱۲۵] گروههای متعددی در تحقیقات شرکت دارند، از جمله مشارکت توقف سل،[۱۲۶] ابتکار واکسن سل در آفریقای جنوبی، و بنیاد جهانی واکسن سل Aeras.[۱۲۷] بنیاد جهانی واکسن سل Aeras هدیهای به مبلغ بیش از ۲۸۰ میلیون دلار (آمریکا) را از بنیاد بیل و ملیندا گیتس به منظور توسعه و تجویز یک واکسن بهبود یافته علیه سل برای استفاده در کشورهای دارای سرایت بالای سل دریافت کرد.[۱۲۸][۱۲۹]
در سایر حیوانات
میکوباکتریها بسیاری از حیوانات مختلف را آلوده میکنند، از جمله پرندگان،[۱۳۰]جوندگان،[۱۳۱] و خزندگان.[۱۳۲] زیرگونه «Mycobacterium tuberculosis» به ندرت در حیوانات وحشی دیده میشود.[۱۳۳] تلاش برای ریشه کنی سل گاوی ناشی از «میکوباکتریوم بوویس» از گلههای گاو و گوزن نیوزیلند نسبتاً موفق بوده است.[۱۳۴] تلاشها در بریتانیا کمتر موفق بودهاند.[۱۳۵][۱۳۶]
ادامه مطلب
| سکته مغزی | |
|---|---|

سیتی اسکن قسمتی از مغز که ایسکمیک ناشی از سکته مغزی را نشان میدهد.
|
|
| آیسیدی-۱۰ | I61-I64ner |
| آیسیدی-۹ | 434.91 |
| اُمیم | 601367 |
| دادگان بیماریها | ۲۲۴۷ |
| مدلاین پلاس | 000726 |
| ایمدیسین | neuro/۹ emerg/558 emerg/557 pmr/187 |
| پیشنت پلاس | سکته مغزی |
| سمپ | D020521 |
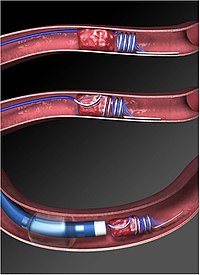
سکته مغزی آسیب عصبی حاد ناشی از اختلال خونرسانی به قسمتی از بافت مغز که ناشی از انسداد رگ مغزی به وسیله یک لخته خونی و یا پارگی یکی از عروق تغذیه کننده آن قسمت بافت مغز میباشد.
به بیان دیگر اگر خونرسانی به قسمتی از مغز دچار اختلال شده و متوقف گردد٬این قسمت از مغز دیگر نمیتواند عملکرد طبیعی خود را داشته باشد. این وضعیت را اصطلاحاً سکته مغزی مینامند. سکته مغزی میتواند به عللی مانند بسته شدن یا پاره شدن یکی از رگهای خون رسان مغز ایجاد شود. به نظر برخی پزشکان و متخصصان، خطر بروز سکته مغزی در زنان به علت بیماری های ژنتیک، موارد هورمونی، مصرف برخی داروها و پیامدهای ناشی از زایمان بیشتر از مردان است.[۱]
معمولاً قبل از بروز سکته مغزی علائم هشدار دهندهای وجود ندارد و یا اینکه علائم بسیار جزئی هستند. بعد از بروز سکته مغزی بیمار باید بلافاصله در بیمارستان بستری گشته تا از بروز صدمات دائمی به مغز جلوگیری شود. عوارضی که بعد از سکته مغزی ایجاد میشود بستگی به محل سکته و وسعت بافتهای گرفتار شدهٔ مغز دارد. عوارض سکته مغزی از عوارض خفیف و گذرا مثل تاری دید تا عوارض فلج کننده دائمی و یا حتی مرگ را شامل میشود.
اگر این علائم در طول ۲۴ ساعت از بین بروند، این وضعیت را اصطلاحاً حمله ایسکمی گذرا (transient ischemic attack)مینامند که یک علامت هشدار دهنده از یک سکته مغزی احتمالی در آینده میباشد. سکته مغزی سومین عامل مرگ و میر در جهان است.[۲]
آمار سکته مغزی در ایران نیز چندان مناسب نیست .پزشکان ایرانی می گویند افراد در ایران 10 سال زودتر از سایر کشورها به سکته مغزی مبتلا می شوند. متخصصان کم تحرکی، مصرف بی رویه نمک و چربی، چاقی، استعمال دخانیات و در مجموع رژیم نامناسب غذایی را عاملی برای حرکت به سمت سکته های مغزی ایرانیان می دانند.[۳] بر اساس آمار میدانی سکته های مغزی در مردان ایرانی 25 درصد بیشتر از زنان است.[۴] دبیر انجمن سکته مغزی ایران اعتقاد دارد که این سکته به عنوان دومین عامل مرگ و میر در ایران و برخی از کشورهای در حال پیشرفت است.[۵]
پژوهش ها نشان می دهند گرچه اشراف بر زبان دوم احتمالا بی ارتباط با سلامت فیزیکی به نظر می رسد، اما ظاهرا این مهارت از مغز در برابر آسیب های ویرانگر به عملکردهای مغزی محافظت می کند و افرادی که در سخن گفتن به دو زبان مهارت دارند، احتمال بهبودی و درمان آنها در صورت بروز سکته مغزی، دو برابر دیگران است.[۶]
محتویات
انواع سکته مغزی
حدود نیمی از تمام موارد سکتههای مغزی بر اثر بسته شدن یک شریان مغزی با یک لخته خون که به آن اصطلاحاً ترومبوز مغزی گفته میشود ایجاد میگردد. دیگر عوامل عمده سکته مغزی را آمبولی مغزی و خونریزی مغزی تشکیل میدهند.
آمبولی مغزی وقتی رخ میدهد که تکهای از یک لخته خون که در جای دیگر بدن مثل قلب یا رگ اصلی گردن ساخته شده، خود را از طریق جریان خون به یکی از شریانهای خونرسان مغز برساند و در آنجا گیر کند. حدود یک چهارم از سکتههای مغزی بر اثر آمبولی مغزی بروز میکنند. خونریزی مغزی باعث حدود ۲۰٪ سکتههای مغزی میباشد بر اثر پاره شدن یکی از شریانهای مغز ایجاد میشود. در این موارد خون بر روی بافتهای اطراف آن ریخته میشود.
لختههای خونی که باعث ترومبوز و آمبولی مغزی میشوند احتمال زیادی دارند که در یک شریانی که بر اثر آترواسکلروسیس آسیب دیدهاست ساخته شده باشند. تصلب شراین وضعیتی است که در آن دیواره رگها بر اثر رسوب چربی سفت میشود. عواملی که باعث افزایش احتمال ایجاد تصلب شراین میشود عبارتند از سیگار کشیدن، مصرف زیاد چربی در رژیم غذایی، دیابت و وجود مقدار زیادی چربی در خون.
محققان آلمانی نوعی پروتیین در عروق مغزی را کشف کردند که بر خطر ابتلا به سکته مغزی تاثیر می گذارد. دیواره مویرگ های خونی مغز نسبت به دیگر مویرگ های بدن، تفاوت دارد. سلول های عصبی مغز، به جای آنکه مانند دیگر سلول های بدن، از طریق نشت غیر فعال مواد غذایی از مویرگ ها، تغذیه شوند به طور فعالانه، توسط مولکول هایی که از عروق خونی جابه جا شده اند، تغذیه می کنند.
سد مویرگی خونی در مغز، بسیار مهم است زیرا نقشی محافظتی دارد و در صورتی که این سد دچار اختلال شود، خطر بروز سکته مغزی و دیگر مشکلات مغزی افزایش می یابد. برای رشد و نمو مویرگ های خونی، سلول های ویژه ای به نام پری سیت ها (pericytes) نیاز است که این سلول ها در مغز، پروتیینی ویژه به نام FoxF2 دارند.این پروتیین فقط در پری سیت های مغزی یافت می شود. محققان دانشگاه گوتنبرگ آلمان متوجه شدند که وجود این پروتئین، به کاهش خطر بروز سکته مغزی کمک می کند.[۷]
آمبولی مغزی ممکن است بر اثر اختلال در ریتم ضربان قلب، اختلالات دریچهای قلب و یا سکته قلبی که به تازگی رخ دادهاست، ایجاد شود که تمام این موارد میتوانند باعث ساخته شدن لخته خون در قلب شوند. خطر بروز آمبولی مغزی، ترومبوز مغزی و خونریزی مغزی با بالا رفتن فشار خون افزایش مییابد. در بیماری سلول داسی شکل (سیکل سل) که یک ناهنجاری گلوبولهای قرمز خون میباشد، بخاطر شکل گوبولهای قرمز که به صورت داس درمیآیند و احتمال چسبیدن به هم و گیر کردن در عروق خونی را دارند، خطر ترومبوز مغزی افزایش مییابد. گاهی ترومبوز ممکن است بر اثر تنگ و باریک شدن شریانهای خون رساننده به مغز بخاطر التهاب ایجاد گردد. التهاب شریان ممکن است به علت وجود یک بیماری خود ایمن مثل پلی آر تریت ندوزا ایجاد شود. در این بیماری سیستم ایمنی بدن به بافتهای سالم بدن حمله میکند.
در سکتههای مغزی خونریزی دهنده که ناشی از پاره شدن یک رگ خونی در داخل یا سطح مغز میباشند وقتی که یک رگ خونی پاره میشود، دیگر حس به سلولهای مغزی نمیرسد، به علاوه نشت خون از رگ پاره شده، میتواند به بافت مغزی آسیب جدی وارد نماید.[۸]
علایم سکته مغزی
در بیشتر افراد علایم سکته مغزی به سرعت و در عرض چند ثانیه یا چند دقیقه بعد از وقوع سکته خود را نشان میدهند. علایم هر سکته مغزی بستگی به قسمتی از مغز دارد که دچار گرفتاری شدهاست. این علایم امکان دارد شامل موارد زیر گردد:
۱-ضعف و کرختی صورت وبازوها یا پاها به خصوص در یک طرف بدن (همی پارزی)
۲-فلج صورت. بازو و پاها در همان طرف (همی پلژی)
۳-عدم تعادل و لنگ زدن (آتاکسی)
۴-اختلال در تکلم یا در درک کلام (دیس آرتری)
۵-اشکال در بلع (دیس فاژی)
۶-کرختی و سوزش قسمتهای بدن-اشکال در درک وضعیت و موقعیت (پارستزی)
۷-دو بینی-تاری دید یا از دست دادن بینایی به خصوص در یک چشم
۸-سردرد شدید و ناگهانی
۹-از دست دادن حافظه کوتاه مدت وطولانی مدت-اختلال در قضاوت
۱۰-سرگیجه بدون دلیل و سقوط ناگهانی
۱۱-بیاختیاری ادرار و مدفوع
۱۲-اشکال در پیدا کردن کلمات و فهمیدن آن چیزی که دیگران میگویند.
۱۳-عدم توانایی در انجام حرکات ظریف.
اگر سکته مغزی شدید باشد، قسمتهایی از مغز که کنترل تنفس و فشار خون را بر عهده دارند ممکن است گرفتار شده و یا اینکه ممکن است شخص به اغماء رفته و نتایج مرگباری را به دنبال داشته باشد.
نحوه درمان
درمان اولیه پس از وقوع یک سکته مغزی شامل تحت نظر گرفتن دقیق فرد و انجام اقدامات پرستاری برای محافظت راه تنفسی او میباشد. اگر در سی تی اسکن دیده شد که یک لخته خون در شریان وجود دارد، باید فوراً با استفاده از داروهای ترومبولیتیک اقدام به حل کردن آن نمود. این درمان ممکن است باعث بهبود عواقب سکته مغزی بشود اما در هر موردی نباید آن را بکار برد، زیرا باعث افزایش خطر بروز خونریزی در مغز میشود.
انجام درمان طولانی مدت برای کاهش خطر وقوع سکتههای مغزی بعدی بستگی به این دارد که علت ایجاد این سکته مغزی چه بودهاست. یکی از راههای درمان سکته مغزی ناشی از انسداد عروق، حل کردن لخته مسدود کننده رگ است. این کار با استفاده از دارویی به نام Alteplase یا به اختصار tPA انجام میشود. هر قدر این درمان سریعتر انجام شود نتیجه بهتری دارد و حداکثر ظرف چهار ساعت و نیم از شروع سکته مغزی قابلیت تزریق وجود دارد. هر قدر تزریق از شروع سکته به تاخیر بیفتد احتمال بروز خونریزی مغزی بدنبال این درمان بیشتر میشود. این دارو از طریق ورید بازویی یا داخل شریانی تزریق میشود. اگر زمان فوق از دست برود و علت سکته آمبولی یا ترومبوز عروق مغزی بودهباشد، داروهایی مثل آسپیرین یا وارفارین تجویز میشود تا با رقیق کردن خون از وقوع لختههای خون جلوگیری کند. اگر مشخص شد که یک شریان دچار تنگی شدهاست ممکن است با جراحی بتوان آن را باز نمود. بعد از بروز یک سکته مغزی که علتش خونریزی و پاره شدن یک شریان بودهاست، درمان بر روی زمینهٔ ایجاد کننده آن متمرکز میشود. درمان طولانی مدت آن ممکن است شامل تجویز داروهای ضد فشار خون باشد تا فشار خون را پایین آورده و از احتمال خونریزیهای بعدی جلوگیری کند. اگر سکته مغزی بر اثر التهاب شریان باشد ٬داروی کورتون دار تجویز میشود.
در بیشتر موارد سکتههای مغزی، درمانهای توانبخشی مثل فیزیوتراپی، کاردرمانی و گفتاردرمانی چه در بیمارستان و چه در خانه ضروری میباشد. بدون شک یکی از مهمترین مراحل درمانی بیماران سکته مغزی توانبخشی تحت نظر یک تیم توانبخشی است که اعضائ تیم شامل متخصص طب فیزیکی و توانبخشی، کاردرمانگر فیزیوتراپیست ارتوپدی فنی، شنوایی شناس، گفتار درمان، بیناییشناسی روانشناس، کارشناس تغذیه، پرستار توانبخشی مددکار اجتماعی و خانه ساز (home maker)میباشد. یکی از روشهای جدیدی که در توانبخشی و درمان بیماران سکته مغزی استفاده شدهاست استفاده از تحریک غیر تهاجمی مغز می باشد که شامل دو تکنولوژی تحریک مغناطیسی مغز یا rTMS و تکنولوژی تحریک الکتریکی مغز یا "تی دی سی اس" میباشد در بررسی بازبینی مقالات که توسط انجمن نوروفیزیولوژی بالینی[۹] در سال ۲۰۰۹ انجام شده و در ژورنال نوروفیزیولوژی بالینی[۱۰] به چاپ رسیدهاست به مطالب زیر اشاره شدهاست. در روش تحریک مغناطیسی مغز تحریک سلولهای مغزی برای اصلاح عملکرد سلولهای مغزی از طریق افزایش خاصیت نوروپلاستیسیتی مغز انجام میشود این روش بسیار کم عارضه بوده و توسط پزشکان متخصص طب فیزیکی و توانبخشی و یا مغز و اعصاب انجام میشود. در این روش یا به کمک القای با فرکانس بالا نیمکره صدمه دیده تحریک می شود و یا به کمک القای با فرکانس پایین فعالیت نیمکره سالم کم می شود که در نتیجه آن فعالیت نیمکره صدمه دیده زیاد می شود. این روش در بازگشت عملکرد دست بهبود گفتار کاهش درد و بهبود عملکرد بیماران موثر بودهاست. این روش درمانی اولین با ر در ایران توسط مرکز تخصصی توانبخشی سکته مغزی تبسم و سپس مرکز آموزشی و درمانی فیروزگر وابسته به دانشگاه علوم پزشکی ایران در سال ۱۳۸۶ و سپس در مرکز جامع توانبخشی سکته مغزی دکتر محمودی در شیراز در سال 1387 مورد استفاده برای درمان بیماران سکته مغزی قرار گرفت.
تغییر عادات و نحوه زندگی مثل کم کردن میزان چربی در رژیم غذایی ترک کردن استعمال دخانیات میتوانند باعث کاهش خطر بروز یک سکته مغزی دیگر آینده شوند. پیش بینی عاقبت یک سکته مغزی بسیار دشوار است و بستگی زیادی ه عوامل ایجاد کننده آن دارد. معمولاً یک سوم افراد بعد از سکته مغزی به بهبودی کامل یا نسبتاً کامل دست مییابند. یک سوم دیگر از افراد نیز دچار ناتوانیهایی به صورت دائمی میشوند. اگر مشکلاتی که برای افراد بعد از سکته مغزی ایجاد شد در طول ۶ ماه بهبود نیابد احتمالاً این مشکلات دائمی خواهند بود. حدود ۲۰٪ از افرادی که دچار سکته مغزی میشوند در عرض یک ماه فوت میکنند.
تشخیص زودهنگام این عارضه می تواند کمک چشمگیری به جلوگیری از آن یا کاهش آسیب های سکته مغزی داشته باشد. بتازگی محققان دانشگاه کورنل آمریکا با استفاده از یک روش جدید، زمان تشخیص را به 10 دقیقه کاهش داده اند. در این روش، محققان یک آنزیم را به نانوذرات متصل کرده و وارد جریان خون می کنند. زمانی که آنزیم وارد جریان خون می شود، روشن شده و محققان با استفاده از آن می توانند نشانگر زیستی ایجاد شده بر اثر آسیب های مغزی را مشاهده کنند.[۱۱]
ادامه مطلب
| سکته قلبی | |
|---|---|

انفارکتوس آپیکال(۲) بعلت گرفتگی کرونر در نقطه(۱)
|
|
| آیسیدی-۱۰ | I21-I22 |
| آیسیدی-۹ | 410 |
| دادگان بیماریها | 8664 |
| مدلاین پلاس | 000195 |
| ایمدیسین | med/1567 emerg/327 ped/2520 |
| پیشنت پلاس | سکته قلبی |
| سمپ | D009203 |
سکته قلبی (در اصطلاح پزشکی امآی) و یا انفارکتوس میوکارد (به انگلیسی: Myocardial infarction) یا حمله قلبی٬ عبارت از انهدام و مرگ سلولی دائم و غیرقابل برگشت در بخشی از عضله قلب (میوکارد) است که به علت ازبینرفتن جریان خون و وقوع یک ایسکمی شدید در آن قسمت از قلب رویمیدهد. این توقف گردش خون ممکن است ناگهانی و بدون هیچ علائم قبلی نمایان گردد یا پس از چند حمله آنژینی (درد قفسه سینه) نمود یابد. عمدهترین دلیل سکته بستهشدن رگهای تغذیهکننده قلب است. برای رفع انسداد غیر از دارو، از بالن و جراحی قلب باز (تعویض رگ مسدود شده) استفاده میشود. سکته قلبی نوعی عارضۀ فراگیر است که هرساله باعث درگذشتن هزاران تن میگردد.[۱]
در میان عوامل مساعدکننده دیابت، فشارخون بالا، کلسترول خون بالا افراط در استعمال دخانیات و الکل، عدم فعالیت بدنی، فشار عصبی، سابقۀ فامیلی و سن قابل ذکراند.
بهطور یقین این بیماری خیلی وخیم است و سالیانه تنها در آمریکا، در سال ۲۰۰۴ میلادی، بیش از ۱۵۰۰۰۰ نفر از این عارضه جانباختند.
محتویات
سببشناسی
اغلب آترواسکلروز عروق کرونری و درنتیجه انسداد عروق تغذیهکننده ماهیچه قلب، منجر به انفارکتوس میوکارد میشود که درمان، آسان نخواهدبود.اگر شریان بستهشده شریان کرونر اصلی باشد احتمال مرگ انسان وجوددارد.
عوامل متعدد مساعدکنندهای مانند دیابت (بیماری قند خون)، فشار خون بالا، سیگار، زیادی کلسترول خون و غیره وجوددارد که عامل تصلب شرائین است.
علائم
در اکثر موارد انفارکتوس میوکارد همراه با تظاهرات معمولی و تیپیک است که تشخیص را آسان میسازد. یک درد موضعی قفسه سینه که در مرکز قفسه صدری(سینه) با قابلیت انتشار بهطرف آرواره، بازوها، پشت و گردن، سمپتوم ویژه در امآی است و بیشتر از ۲۰ دقیقه طولمیکشد.[۲] اگر درمان نشود این درد آزاردهنده و بحرانی است و مدتها بهطولمیانجامد.
گاهی چندین ساعت با مصرف ترینیترین مقاومت میکند، داروی دوپواترین درد آنژین را آرام میکند. همچنین علائم دیگری که آشکارکننده هستند عبارتند از الکتروکاردیوگرام اورژانس و فوری میتواند تشخیص را آسان سازد. در تعداد زیادی از موارد انواع انفارکتوس وجود دارد که بهصورت تشویش و اضطراب تظاهر میکند.
مثلاً اشکال هاضمهای و احساس کاذب آروغزدن، عصبی بودن، تنگی نفس (به علت اشکال در بطن چپ و درنتیجه ادم ریوی)٬ ادم و تورم در دست و پا که گاهی بدون تشخیص است و تنها اتفاقی در آزمایش قلبی و آزمایش روتین و منظم پزشکی با تشخیص آن برخورد میشود.
باید بخاطر داشت که هنگام مراجعه یک بیمار مسن با فشار خون بالا، سن بیش از ۴۰ سال، زندگی مشوش و پراضطراب که دچار درد شدید وناگهانی و ممتد قفسه سینه، بفکر انفارکتوس بود و الکتروکاردیوگرام درخواست نمود .
تشخیص
شناسایی یک بیمار از نظر رویداد واقعه سکته قلبی حاد می تواند ساده، دشوار و یا در حد وسط این دو حالت باشد. معمولاً تشخیص ساده سکته قلبی حاد در افرادی است که تعدادی از عوامل خطر آترواسکلروز را به همراه علائم و نشانه هایی دال بر فقدان جریان خون به قلب را دارند. معمولاً بیماران مشکوک به رویداد سکته قلبی را به اورژانس انتقال می دهند. زمانی که تصویر بالینی بیمار دال بر بروز سکته قلبی باشد بلافاصله چندین آزمایش تشخیصی به مرحله اجرا در خواهد آمد این ازمون ها شامل: نوار قلب، آزمایش خون، و اکوکاردیوگرافی است.
الکتروکاردیوگرام: نخستین تست تشخیصی الکتروکاردیوگرام است که ممکن است نشان دهد سکته قلبی در حال روی دادن است و یا اینکه قبلاً روی داده است.
تست های آزمایشگاهی: سلولهای زنده حاوی آنزیم ها و پروتئین هایی (همانند کراتین کیناز،تروپونین و میوگلوبین) هستند که در ارتباط با عملکرد تخصصی آنها می باشند. هنگاهی که یک سلول قلبی می میرد، غشاء شلولی یکپارچکی خود را از دست می دهد و در این شرایط آنزیم ها و پروتئین ها آرام آرام به جریان خون راه می یابند. این آنزیم ها و پروتئین ها را می توان با روش های آزمایشگاهی شناسایی نمود.
تصویر برداری(اکو): در اکو کاردیوگرام به مقایسه بطن چپ از نظر وضعیت انقباض نرمال یا غیر نرمال پرداخته می شود. یکی از اولین اقدامات حفاظتی سلولهای میوکارد در هنگام کاهش جریان خون، خاموش نمودن مکانیسم نیاز به انرژی برای انقباض است. این مکانیسم بلافاصله پس از کاهش جریان خون شروع می شود. اکوکاردیوگرام می تواند در شناسایی نقاطی از قلب که تحت تاثیر سکته قلبی بوده اند و تشخیص عروقی که به احتمال زیاد مسدود شده اند مفید واقع شود.[۳]
درمان
اولین قدم استراحت کامل، تجویز اکسیژن و کنترل فشار خون و ریتم قلبی است. معمولاً داروهای ضدانعقاد مانند آسپرین یا هپارین و بلوککنندههای گیرندۀ بتای سمپاتیک مانند پروپرانولول تجویز می شود. روشهای بازکردن رگ مسدودشده در بیمارستان عبارتنداز داروهایی مانند استرپتوکیناز و اوروکیناز، بالن و جراحی اورژانس عروق کرونر.
پیوند به بیرون
|
|
در ویکیانبار پروندههایی دربارهٔ سکته قلبی موجود است. |
- سکته قلبی چیست؟ (انگلیسی)
- فیلم ویدئویی حمله قلبی http://familydoctor.ir/fa/page/484
پیشگیری
با تغییر سبک زندگی به یک سبک سالم میشود از خطر بیماریهای قلبی پیشگیری نمود.[۴] عوامل اساسی یک سبک زندگی سالم شامل:
- سیگار نکشیدن و یا ترک سیگار[۴]
- رژیم غذایی مناسب (سبزی و میوه زیاد و چربی، قند و گوشت کم)
- حداقل 30 دقیقه ورزش در روز[۴]
- کنترل بیماری هایی از قبیل دیابت، فشارخون بالا و کلسترول
- دوری از محیط پر استرس
- خوابیدن به مدت نیم ساعت یا کمی بیشتر در میانه روز می تواند فشار خون را پایین آورده در نتیجه سبب کاهش خطر حمله قلبی تا 10 درصد شود.[۵]
- پژوهشگران اعتقاد دارند که واکسن آنفلوآنزا در برابر حمله قلبی و سکته مغزی نقش محافظتی دارد و برای بیماران قلبی توصیه شده است.
ادامه مطلب
| سقط خودبهخودی | |
|---|---|
| آیسیدی-۱۰ | O03 |
| آیسیدی-۹ | 634 |
| مدلاین پلاس | 001488 |
| ایمدیسین | topic list |
| پیشنت پلاس | سقط خودبهخودی |
| سمپ | D000022 |
سقط خودبهخودی (به انگلیسی: Miscarriage، spontaneous abortion) به از دست رفتن طبیعی محصول لقاح طی سه ماههٔ اول بارداری گویند. در گذشته از دست رفتن محصول لقاح پیش از هفتهٔ ۲۰ را نیز سقط میخوانند، اما با پیشرفت سونوگرافی تشخیصی امروزه کمتر از این محدودهٔ زمانی استفاده میشود.[۱]
گاه سقط بطور عمدی و ناشی از مصرف دارو یا دستکاری است که به آن سقط خودبخودی Miscarriage نمیگویند. واژه سقط جنین (Abortion) واژه ای کلی تری است و برای تمام انواع سقط اطلاق میشود.
محتویات
علل
علل ایجاد سقط به ۲ دستهٔ علل مربوط به رویان وعلل مربوط به والدین تقسیم میشود
- علل رویانی: غیر طبیعی بودن سلولهای زایشی، اختلالات کروموزومی، جایگزینی نامناسب محصول لقاح، اختلال در نمو جفت یا رویان
در مجموع در ۶۰٪ سقطهای خودبخود سه ماههٔ اول اختلال کروموزومی مانند (تریزومیها ی اتوزومی ۱۶٬۲۱٬۲۲، مونوزومی ۴۵x، تریپلوئیدی، تتراپلوئیدی، ترانس لوکاسیون، موزائیسم) وجود دارد
- علل مربوط به والدین: عفونت، سیگار کشیدن، مصرف قهوه اتانول، داروها
انواع سقط
تهدید به سقط
هر نوع ترشح خونی مهبلی یا خونریزی رحمی در نیمه اول حاملگی را به عنوان تهدید به سقط محسوب میکنند. (Threatened miscarriage)
خونریزی ناشی از تهدید به سقط معمولاً اندک است و ممکن است طی چند روز تکرار شود. تهدید به سقط معمولاً با کرامپ رحمی یا دردپشت آغاز میشود. در معاینه سرویکس بستهاست و فاقد افاسمان میباشد و بافت دفعی دیده نمیشود.
با روشهای سونوگرافی پیشرفته، جنین زنده در هفته ۵٫۵ بارداری قابل تشخیص است. یافتههای سونوگرافی تا هفتههای ۳ تا ۴ حاملگی غیرقابل اطمینان هستند. در صورت هرگونه شکی بیمار با B-hcG یا سونوگرافی مکرر پیگیری میشود. از هفته ۵ تا ۶ با کمک سونوگرافی واژینال، کیسه زرده و ساک حاملگی قابل تشخیص است و رویان و حرکات قلب وی بلافاصله بعد از آن دیده میشود. از علایم سونوگرافیک پیش روی بودن سقط میتوان: غیرطبیعی بودن ساک حاملگی و اندازه کیسه زرده، رویان کوچکتر از سن تخمینی و سرعت ضربان قلب آهسته رویان را نام برد.
درمان
زنان در معرض تهدید به سقط با جنین زنده باید دسترسی نزدیک به خدمات پزشکی داشته باشند. تا زمان خفیف بودن خونریزی و کرامپ، بسته بودن سرویکس و طبیعی بودن افزایش سطح B-hcG و مشاهده یک جنین طبیعی در سونوگرافی بیمار باید تحت نظارت مداوم باشد. موارد زیر نشان دهنده پیش آگهی نامطلوب هستند:
- سطح B-hcG منفی یا در حال کاهش
- کاهش اندازه رویان یا جنین در سونوگرافی.
- کاهش ضربان قلب رویان یا جنین
- عدم افزایش اندازه رحم در معاینه لگن خاصره
اگر بر اساس ارزیابی بالینی محصول حاملگی قابل زنده ماندن نباشد، راههای انتخابی شامل درمان انتظاری یا تخلیه رحم است. در صورت مشاهده بافت داخل رحمی اندک در سونوگرافی، میتوان منتظر دفع خودبخودی محصولات حاملگی ماند. برای کاهش عوارض در زنانی که بافت زیادی در داخل رحم دارند از کورتاژ الکتیو رحم استفاده میکنیم.
سقط اجتناب ناپذیر
در صورتی که خونریزی و کرامپ با پارگی آشکار پردهها یا اتساع سرویکس همراه باشد. ممکن است خونریزی شدید باشدو به ناپایداری همودینامیک بینجامد.
تشخیص
با معاینه دقیق واژینال تشخیص داده میشود، هر چند اغلب سونوگرافی انجام میشود
درمان
برای پیشگیری از خونریزی یا عفونت مادر باید رحم تخلیه شود اگر بیمار از نظر بالینی وضعیتی پایدار داشته باشند میتوان درمان سرپایی انجام داد.
سقط فراموش شده
در سقط فراموش شده علیرغم سپری شدن مدت طولانی از مرگ جنین محصولات حاملگی دفع نمیشود. معمولاً علایم حاملگی بتدریج محو میشود وتست حاملگی منفی میشود.
تشخیص
با کمک سونوگرافی میتوان صدای قلب جنین را شنید.
درمان
سرانجام در بیشتر بیماران سقط خودبخود صورت میگیرد اما درمان انتظاری از نظر روانی برای بیمار مشکل ساز است از این رو تخلیه رحم به روش کورتاژ یا تحریک زایمان با میزوپروستول انجام میگیرد.[۲]
جستارهای وابسته
ادامه مطلب