| هموفیلی | |
|---|---|
| آیسیدی-۱۰ | D66-D68 |
| آیسیدی-۹ | 286 |
| اُمیم | 306700 306900 264900 |
| دادگان بیماریها | ۵۵۵۵ 5561 29376 |
| مدلاین پلاس | 000537 |
| ایمدیسین | med/۳۵۲۸ |
| سمپ | D025861 |
هِموفیلی یا خونتَراوی دستهای از بیماریهای ارثی هستند که در آنها توان بدن برای ایجاد لخته و انعقاد خون برای جلوگیری از خونریزی در صورت پاره شدن رگ مختل شده است. هموفیلی آ (نقص فاکتور انعقادی هشت) شایعترین شکل این اختلال است و در یک نوزاد از هر ۵ تا ۱۰ هزار نوزاد پسر دیده میشود. هموفیلی بی (نقص فاکتور نه) در یک مورد از هر ۲۰ تا ۳۴ هزار نوزاد پسر مشاهده میشود.
این بیماری که تقریباً به طور انحصاری در افراد مذکر بوجود میآید، در ۸۵٪ موارد ناشی از کمبود فاکتور VIIIاست که به آن هموفیلی نوعA یا هموفیلی کلاسیک میگویند.[۱]
محتویات
انواع هموفیلی
هموفیلی A و B اختلالات انعقادی وابسته به کروموزوم جنسی هستند که به ترتیب بر اثر جهشهایی در ژنهای F۸C و F۹ ایجاد میشوند. جهشهای F۸C موجب کمبود یا اختلال عملکرد عامل انعقادی ۸ (فاکتور هشت)و جهشهای ژن F۹ باعث کمبود یا اختلال عملکرد عامل انعقادی ۱۱ میشوند. هموفیلی نوعی اختلال در تمام نژادها و بدون ترجیح نژادی است. میزان شیوع هموفیلی A از هموفیلی B بیشتر است. هموفیلی نوع C یک نوع اختلال ژنتیکی اتوزومال است که به علت کمبود فاکتور یازده خونی میباشد.
شرح بیماری
این بیماری از طریق مادر به پسرانش منتقل شده و مردان نمیتوانند بیماری را به پسرانشان منتقل کنند. هموفیلی در ۸۵ درصد موارد ناشی از کمبود فاکتور انعقاد خون شماره ۸ است و این نوع هموفیلی موسوم به هموفیلی A یا هموفیلی کلاسیک است. در ۱۵ درصد دیگر بیماران هموفیلیک، تمایل به خونریزی بر اثر کمبود فاکتور انعقادی ۱۱ بوجود میآید. هر دوی این فاکتورها بطور ژنتیکی از طریق کروموزوم X به صورت یک خاصیت مغلوب انتقال مییابند.
اگر یک مرد هموفیلی با یک زن ناقل هموفیلی( یکی از کروموزومهای جنسی زن معیوب باشد)ازدواج کند در آن صورت نصف زادههای آنان پسر سالم ودختر ناقل و نصف زادههای آنان پسر و دختر هموفیل خواهد بوددختران هموفیل معمولا در اولین قاعدگی در اثر خونریزی از بین میروند.
این بیماران معمولاً با التهاب مفاصل روبرو هستند به همین دلیل در هنگام بروز درد و التهاب از راه رفتن عاجز میشوند.
بسیاری از بیماران پس از مدتی به دلایلی مانند تولید آنتیبادیهای خنثی کننده قادر به ادامهٔ مصرف فاکتور هشت انسانی نیستند و باید از نوع حیوانی آن استفاده کنند یا اینکه از فاکتور هفت نوترکیب انسانی استفاده کنند.
علایم شایع
علایم اولیه هموفیلی خونریزیهای طولانی پس از خراشهای کوچک است. البته عقیده عمومی بر این است که اینگونه خونریزیهای کوچک ولی طولانی باعث مرگ شخص مبتلا نمیشود ولی به تدریج بیماری پیشرفت نموده علایم شدیدتری از قبیل خونریزیهای دردناک داخل مفصلی مانند مفصل زانو ایجاد خواهد کرد.
اینگونه حوادث با کوچکترین تحریکی پیش میآید و احتمالاً یک پسر بچه را از انجام بازی محبوبش یعنی فوتبال و یا انجام هر کار کوچک دیگری که احتمال دارد زانو دچار پیچیدگی شود باز میدارد. تجمع خون در مفاصل ممکن است باعث خشک شدن مفصل شده و کودک را بطور کامل فلج کند و یا خونریزیهای غیر منتظرهای در ماهیچهها به وقوع بپیوندد.
فنوتیپ و سیر طبیعی
هموفیلی معمولاً بیماری مردان است هر چند ندرتاً خانمها هم به علت انحراف غیر فعال شدن کروموزوم ایکس از حالت طبیعی مبتلا میشوند. از نظر بالینی این دو نوع هموفیلی غیرقابل افتراق هستند. هر دوی اینها با خونریزی به داخل بافتهای نرم، ماهیچهها و مفاصل متحمل وزن مشخص میشوند. خونریزی ظرف چند ساعت تا چند روز پس از تروما رخ میدهد و اغلب تا چند روز یا چند هفته ادامه مییابد.
آنهایی که بیماری شدیدی دارند معمولاً در دوره نوزادی به علت هماتوم شدید سر یا خونریزی طولانی از زخمهای ناف یا محل ختنه تشخیص داده میشوند. افراد دچار بیماری متوسط اغلب تا زمانی که شروع به خزیدن یا راه رفتن نکنند دچار هماتوم نمیشوند و لذا تا آن زمان بیماری آنها تشخیص داده نمیشود.
درمان
اگر چه کار آزماییهای فعلی ژن درمانی بسیار امیدوار کننده به نظر میرسند، هیچ درمانی علاج دهندهای بجز پیوند کبد برای هموفیلی A و B وجود ندارد. هر گاه شخص مبتلا به هموفیلی دچار خونریزی شدید و طولانی شود تقریباً تنها درمانی که واقعاً موثر است تزریق فاکتور انعقادی شماره ۸ خالص است. قیمت این فاکتور بسیار گران بوده و زیاد نیز در دسترس نیست زیرا این فاکتور فقط میتواند از خون انسان و آنهم فقط به مقادیر فوقالعاده اندک بدست آورد. فاکتور ۸ به روش مهندسی ژنتیک نیز تهیه شده و بنام ادویت (Advate) و برای مصرف انسانی در دسترس بیماران قرارگرفته است. بسیاری از بیماران پس از مدتی بدلایلی مانند تولید آنتی بادیهای خنثی کننده قادر به ادامه مصرف فاکتور هشت انسانی نیستند و باید از نوع حیوانی آن استفاده کنند یا اینکه از فاکتور هفت نوترکیب انسانی استفاده کنند که هم اکنون یک شرکت دانمارکی با نام تجاری نوووسون (Novoseven) آنرا تولید میکند. به دلیل گرانی فوقالعاده زیاد بسیاری از کشورها و افراد قادر به تهیه این داروهای نوترکیب نیستند. نوع بیوژنریک یا بیوسیمیلار این دارو توسط شرکت آریوژن تولید شده و بنام آریوسون در اختیار بیماران هموفیلی قرارگرفته است.[نیازمند منبع]
خطر توارث
اگر خانمی سابقه خانوادگی هموفیلی داشته باشد با تجزیه و تحلیل پیوستگی یا شناسایی دو ژن جهش یافته F۸C و F۹ تجمع یافته در خانواده میتوان وضعیت حامل بودن او را تعیین کرد. تشخیص افراد حامل با سنجش آنزیمی دشوار میباشد و همه جا مقدور نیست. اگر مادری حامل باشد هر یک از پسرانش به احتمال ۵۰ درصد ژنهای جهش یافته را به ارث خواهند برد. اگر مادری دارای پسری مبتلا به هموفیلی باشد اما هیچ خویشاوند مبتلای دیگری نداشته باشد احتمال حامل بودن او ۲ در ۳ است.
تخریب مفصلی در هموفیلی
بیشتر خونریزیهای داخلی در این بیماری در مفاصلی چون زانو، آرنج، مچ دست، مچ پا، شانه، لگن و دیده میشود؛ که بیشتر در افراد نوع شدید اتفاق میافتد. خونریزی داخلی باعث تجمع خون در داخل بافت ومفصل شده و مفصل متورم و دردناک می شودو از کار میافتد. بعد از قطع خونریزی باید تحت نظر فیزیوراپ آشنا به هموفیلی و با انجام حرکات سبک فیزیوتراپی به جذب و خارج شدن تدریجی خون از مفاصل کمک نمود. چون تجمع خون در مفصل برای طولانی مدت باعث تخریب مفصل میشود و صدمات جدی به آن وارد میکند؛ و هم استعداد خونریزی خودبخودی و مجدد را بالا میبرد.
یک درمان امیدوار کننده برای کاهش درد و خونریزی مفاصل درگیر و دائما در حال خونریزی تزریق درون مفصلی رادیو دارو بصورت فسفر یا رنیوم میباشد. با تشخیص پزشک متخصص ارتوپد و هماهنگی پزشک هسته ای انجام این تزریق درد دائم و خونریزی و محدودیت حرکتی را تا حدود بسیار زیادی از بین می برد. سينوويورتز با فسفر راديواكتيو، مي تواند روشي موثر و به صرفه در كاهش همارتروز و مصرف فاكتور در بيماران مبتلا به آرتروپاتي هموفيليك باشد.[۲]
منابع و پانویس
پیوند به بیرون
ادامه مطلب
| هپاتیت دی | |
|---|---|
| طبقهبندی ویروسها | |
| Group: | گروه ۵ ((-)ssRNA) |
| راسته: | Unassigned |
| تیره: | Unassigned |
| سرده: | هپاتیت دی |
| گونه: | Hepatitis delta virus |
| هپاتیت دی | |
|---|---|
| آیسیدی-۱۰ | B17.0, B18.0 |
| آیسیدی-۹ | 070.31 |
| سمپ | D003699 |
تقریباً ۱۵ میلیون نفر در دنیا آلوده به ویروس هپاتیت D هستند. هپاتیت D همیشه همراه با هپاتیت ب دیده میشود.
محتویات
ویروس شناسی
ویروس هپاتیت D برای همانند سازی خود از ویروس هپاتیت B و امکانات سلول میزبان استفاده می کند. این ویروس ناقص است و از نظر اندازه و ساختمان ژنوم نیاز به کمک برای همانندسازی مانند ویروئیدهای گیاهی است. ژنوم این ویروس فقط یک پروئتین کپسیدی را کد می نماید. ویروس دارای ژنوم RNA منفی، تک رشته ای، حلقوی و کوچک است. ویروس دارای پوشش است و احتمالاً دارای ۳ فرم است. همانند هپاتیت B به سلولهای کبد متصل شده و وارد آن می شود. نسخه برداری و همانندسازی ویروس غیر متعارف است.
بیماریزایی
این ویروس مانند هپاتیت B از طریق مایعات بدن انتشار می یابد. هر دو ویروس با یک روش مشترک به سلول میزبان متصل می شوند. یک فرد ممکن است به عفونت توام هپاتیت B و D مبتلا گردد. همانندسازی ویروس همراه با صدمه زدن به سلول میزبان ( سلول کبد ) است. صدمات حاصله از ویروس هپاتیت D به سلول کبد بر خلاف ویروس هپاتیت B منحصر به پاسخ ایمنی سلول میزبان نیست. احتمالاً عفونت مزمن هپاتیت D در افراد مبتلا به هپاتیت مزمن B نیز بروز می کند.
هپاتیت D در کودکان و افراد بالغ مبتلا به هپاتیت B ایجاد می شود. ویروس انتشار جهانی داشته و آندمیک جنوب ایتالیا، خاورمیانه، قسمتهایی از آفریقا و آمریکا لاتین می باشد. اساس تشخیص آزمایشگاهی بر مبنای افزایش آنزیمهای کبدی است. بررسی آنتی ژن و ژنوم در خون نیز مفید است. تاکنون درمان اختصاصی برای هپاتیت D پیشنهاد نشده است، اما چون همانند سازی ویروس به وجود هپاتیت B وابسته است لذا پیشگیری از هپاتیت B در پیشگیری از این ویروس موثر خواهد بود. با واکسیناسیون هپاتیت B, حذف محصولات خونی آلوده، عدم مصرف از مواد مخدر تزریقی و کنترل ناقلین ویروس از انتشار هپاتیت D جلوگیر خواهد کرد.
جستارهای وابسته
منابع
ادامه مطلب
| هپاتیت سی | |
|---|---|
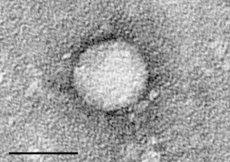
تصویر گرفته شده ویروس هپاتیت سی توسط میکروسکوپ الکترونی
|
|
| آیسیدی-۱۰ | B17.1, B18.2 |
| آیسیدی-۹ | 070.70,070.4, 070.5 |
| اُمیم | 609532 |
| دادگان بیماریها | ۵۷۸۳ |
| مدلاین پلاس | 000284 |
| ایمدیسین | med/993 ped/979 |
| پیشنت پلاس | هپاتیت سی |
| سمپ | D006526 |
هپاتیت سی (به انگلیسی: Hepatitis C) نوعی عفونت است که عمدتاً کبد را تحت تأثیر قرار میدهد. ویروس هپاتیت سی (HCV)علت این بیماری است.[۱]هپاتیت سی اغلب هیچ علائمی ندارد، اما عفونت مزمن موجب زخم شدن کبد میشود، و پس از چند سال به سیروز کبد میانجامد. در بعضی موارد، افراد مبتلا به سیروز کبد همچنین دارای نارسایی کبد، سرطان کبد، و یا عروق بسیار متورم مری و معده میباشند که این مورد آخر میتواند منجر به خونریزی تا حد مرگ شود. .[۱]
افراد اغلب از طریق تماس خونی ناشی از استعمال درون وریدی مواد مخدر، تجهیزات پزشکی ضد عفونی نشده، و تزریق خون به هپاتیت سی مبتلا میشوند. به صورت تخمینی ۱۳۰ تا ۱۷۰ میلیون نفر در سراسر جهان به هپاتیت سی مبتلا هستند. دانشمندان در دهه ۱۹۷۰ تحقیقات در مورد HCVرا آغاز کردند و در ۱۹۸۹ وجود این بیماری را تأیید نمودند.[۲] این ویروس به عنوان عامل بیماری در سایر حیوانات شناخته نشده است.
اینترفرون و ریباویرین داروهای استاندارد برای HCV هستند. بین ۵۰٪ تا ۸۰٪ افرادی که با این داروها تحت معالجه قرار میگیرند، درمان میشوند. کسانی که به سیروز یا سرطان کبد دچار میشوند، ممکن است به پیوند کبد نیاز پیدا کنند، ولی ویروس اغلب پس از پیوند مجدداً عود میکند.[۳] هیچ واکسنی برای هپاتیت سی وجود ندارد.
محتویات
علایم و نشانه ها
هپاتیت سی تنها در ۱۵٪ موارد به علایم حاد منجر میشود.[۴] علایم اغلب ملایم و نامشخص هستند، از جمله کاهش اشتها، خستگی، تهوع، دردهای مفصلی یا عضلانی، و کاهش وزن.[۵]تنها موارد کمی از عفونت حاد با زردی همراه است.[۶] عفونت در ۱۰-۵۰٪ افراد و بیش از سایرین در بانوان جوان، بدون درمان بهبود مییابد.[۶]
عفونت مزمن
هشتاد درصد افرادی که در معرض این ویروس قرار میگیرند، به عفونت مزمن دچار میشوند.[۷]اکثر افراد در دهههای نخستین عفونت، کمترین و یا هیچ علائمی را تجربه نمیکنند،[۸] اگرچه هپاتیت سی مزمن میتواند با خستگی همراه باشد. .[۹] هپاتیت سی در میان افرادی که برای چندین سال به این بیماری مبتلا بودهاند، علت اصلی سیروز کبد و سرطان کبد است.[۳] بین ۱۰-۳۰٪ از افرادی که بیش از ۳۰ سال مبتلا بودهاند، به سیروز کبد دچار میشوند.[۳][۵]سیروز کبد در افرادی که همچنین به هپاتیت بی یا HIV مبتلا بودهاند، معتادان الکلی و مردان شایع تر است. [۵] افرادی که به سیروز کبد مبتلا میشوند، با خطری ۲۰ برابر بیشتر در ابتلا به سرطان کبد مواجه هستند؛ با میزان ۱-۳٪ در سال.[۳][۵] در معتادان به الکل، خطر ابتلا ۱۰۰ برابر بیشتر است.[۱۰] هپاتیت سی علت ۲۷٪ از موارد سیروز کبد و ۲۵٪ از موارد سرطان کبد است.[۱۱]
سیروز کبد میتواند منجر به فشار خون بالا در رگهای متصل به کبد، تجمع مایعات در شکم، خونریزی یا کبودی به سادگی، رگهای بزرگ شده، به خصوص در مری و معده، زردی (زرد شدن پوست)، و آسیب مغزی گردد.[۱۲]
اثرات خارج از کبد
هپاتیت سی همچنین در موارد نادر با سندروم شوگرن (نوعی اختلال در سیستم دفاعی بدن)، تعداد کم تر از حد طبیعی پلاکتهای خون، بیماری مزمن پوستی، دیابت، و لنفومای غیر هوچکینی همراه است.[۱۳][۱۴]
علت
ویروس هپاتیت سی یک ویروس RNA کوچک پوشینه دار تک زنجیرهای مثبت است.[۳] این ویروس عضو جنس "هپاسی ویروس" در خانواده ‘‘فلاوی ویریده’’ است.[۹] HVC ۷ ژنوتایپ اصلی دارد.[۱۵] در ایالات متحده آمریکا، ژنوتایپ ۱ در ۷۰٪ موارد عامل بیماری است، و هر یک از دیگر ژنوتایپها ۱٪ موارد را ناشی میشوند.[۵] در آمریکا و اروپا نیز ژنوتایپ ۱ شایع ترین نوع است.[۳]
سرایت
راه اصلی سرایت بیماری در کشورهای توسعه یافته استعمال درون وریدی مواد مخدر (IDU)است. در کشورهای در حال توسعه، راههای اصلی عبارتند از تزریق خون و شیوههای پزشکی غیر ایمن[۱۶] علت سرایت در ۲۵٪ موارد نامعلوم باقی میماند. ;[۱۷] ولی تعداد زیادی از این موارد احتمالاً به علت استعمال درون وریدی مواد مخدر هستند.[۶]
استعمال درون وریدی مواد مخدر
استعمال درون وریدی مواد مخدر (IDU)یک عامل مهم ریسک برای هپاتیت سی در بسیاری از قسمتهای جهان است. .[۱۸] یک بررسی از ۷۷ کشور نشان میدهد که در ۲۵ کشور میزان هپاتیت سی در جمعیت مصرف کننده مواد مخدر بین ۶۰٪ تا ۸۰٪ است؛ از جمله آمریکا[۷] و چین.[۱۸] دوازده کشور دارای میزانی بیش از ۸۰٪ هستند.[۷] در میان مصرف کنندگان مواد مخدر ده میلیون نفر به هپاتیت سی مبتلا هستند؛ چین (۱٫۶ میلیون)، ایالات متحده (۱٫۵ میلیون)، و روسیه (۱٫۳ میلیون) بیشترین میزان مجموع مبتلایان را دارند.[۷]میزان هپاتیت سی در میان زندانیان در ایالات متحده ۱۰ تا ۲۰ برابر این میزان در جمعیت عمومی است، که این مطالعات نشان دهنده رفتارهای پرخطر مانند استعمال درون وریدی مواد مخدر (IDU) و خالکوبی با تجهیزات غیر استریل است. .[۱۹][۲۰]
تماس در حین مراقبتهای پزشکی
تزریق خون، فراوردههای خونی، و پیوند اعضا بدون آزمایش HCV ریسک بالای ابتلا را ایجاد میکند.[۵] ایالات متحده آزمایش جهانی را در سال ۱۹۹۲ پایه ریزی کرد. از آن زمان تا کنون میزان ابتلا با کاهشی تا میزان یک در ۱۰٬۰۰۰ تا ۱۰٬۰۰۰٬۰۰۰ در واحدهای خون[۶][۱۷] از میزان یک در ۲۰۰ واحد خون روبه رو بوده است. .[۲۱] این ریسک کم، باقی میماند زیرا یک دوره حدوداً ۱۱-۷۰ روزه بین این که یک اهداکننده خون احتمالی، هپاتیت سی بگیرد و این که جواب آزمایش خون مثبت باشد، زمان وجود دارد. .[۱۷] برخی کشورها هنوز به دلیل هزینه آن، برای هپاتیت سی آزمایش انجام نمیدهند.[۱۱]
کسی که از سوزن یک فرد مبتلا به HCV زخم ناشی از سوزن برمی دارد، پس از آن با احتمال ۱٫۸٪ ابتلا به بیماری رو به رو است.[۵] این احتمال بیشتر است چنانچه سوزن به کار رفته خالی و زخم عمیق باشد. .[۱۱] در تماس مخاط با خون هم ریسک ابتلا وجود دارد؛ اما این ریسک کم است، و اگر تماس خونی بر روی پوست سالم رخ دهد، هیچ ریسکی وجود ندارد.[۱۱]
تجهیزات بیمارستانی نیز هپاتیت سی را انتقال میدهند، از جمله: استفاده مجدد از سوزنها و سرنگها، استفاده چندباره از شیشههای دارو، کیسههای تنفسی، و تجهیزات جراحی غیر استریل.[۱۱] استانداردهای ضعیف در تسهیلات پزشکی و دندانپزشکی دلیل اصلی شیوع HCV در مصر است که بیشترین میزان ابتلا در جهان را داراست.[۲۲]
آمیزش جنسی
این که آیا هپاتیت سی از راه آمیزش جنسی قابل انتقال است، نامعلوم است.[۲۳] در حالی که بین رفتار جنسی پرخطر و هپاتیت سی پیوندی وجود دارد، روشن نیست که آیا انتقال بیماری ناشی از مصرف مواد مخدر است که به آن اشارهای نشده، یا خود رابطه جنسی.[۵] شواهد نشان میدهد که ریسکی برای زوجهای متشکل از دو جنس مخالف که با افراد دیگر رابطه جنسی ندارند، وجود ندارد.[۲۳] اعمال جنسی که سطوح بالای آسیب به لایه درونی مجرای مقعد را دربرمی گیرد، مانند دخول از راه مقعد، و یا اعمالی که هنگامی اتفاق میافتد که بیماریهای منتقل شونده از راه آمیزش جنسی، از جمله HIV یا زخم در ناحیه تناسلی، نیز وجود دارند، ریسک ابتلا ایجاد میکنند.[۲۳] دولت ایالات متحده تنها برای جلوگیری از انتقال هپاتیت سی در افراد دارای چند شریک جنسی، استفاده از کاندوم را توصیه میکند.[۲۴]
\\\ پیرسینگهای بدن\\\
خالکوبی با دو یا سه برابر خطر بیشتر هپاتیت سی همراه است.[۲۵] این میتواند به دلیل لوازم استریل نشده یا آلودگی رنگهای استفاده شده باشد.[۲۵] خالکوبی یا سوراخ کردن بدن (پیرسینگ) که پیش از اواسط دهه ۱۹۸۰ یا به صورت غیرحرفهای انجام میشد نگران کننده است، چرا که ممکن است تکنیکهای استریل کردن در این شرایط ضعیف باشد. ریسک در خالکوبیهای بزرگ تر بیشتر میشود.[۲۵] تقریباً نیمی از زندانیان از لوازم خالکوبی غیراستریل مشترک استفاده میکنند.[۲۵] به ندرت در مراکز مجاز خالکوبی ابتلا مستقیم به HCV رخ میدهد.[۲۶]
تماس با خون
لوازم بهداشتی شخصی مانند تیغها، مسواک، و لوازم مانیکور و پدیکور میتوانند با خون تماس پیدا کنند. به اشتراک گذاشتن آنها افراد را در معرض خطر HCV قرار میدهد.[۲۷][۲۸] افراد باید مراقب بریدگیها، زخمها، و دیگر خونریزیها باشند.[۲۸] HCV از طریق تماسهای معمول مانند بغل کردن، بوسیدن، یا غذا خوردن از ظروف یا وسایل آشپزی مشترک شیوع پیدا نمیکند.[۲۸]
انتقال از مادر به بچه
انتقال هپاتیت سی از مادر مبتلا به فرزند وی در کمتر از ۱۰٪ بارداریها اتفاق میافتد.[۲۹] هیچ اقدامی وجود ندارد که بتواند این ریسک را تغییر دهد.[۲۹] انتقال میتواند در دوره بارداری یا زایمان اتفاق افتد. یک زایمان طولانی با خطر بیشتر انتقال در ارتباط است.[۱۷] هیچ مدرکی مبنی بر اینکه تغذیه از شیر مادر HCV را انتقال میدهد وجود ندارد، گرچه مادر مبتلا باید از شیر دادن به نوزاد، در صورت شکاف و خونریزی از نوک سینه[۳۰] یا در صورتی که بار ویروسی وی زیاد است، خودداری کند.[۱۷]
تشخیص
آزمایشهای تشخیص هپاتیت سی عبارتند از: آنتی بادی HCV، تست الایزا (ELISA)، وسترن بلات، HCV RNA کمی.[۵] واکنش زنجیرهای پلی مراز (PCR)، میتواند HCV RNA را یک تا دو هفته پس از ابتلا شناسایی کند، در حالی که آنتی بادیها ممکن است برای شکل گیری و نمایاندن خود به زمان بسیار بیشتری نیاز داشته باشند.[۱۲] هپاتیت سی مزمن، ابتلا به ویروس هپاتیت سی است که بر اساس حضور RNA خود، تا شش ماه مقاومت نشان میدهد. .[۸] به این دلیل که بیماریهای مزمن معمولاً تا دهها سال علایمی نشان نمیدهند،[۸] پزشکان بالینی عموماً از طریق آزمایشهای عملکرد کبد و یا در حین آزمایشهای روتین از افراد دارای ریسک بالا، به این بیماری پی میبرند. آزمایش نمیتواند بین بیماریهای مزمن و حاد تمایزی قایل شود.[۱۱]
آزمایش خون
آزمایش هپاتیت سی معمولاً با آزمایشهای خون آغاز میشود تا با استفاده از روش ایمونواسی آنزیمی وجود پاد تنها در ویروس هپاتیت سی تشخیص داده شوند.[۵] اگر آزمایش مثبت باشد، برای تایید صحت ایمونواسی و به منظور تعیین شدت بیماری آزمایش دومی انجام میشود.[۵] آزمایش recombinant immunoblot صحت ایمونواسی را تایید کرده، و واکنش زنجیرهای پلیمراز ویروس هپاتیت سی و اسید ریبونوکلیئیک (RNA) شدت بیماری را تعیین میکند.[۵] اگر اثری از اسید ریبونوکلیئیک (RNA) و جود نداشته باشد و آزمایش immunoblot مثبت باشد، این به این معنی است که شخص قبلاً به ویروس آلوده شده اما یا بوسیله معالجه و یا خود به خود این ویروس از بین رفته است؛ اگر آزمایش immunoblot منفی باشد، به این معنی است که آزمایش ایمونواسی اشتباه بوده است.[۵] برای مثبت بودن آزمایشهای ایمونواسی بین شش تا هشت هفته باید از زمان آلودگی به ویروس گذشته باشد.[۹] آنزیمهای کبدی در ابتدای آلودگی به ویروس متغیر میباشند؛[۸] معمولاً پس از گذش هفت هفته از آلودگی به ویروس آنزیمهای کبدی افزایش مییابند.[۹] آنزیمهای کبدی ارتباط چندانی با شدت بیماری ندارند.[۹]
بافت برداری
بافت برداریهای کبدی میتوانند شدت آسیب کبدی را مشخص سازند، اما این فرایندها خطراتی نیز به همراه دارند[۳]. تغییرات معمولی که از طریق بافت برداری قابل تشخیص هستند تغییرات مربوط به لنفوسیتهای درون بافت کبد، فولیکولهای لنفاوی در ورید باب، و مجاری صفرا میباشند.[۳] چندین آزمایش خون را میتوان انجام داد که شدت آسیب را تعیین کرده و نیاز به بافت برداری را کاهش میدهند.[۳]
آزمایش
تنها بین ۵ تا ۵۰٪ کسانی که در ایالات متحده و کانادا به این ویروس آلوده هستند از وضعیت خود اطلاع دارند.[۲۵] برای افرادی که در خطر زیادی هستند، مانند کسانی که خالکوبی بر بدن خود دارند آزمایش توصیه میشود.[۲۵] آزمایش همچنین به افرادی که آنزیم کبدی بالایی دارند توصیه میشود چرا که آنزیم کبدی بالا در اغلب اوقات تنها نشانه مزمن هپاتیت میباشد.[۳۱] آزمایش دائم در ایالات متحده توصیه نمیشود.[۵]
پیشگیری
تا سال ۲۰۱۱ هیچ واکسنی برای هپاتیت سی وجود نداشته. تولید واکسنها در حال پیشرفت بوده و برخی از این پیشرفتها نتایج امیدبخشی را از خود نشان دادهاند.[۳۲] ترکیبی از راهکارهای پیشگیرانه، نظیر طرح تعویض سرنگ و درمان سوء مصرف مواد، خطر ابتلا به هپاتیت سی را در بین تزریق کنندگان مواد حدود ۷۵٪ کاهش میدهد.[۳۳] آزمایش اهداکنندگان خون در سطح ملی امری مهم تلقی میشود، چرا که این کار به معنی پیروی از احتیاطات عمومی در درون مراکز مراقبتهای بهداشتی است.[۹] درکشورهایی که به اندازه کافی سرنگ پاکیزه وجود ندارد، مراقبین سلامت باید داروها را از راه دهان به بیماران بدهند و نه از راه تزریق.[۱۱]
درمان
ویروس هپاتیت سی در ۵۰ تا ۸۰٪ مبتلایان به این ویروس موجب بوجود آمدن عفونت مزمن میشود. حدود ۴۰ تا ۸۰٪ این عفونتها با درمان از بین میروند.[۳۴][۳۵] در موارد نادر، این عفونت میتواند بدون درمان از بین برود.[۶] افرادی که دچار هپاتیت سی مزمن هستند باید از مصرف الکل و داروهایی که موجب تولید سم در کبد میشوند خودداری کنند،[۵] این افراد همچنین باید برای هپاتیت آ و هپاتیت ب واکسینه شوند.[۵] افراد مبتلا به سیروز کبدی میبایست به منظور تشخیص سرطان کبد آزمایشهای فراصوتی انجام دهند.[۵]
در حال حاضر آزمایش ویروس هپاتیت سی دو مرحله ای، گران و ناخوشایند است، به طور گسترده در دسترس نیست و یا به طور کلی در سطح جهان صرفه اقتصادی ندارد اما سیستم جدید آزمایش آنتی ژن ویروس هپاتیت سی که توسط محققان دانشگاه ارواین امریکا ابداع شده است، نسبت به آزمایش های فعلی مقرون به صرفه تر و از حساسیت و ویژگی بهبود یافته قابل توجهی برخوردار است.[۳۶] در پژوهشی دیگر مطالعات محققان بیمارستان TWH تورنتو کانادا نشان می دهد که یک رژیم دارویی ساده 12 هفته ای قادر به درمان عفونت هپاتیت C است. نتایج اولیه این آزمایش روی 99 درصد بیماران موفقیت آمیز بوده است. این رژیم، ترکیب دو داروی sofosbuvir و velpatasvir است و روزی یک بار به بدن تزریق می شود.[۳۷]
داروها
افرادی که آلودگی آنها به ویروس هپاتیت سی اثبات شده و دارای ناهنجاریهای کبدی هستند میبایست به دنبال درمان خود باشند.[۵] درمان فعلی این بیماری ترکیبی است از پگ اینترفرون و داروی ضد ویروس ریباویرین که بسته به نوع ویروس هپاتیت سی ۲۴ تا ۴۸ هفته به طول میانجامد.[۵] آثار بهبودی در ۵۰ تا ۶۰٪ افراد درمان شده قابل مشاهده است.[۵] ترکیب بوسپروویر یا تلاپرویر با ریباویرین و پگ اینترفرون آلفا موجب بهبود واکنش به ژنوتیپ ۱ هپاتیت سی میشود.[۳۸][۳۹][۴۰] پیدایش عوارض جانبی با درمان این بیماری امری عادی است؛ نیمی از افرادی که درمان میشوند دچار علائم آنفلوآنزا مانند، و یک سوم آنها دچار مشکلات احساسی میشوند.[۵]درمان در طول شش ماهه اول این بیماری موثر تر از زمانی است که هپاتیت سی مزمن میشود.[۱۲] اگر شخصی دچار عفونت جدیدی شود و با گذشت هشت تا دوازده هفته این عفونت از بین نرود، به وی توصیه میشود تا از پگ اینترفرون (pegylated interferon) به مدت ۲۴ هفته استفاده کند.[۱۲] برای افراد مبتلا به تالاسمی (نوعی اختلال خونی)، ریباویرین (ribavirin) مفید به نظر میرسد، اما این دارو نیاز به تزریق خون را افزایش میدهد. .[۴۱]
طب جایگزین
طرفداران این طب ادعا میکنند که بسیاری از درمانهای جایگزین نظیر خار شیری، جینسنگ، و نقره کلوئیدی برای هپاتیت سی مفید میباشند.[۴۲] با این حال، هیچ کدام از این درمانهای جایگزین بهبود درمانی هپاتیت سی را از خود نشان ندادهاند، و هیچ مدرکی دال بر اینکه درمانهای جایگزین تاثیری بر ویروس این بیماری داشته باشند وجود ندارد.[۴۲][۴۳][۴۴]
پیش بینی روند بیماری
بسته به نوع ژنوتیپ، واکنشها نسبت به درمان میتواند متفاوت باشد. در افرادی که ژنوتیپ ۱ ویروس هپاتیت سی را دارند و طول دوره درمانی آنها ۴۸ هفته است میزان واکنش طولانی مدت حدود ۴۰ تا ۵۰٪ میباشد.[۳] در ۷۰ تا ۸۰٪ افرادی که ژنوتیپ ۲ و ۳ ویروس هپاتیت سی را دارند و طول دوره درمانی آنها ۲۴ هفته میباشد واکنش طولانی مدت روی میدهد.[۳] در افرادی که ژنوتیپ ۴ دارند و طول دوره درمانی آنها ۴۸ هفته میباشد میزان واکنش طولانی مدت حدود ۶۵٪ میباشد. در حال حاضر نشانههای درمانی در بیماری ژنوتیپ ۶ کم میباشد، و این نشانههای درمانی برای دوره درمانی ۴۸ هفتهای بوده و دوز آن نیز به میزان دوز بیماری ژنوتیپ ۱ میباشد.[۴۵]
همه گیر شناسی
|
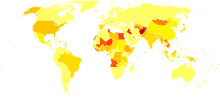
no data <10 ۱۰-۱۵ ۱۵-۲۰ ۲۰-۲۵ ۲۵-۳۰ ۳۰-۳۵
|
۳۵-۴۰ ۴۰-۴۵ ۴۵-۵۰ ۵۰-۷۵ ۷۵–۱۰۰ >۱۰۰
|
بین ۱۳۰ تا ۱۷۰ میلیون نفر، یا ۳٪ جمعیت جهان، با هپاتیت سی مزمن زندگی میکنند.[۴۶] هر ساله بین ۳ تا ۴ میلیون نفر به این ویروس آلوده میشوند، و سالیانه بیش از ۳۵۰،۰۰۰ نفر به خاطر بیماریهای مربوط به هپاتیت سی میمیرند.[۴۶] در ایران نیز طبق آخرین آمار شیوع هپاتیت C کمتر از نیم درصد جمعیت کشور است. این در حالی است که در کشورهای همسایه افغانستان ، عراق ، پاکستان و کشورهای شمالی ایران شیوع هپاتیت C بیش از 5 تا 6 برابر کشور ایران است.[۴۷]
ترکیبی از مصرف ایدوکسوریدین (IDU) و داروهای تزریقی و یا تجهیزات پزشکی ضد عفونی نشده در قرن بیستم منجر به افزایش قابل توجه این میزان شده است.[۱۱] در ایالات متحده حدود ۲٪ از مردم به هپاتیت سی مبتلا هستند،[۵] و هر ساله بین ۳۵،۰۰۰ تا ۱۸۵،۰۰۰ نفر به این بیماری مبتلا میشوند. میزان شیوع این بیماری در ایالات متحده از دهه ۱۹۹۰ به خاطر بهبود آزمایشهای خونی قبل از تزریق خون کاهش یافته است.[۱۲] مرگ و میر ناشی از ویروس هپاتیت سی در ایالات متحده سالیانه بین ۸،۰۰۰ تا ۱۰،۰۰۰ نفر میباشد. از آنجایی که افراد قبل از آزمایش ویروس هپاتیت سی با تزریق خون به این بیماری دچار شده و میمیرند، انتظار میرود که این میزان مرگ و میر افزایش یابد.[۴۸] میزان آلودگی به ویروس این بیماری در برخی از کشورهای آفریقایی و آسیایی بالا است.[۴۹] کشورهایی که میزان آلودگی بالایی دارند شامل مصر (۲۲٪)، پاکستان (۴٫۸٪) و چین (۳۰۲٪) میباشند.[۴۶] میزان بالای این آلودگی در مصر مربوط میشود به حرکت در حال حاضر متوقف شده این کشور در درمان همگانی شیستو زومیازیس (schistosomiasis) با استفاده از سرنگهای شیشهای که به طور نامناسبی ضد عفونی شده بودند.[۱۱]
تاریخچه
در اواسط دهه ۱۹۷۰، هاروی جی آلتر (Harvey J. Alter)، رئیس بخش بیماریهای عفونی سازمان انتقال خون واقع در موسسات ملی بهداشت، و تیم تحقیقاتی اش اثبات کردند که در اکثر موارد ویروس هپاتیت آ یا هپاتیت ب نقشی در بروز هپاتیت پس از تزریق خون به بیمار ندارند. علیرغم این اکتشاف، در طول دهه بعد تلاشهای تحقیقاتی بینالمللی برای تشخیص ویروس این بیماری با شکست مواجه شد. در سال ۱۹۸۷، مایکل هاگتون (Michael Houghton)، کوی لیم چو (Qui-Lim Choo)، و جورج کو (George Kuo) در شرکت کایرون (Chiron) با همکاری دکتر دی دبیلیو برادلی (D.W. Bradley) از مرکز کنترل و پیشگیری بیماریها، به منظور تشخیص اورگانیسم ناشناخته و انجام آزمایش تشخیصی از یک شیوه جدید تولید مثل مولوکولی ااستفاده کردند.[۵۰] در سال ۱۹۸۸، آلتر (Alter) ویروس مورد نظر را با تایید وجود آن در گروهی از نمونههای هپاتیت غیر آ و غیر ب به اثبات رسانید. در آوریل ۱۹۸۹، کشف ویروس هپاتیت سی در دو مقاله در مجله «ساینس» منتشر شد.[۵۱][۵۲]
این کشف منجر به پیشرفتهای مهمی در زمینه تشخیص بیماری و درمان ضد ویروسی شد.[۵۰] در سال ۲۰۰۰، دکتر آلتر (Alter) و هاگتون (Houghton) به خاطر «کار پیشگامانه خود که منجر به کشف ویروس هپاتیت سی و توسعه شیوههای آزمایشی که باعث کاهش خطر ابتلا به هپاتیت مرتبط با تزریق خون در ایالات متحده از ۳۰٪ در سال ۱۹۷۰ به صفر درصد در سال ۲۰۰ شد» مفتخر به دریافت جایزه لاسکر برای پژوهش پزشکی بالینی شدند.[۵۳] شرکت کایرون (Chiron) حق انحصاری کشف ویروس و تشخیص آن را چندین بار به نام خود به ثبت رسانید.[۵۴] در سال ۱۹۹۰ سی دی سی (CDC) پس از اینکه شرکت کایرون (Chiron) ۱٫۹ میلون دلار به سی دی سی (CDC) و ۳۳۷،۵۰۰ دلار به برادلی (Bradley) پرداخت کرد از تقاضانامه ثبت حق انحصاری خود صرفنظر کرد. در سال ۱۹۹۴، برادلی (Bradley) که به دنبال بی اعتبار کردن ثبت امتیاز انحصاری توسط شرکت کایرون (Chiron) و دریافت خسارت و حق کشف بود، دادخواستی را علیه این شرکت تنظیم و خود را به عنوان شریک کشف ویروس معرفی کرد. وی پس از ناکام ماندن در دادگاه استیناف از این دادخواست خود صرفنظر کرد.[۵۵]
جامعه و فرهنگ
اتحادیه جهانی هپاتیت روز جهانی هپاتیت را برپا میکند. مراسم این روز همه ساله در ۲۸ ژوئیه برگزار میگردد.[۵۶] هزینههای اقتصادی هپاتیت سی هم برای خود فرد و هم برای اجتماع قابل توجه میباشند. در سال ۲۰۰۳ در ایالات متحده متوسط هزینه مادام العمر این بیماری چیزی حدود ۳۳،۴۰۷ دلار برآورد شده است،[۵۷] و تا تاریخ ۲۰۱۱ این هزینه بعلاوه هزینه پیوند کبد چیزی حدود ۲۰۰،۰۰۰ دلار برآورد شده است.[۵۸] در کانادا هزینه یک دوره درمانی ضد ویروسی در سال ۲۰۰۳ ۳۰،۰۰۰ دلار کانادا میبود،[۵۹] این در حالی است که در سال ۱۹۹۸ هزینه این دوره درمانی در ایالات متحده بین ۹،۲۰۰ تا ۱۷،۶۰۰ دلار میبود.[۵۷] در بسیاری از مناطق دنیا مردم قادر به پرداخت هزینه درمان ضد ویروسی نمیباشند چرا که این افراد تحت پوشش بیمه درمانی نیستند و یا نوع بیمهای که دارند هزینهای در قبال درمانهای ضد ویروسی پرداخت نمیکند.[۶۰]
تحقیقات
از سال ۲۰۱۱، حدود ۱۰۰ نوع دارو برای هپاتیت سی در حال ساخت میباشد.[۵۸] این داروها شامل واکسنهایی میشوند که برای درمان هپاتیت استفاده میشوند، و همچنین تعدیل کنندگان سیستم ایمنی، و بازدارندههای سیکلوفیلین میباشند.[۶۱] ظهور همه این درمانهای بالقوه جدید به دلیل شناخت بهتر ویروس هپاتیت سی بوده است.[۶۲]
ادامه مطلب
| هپاتیت ب | |
|---|---|

|
|
| آیسیدی-۱۰ |
B16, B18.0-B18.1 |
| آیسیدی-۹ | 070.2-070.3 |
| اُمیم | 610424 |
| دادگان بیماریها | ۵۷۶۵ |
| مدلاین پلاس | 000279 |
| ایمدیسین | med/992 ped/978 |
| پیشنت پلاس | هپاتیت ب |
| سمپ | D006509 |
هپاتیت B یا هپاتیت ب (به انگلیسی: Hepatitis B) نوعی بیماری ویروسی در انسانهاست که به کبد بیشترین آسیب را میزند. ویروس این بیماری یکی از جدیترین انواع هپاتیت را سبب میشود.
محتویات
ویروس هپاتیت ب
این ویروس عامل مولد هپاتیت ب است و جزء ویروسهای کبدی دارای DNA طبقهبندی میشود. HBV از خانواده Hepadenaviridae میباشد. بافت هدف این بیماری و میزبان آن محدود و فقط در کبد، گاهی پانکراس و کلیه انسان و میمون را نیز آلوده میکند. این ویروس کوچک، دارای پوشش، دارای DNA دو رشته و حلقوی که قسمتی از آن تک رشتهای است ودارای آنزیم ریورز ترانس کرپیتاز (RTase) است که این آنزیم چسبیده به ژنوم ویروس است و دارای فعالیت ریبونوکلئاز است.
این ویروس دارای ۳ نوع آنتی ژن مهم به نامهای آنتی ژن سطحی، آنتی ژن مرکزی و یک آنتی ژن دیگر است. آنتی ژن سطحی که آنتی ژن استرالیا نامیده میشود (بعلت اینکه اولین بار در سرم یک فرد بومی استرالیل که در ظاهر سالم شناسایی شد). از نظر شکل ظاهری دارای دو فرم است: ۱- شکل کروی که فراوانترین نوع این خانواده است. ۲- شکل لولهای یا رشتهای. این آنتی ژن در PH کمتر از ۴ به مدت ۶ ساعت پایدار میماند؛ ولی در این PHعفونت زایی هپاتیت B از بین میرود. این ویروس به علت داشتن غشا در برابر اتر مقاوم است، PH پایین، حرارت متوسط، یخ زدن و اشعه ماورا بنفش پایدار میماند. DNA ویروس تمایل زیادی برای ادغام شدن با DNA سلول میزبان دارد. نسخه برداری ویروس توسط عوامل نسخه بردار سلول میزبان کنترل میشود.
پوشش ویروس هپاتیت B شامل سه پلی پپتید بصورت همپوشان است که پروتئینهای اصلی Small (S)، Middle (M) و Large (L) را بوجود میآورد و به ترتیب توسط سکانسهای ژنی S، Pre-S1 و Pre-S2 کدگذاری میشوند. پلی پپتید s دارای وزن مولکولی ۲۴ کیلو دالتون و۲۲۶ اسیدآمینه، توسط ناحیه S ژن سطحی ویروس کد گذاری میشود و به نام پروتئین اصلی (Major)خوانده میشود؛ که شامل دترمینانتهای ساب تایپیک متداول، (a) و (d/y , w/r) میباشد. بر اساس متغیرهای سرولوژیکی بیوشیمیایی و ژنتیکی مشاهده شده در HBsAg جداشده از سویههای مختلف HBV، این ویروس به ژنوتایپها و سروتایپهای مختلفی طبقهبندی شده است.
این ویروس دارای چندین ساب تایپ اصلی به نامهای ayr, ayw, adr, adw میباشد؛ که شاخص آنتی ژنیکی a در همگی مشترک است و از نظر اپیدمیولوژی در جهت تعیین شیوع عفونت اهمیت ویژهای دارد. همچنین دو شاخص آنتی ژنیکی دیگر مثل “r” یا “w” و “y” یا “d” را نیز شامل میگردند. در افرادی که به عفونت HBV آلوده شدهاند پاسخ ایمنی علیه شاخص a ایجاد میشود. . آنتی بادی ایجاد شده علیه شاخص a در مقابل همه ساب تایپهای متداول HBV ایمنی میدهد.
علاوه بر چهار ساب تایپ اصلی ساب تایپهای غیرمعمول HBV نظیر aywr, adwr, adyr, adywr نیز گزارش شدهاند. ساب تایپ ayw بیشتر در نواحی مدیترانه، خاورمیانه، هند شایع میباشد. ساب تایپ adw در شمال غربی اروپا و آمریکا مشاهده شده است. وساب تایپهای دارای شاخص r اکثراً در خاور دور دیده شده است. سروتایپهای HBV در تشخیص و بررسیهای اپیدمیولوژیک حائز اهمیت است.
علایم
علایم و نشانههای هپاتیت ب مهمولا ۳ ماه بعد از آلوده شدن به ویروس HBV ظاهر میشوند و میتوانند طیف گستردهای از علایم را شامل شود،[۱] علایم عفونت هپاتیت ب میتواند شامل:
- درد شکم
- ادرار تیره[۱]
- تب
- درد مفاصل و ماهیچهها
- حالت تهوع و استفراغ
- زرد شدن پوست و سفیدی چشم ها[۱]
- خستگی و ضعف
نحوه انتقال
دلیل ابتلا به بیماری هپاتیت ب، ویروس این بیماری بنام HBV یا ویروس هپاتیت ب است. دلایل معمول انتقال هپاتیت ب به بدن افراد شامل:
۱)تماس جنسی، درصورتیکه شما رابطه جنسی محافظت نشده با فرد مبتلا به این بیماری داشته باشید که خون، بزاق، منی و یا ترشحات واژنیاش وارد بدن شما شود، ممکن است شما مبتلا شوید.
۲)استفاده از سوزن مشترک، ویروس هپاتیت ب براحتی از طریق سوزن و سرنگ آلوده به خون فرد مبتلا منتقل میشود. این راه شامل تیغ اصلاح و لوازم دندانپزشکی غیر استریل نیز میشود.
۳)انتقال از مادر به فرزند، زنان باردار مبتلا به این بیماری میتوانند ویروس را به بدن فرزند خود منتقل نمایند.
۴)انتقال از راه تزریق خون وفراوردههای خونی بیمار مبتلا به فرد سالم. امروزه چون قبل از انتقال خون، سالم بودن خون اهداشده از نظر ویروس هپاتیت بررسی میشود احتمالابتلا از این طریق بسیار کاهش یافته است ولی درگذشته بیماران بخصوص بیماران هموفیل که نیاز به تزریق خون مکرر داشتند اغلب از این راه مبتلا به هپاتیت میشدند.
5-احتمال انتقال این بیماری از طریق استنشاق سرم افرادی که خیلی آلوده هستند وجود دارد.
بیماریزایی
از طریق مایعات بدن، خون، مقاربت جنسی ودر ماههای آخر حاملگی از مادر به جنین منتقل میشود و ابتلا به این بیماری هیچ ارتباطی به سن، فصل و جنس ندارد. دارای دوره کمون متوسط سهماهه است. در ۵ تا ۱۰ در صد مبتلایان تبدیل به حالت مزمن میشود و گاهی منجر به سرطان کبد میشود. این ویروس ۳ روز پس از ورود به سلولهای کبدی شروع به تکثیر مینماید؛ اما علایم بالینی بعلت نا معلومی حدود ۴۵ روز بعد ظاهر میشود که بستگی به راه ورود مقدار ویروس و وضعیت فرد مبتلا دارد. علایم بالینی شامل تهوع، استفراغ، بی اشتهایی شدید میباشد که به دنبال آن یرقان ظاهر میشود (گرچه هپاتیت بدون یرقان نیز شایع است). حدود ۸۵ در صد بیماران کاملاً بهبود حاصل پیدا میکند. مرگ و میر بین ۷/۲- ۶/۰ درصد است که بسته به سن و شرایط متغیر است. حدود ۱۰ تا ۵ در صد افراد به هپاتیت مزمن میشوند که این مبتلایان منبع اصلی انتشار ویروس در جامعه هستند. در اکثر موارد ژنوم ویروس ادغام شده در ژنوم سلولهای سرطانی دیده میشود. درمان اختصاصی برای هپاتیت B وجود ندارد. درمان بیشتر جنبه علامتی و حفاظتی دارد. انترفرون آلفا ممکن است برای هپاتیت مزمن موثر باشد. این ویروس انتشار جهانی دارد. حاملین ویزوس در جهان حدود ۲۰۰ میلیون نفر هستند که یک میلیون آنها در امریکا زندگی میکنند. افراد در معرض خطر شامل شاغلین، در مراکزبهداشتی و درمانی، کارکنان آزمایشگاهها، کارکنان بانک خون، افراد ساکن در مناطق آندمیک (چین، آفریقا …………..) نوزادان متولدشده از مادر مبتلا، معتادین تزریقی و افراد دارای هموفیلی و دریافت کنندگان خون و محصولات آن. بیشترین موارد آلودگی به این ویروس در کشورهای عقب مانده است بطوریکه ۵ درصد نوزادان در هنگام متولد شدن و شیردادن مبتلا میشوند.
پیشگیری
روشهای پیشگیری و کنترل وجود دارند که عبارتند از: ۱- انجام واکسیناسیون ۲- کنترل و جدا کردن خونهای آلوده ۳- تزریق ایمنوگلوبین به نوزدان که از مادر مبتلا متولد شده و افرادی که با بیماران تماس داشته ۴- عدم مصرف خون کسانی که هرگونه ناراحتی کبدی دارند ۵- استفاده از وسایل مانند دستکش هنگام معاینه بیمار و …….. ۶- حذف سریع وسایل آلوده وضدعفونی وسایل مورد استفاده ۷- اجتناب از رفتارهای اجتماعی پر خطر وخطرساز که انتشار ویروس را تسهیل میکند
در ایران
بنا بر گفته رئیس شبکه هپاتیت کشور در سال ۱۳۹۳، یک میلیون و ۴۰۰ هزار نفر در ایران به این بیماری مبتلا هستند و ناقل آن به حساب میآیند. از سال ۱۳۷۳ و با انجام واکسیناسیون نوزادان و افراد پرخطر میزان بروز هپاتیت B رو به کاهش است و هپاتیت B در جمعیت زیر ۲۰ سال کشور بسیار نادر میباشد.[۲]
جستارهای وابسته
منابع
- «1.4 میلیون ایرانی مبتلا به هپاتیت B». خبرگزاری مهر.
- انواع هپاتیت به نقل از سایت پزشکان بدون مرز
- وضعیت هپاتیت در ایران
- Yoder MC, Polin RA. Hepatits B virus. In:Fanaroff AA, Martin RJ, eds. Neonatal PerinatalMedicine. 6th ed. St. Louis: Mosby; ۱۹۹۷: ۷۸۴-۶.
ادامه مطلب
| هپاتیت A | |
|---|---|

نمونهای از زردی به وجود آمده در اثر هپاتیت
|
|
| آیسیدی-۱۰ | B15 |
| آیسیدی-۹ | 070.0, 070.1 |
| دادگان بیماریها | ۵۷۵۷ |
| مدلاین پلاس | 000278 |
| ایمدیسین | med/۹۹۱ ped/977 |
| پیشنت پلاس | هپاتیت آ |
| سمپ | D006506 |
هپاتیت آ (به انگلیسی: Hepatitis A) (که سابقاً با نام هپاتیت عفونی شناخته میشد) نوعی بیماری عفونی حاد کبد است که توسط ویروس هپاتیت آ (HAV) ایجاد میشود.[۱] بسیاری از افراد مبتلا بویژه افراد کم سن و سال علایم کمی دارند و یا هیچ علامتی ندارند.[۲] فاصله زمانی بین ابتلاء و بروز علایم در افرادی که علایم بیماری را نشان میدهند بین دو تا شش هفته است.[۳] اگر علایمی وجود داشته باشند به طور عادی تاهشت هفته باقی میمانند، علایم آن ممکن است شامل تهوع، استفراغ، اسهال، زردی پوست، تب و شکم درد باشد.[۲] حدود ۱۰–۱۵٪ افراد طی شش ماه پس از ابتلای اولیه بازگشت علایم را تجربه میکنند.[۲] نارسایی حاد کبد به ندرت ممکن است اتفاق بیافتد با این حال در میان افراد سالخورده رایج تر است.[۲]
این بیماری از طریق خوردن یا نوشیدن غذا و آبی که با مدفوع فرد آلوده، آلوده شده است گسترش مییابد.[۲] سخت پوستان دریایی که به اندازه کافی پخته نشدهاند منشأ بیماری نسبتاً رایجی هستند.[۴] این بیماری همچنین ممکن است از طریق تماس نزدیک با فرد آلوده منتقل شود.[۲] در حالی که بچهها اغلب در زمان ابتلاء هیچ علامتی ندارند اما میتوانند آلودگی را به دیگران سرایت دهند.[۲] یک بار ابتلاء به این بیماری، فرد را برای تمام عمر در مقابل آن مصون میسازد.[۵] تشخیص بیماری نیاز به آزمایش خون دارد چرا که علایم آن شبیه به علایم چند بیماری دیگر است.[۲] این ویروس یکی از پنج ویروس شناخته شده هپاتیت است که عبارتند از: آ، ب، سی، دی و ای.
واکسن هپاتیت آ در پیشگیری از بیماری مؤثر است.[۲][۶] در برخی از کشورها این واکسن به طور معمول برای کودکان و افراد در معرض خطر بالای ابتلاء که قبلاً واکسینه نشدهاند توصیه میشود.[۲][۷] و به نظر میرسد به صورت مادام العمر مؤثر باشد.[۲] سایر اقدامات پیشگیرانه شامل شستن دست و پخت صحیح غذا میشود.[۲] هیچ درمان خاصی برای تهوع یا اسهال با استفاده از دارو و استراحت وجود ندارد تا در صورت لزوم توصیه شود.[۲] عفونتها معمولاً به طور کامل و بدون ایجاد بیماری کبدی مزمن برطرف میشوند.[۲] برای درمان نارسایی حاد کبد، در صورت وقوع، به پیوند کبد نیاز خواهد بود.[۲]
در سراسر جهان هر ساله حدود ۵/۱ میلیون مورد ابتلاء علامت دار رخ می هد.[۲] و روی هم رفته احتمالاً دهها میلیون نفر مبتلا میشوند.[۸] این بیماری در مناطقی از جهان که وضعیت بهداشتی ضعیفی دارند و آب سالم به اندازه کافی در دسترس نیست رایج تر است.[۷] در کشورهای در حال توسعه حدود ۹۰٪ کودکان تا سن ۱۰ سالگی به این بیماری مبتلا شدهاند و بنابراین در بزرگسالی مصون هستند.[۷] این بیماری اغلب در کشورهای نسبتاً توسعه یافته که کودکان در سنین کم در معرض بیماری قرار نمیگیرند و واکسیناسیون گسترده وجود ندارد شیوع پیدا میکند.[۷] در سال ۲۰۱۰ بیماری حاد هپاتیت A منجر به مرگ ۱۰۲۰۰۰ نفر شد.[۹] ۲۸ جولای (۶ مرداد) هر سال به منظور آگاهی دادن در مورد هپاتیت ویروسی به عنوان روز جهانی هپاتیت نام گذاری شده است.[۷]
محتویات
علایم
| ویروس مولد هپاتیت A | |
|---|---|
 |
|
| میکروگراف الکترونی از ویریون هپاتیت ای. | |
| طبقهبندی ویروسها | |
| Group: | گروه ۴ ((+)ssRNA) |
| تیره: | پیکورنا |
| سرده: | هپاتوویروس |
| گونه: | ویروس هپاتیت ای |
علایم بیماری معمولاً تا ۲ ماه به طول میانجامد، اگرچه در بعضی موارد بیمار ممکن است تا ۶ ماه این علایم را داشته باشد:[۱۰]
- خستگی (پزشکی)
- تب
- تهوع
- بیاشتهایی
- یرقان و زردی پوست یا چشمها در اثر بیلیروبین
- صفرا از جریان خون جدا شده و به ادرار میپیوندد و رنگ آن را تیره میکند
- اسهال
جستارهای وابسته
منابع
- Ryan KJ, Ray CG (editors) (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 541–4. ISBN 0-8385-8529-9.
- Matheny, SC; Kingery, JE (1 December 2012). "Hepatitis A.". Am Fam Physician 86 (11): 1027–34; quiz 1010–2. PMID 23198670.
- Connor BA (2005). "Hepatitis A vaccine in the last-minute traveler". Am. J. Med. 118 (Suppl 10A): 58S–62S. doi:10.1016/j.amjmed.2005.07.018. PMID 16271543.
- Bellou, M.; Kokkinos, P.; Vantarakis, A. (March 2013). "Shellfish-borne viral outbreaks: a systematic review.". Food Environ Virol 5 (1): 13–23. doi:10.1007/s12560-012-9097-6. PMID 23412719.
- The Encyclopedia of Hepatitis and Other Liver Diseases. Infobase. 2006. p. 105. ISBN 9780816069903.
- Irving, GJ.; Holden, J.; Yang, R.; Pope, D. (2012). "Hepatitis A immunisation in persons not previously exposed to hepatitis A.". Cochrane Database Syst Rev 7: CD009051. doi:10.1002/14651858.CD009051.pub2. PMID 22786522.
- "Hepatitis A Fact sheet N°328". World Health Organization. July 2013. Retrieved 20 February 2014.
- Wasley, A; Fiore, A; Bell, BP (2006). "Hepatitis A in the era of vaccination.". Epidemiol Rev 28: 101–11. doi:10.1093/epirev/mxj012. PMID 16775039.
- Lozano, R (Dec 15, 2012). "Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet 380 (9859): 2095–128. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
- "Hepatitis A Information for the Public". Center for Disease Control. 2009-09-17. Retrieved 2011-01-08.
پیوند به بیرون
ادامه مطلب
هپاتیت (به انگلیسی: Hepatitis) به معنی التهاب در پارانشیم کبد است و به دلایل مختلفی میتواند ایجاد شود که بعضی از آنها قابل سرایت هستند و برخی مسری نیستند. از عواملی که ایجاد هپاتیت میکنند میتوان به افراط در مصرف الکل، اثر برخی داروها، آلودگی به باکتری و همچنین ویروس اشاره نمود. هپاتیت ویروسی منجر به عفونت کبدی میگردد.[۱]
عامل بیماری هپاتیت ویرال (ویروسی) یک ویروس است و در ابتدا میتواند مثل یک سرماخوردگی بروز نماید؛ ولی بیماری مزمن هپاتیت "C" بر عکس سرماخوردگی معمولی به دلیل از کار افتادن کبد و مشکل بودن درمان میتواند حیات بیمار را تهدید کند. بیشتر مبتلایان به هپاتیت از نوع C و B علائمی ندارد. برخی از این بیماران علائم سرشتی عفونت ویروسی را نشان میدهند از قبیل خستگی، دل درد، درد عضلانی و تهوع و بی اشتهایی، ولی در موارد پیشرفته علائم نارسایی کبدی بروز میکند که شامل تورم شکم، اندامها، یرقان و خونریزیهای گوارشی و ... است.
در ایران بالغ بر ۳٪ افراد آلوده به این ویروس میباشند.[۲]حدود ۷۵ الی ۸۰ درصد از افرادی که تازه به این ویروس مبتلا شدهاند، دچار پیشرفت و مزمن شدن این بیماری شده و از بین آنها نیز ۶- الی ۷۰ درصد به بیماریهای مزمن کبدی دچار میشوند. از بین افراد حدود ۵ الی ۲۰ درصد به سیروز کبدی مبتلا شده و ۱ الی ۵ درصد آنان بر اثر بیماری سیروز کبدی و یا سرطان کبد میمیرند.
محتویات
انواع
هپاتیت ویروسی
در حال حاضر ۸ نوع ازاین ویروس شناخته شدهاست.
- هپاتیت نوع A
- هپاتیت نوع B
- هپاتیت نوع C
- هپاتیت نوع D (همیشه همراه با نوع B)
- هپاتیت نوع E
- هپاتیت نوع F
-
هپاتیت نوع G
- در حال حاضر ۱۰ تا ۱۵ درصد افراد در هیچکدام از این دستهها قرار نمیگیرند به همین دلیل میشود انتظار ویروس نوع H را نیز داشت.[۳]
روشهای انتقال هپاتیت ب و c
این ویروس عمدتاً از طریق تماس با خون افراد آلوده منتقل میشود.
همچنین روشهای زیر میتواند باعث انتقال این ویروس گردد:
- ارتباط جنسی با افراد آلوده
- استفاده از سوزنهای آلوده که به عنوان سرنگ استفاده میشود، به ویژه در افراد معتاد به مواد مخدر تزریقی و همچنین سوراخ شدن بدن با هر وسیلهٔ تیز یا سوزن آلوده (مثل خالکوبی غیر بهداشتی)
- استفاده از لوازم شخصی به صورت اشتراکی
- دریافت فرآوردههای خون و پلاسمای آلوده که در ایران اکثراً در بیماران تالاسمی و هموفیلی دیده میشود.
- زخمی شدن پوست بدن در یک بخش آلودهٔ بیمارستانی.
آزمایشها
از دیگر نکات مهم در مورد این ویروس این است که به تدریج به کبد آسیب میرساند. یک کبد سالم مواد شیمیایی مورد نیاز بدن را میسازد و مواد سمی را از خون خارج میکند. وقتی شما به این بیماری مبتلا میشوید کبد شما ملتهب میشود و بافت طبیعی تخریب شده به جای آن بافت فیبری و فرسوده میماند.
پس از تشخیص پزشک آزمایش کبد انجام میگیرد. این کار از طریق آزمایشهای خون، سونوگرافی و نمونه برداری از کبد کار بسیار آسانی است و از طریق بیحسی موضعی و از طریق یک سوزن نمونه گیری انجام میشود و بیمار حداکثر یک روز در بیمارستان بستری میشود. پژوهشگران ایرانی نانو ابزار کاغذی را برای آنالیز DNA ابداع کردند که قادر به تشخیص سریع و ارزان بیماری هایی همچون هپاتیت B و ناباروری در مردان است.[۴]
جلوگیری
برای جلوگیری از انتشار این ویروس کارهای زیر ضروری به نظر میرسد:
- زخم و بریدگیهای پوست را خودتان پانسمان کنید. در صورت نیاز به کمک برای پانسمان زخم از دستکش استریل استفاده شود.
- در صورتی که به این بیماری مبتلا هستید، خون، پلاسما و اعضای بدن و بافت اهداء نکنید.
- از ریشتراش، مسواک، و لوازم آرایشی با لوازم شخصی دیگران به طور مشترک استفاده نکنید.
- به یاد داشته باشید غیر از واکسن نوع B این بیماری، این بیماری واکسن و درمان کامل ندارد. ازاینرو پیشگیری از آلودگی دیگران با عمل به توصیههای بهداشتی بر عهدهٔ شماست.
ادامه مطلب
| بیماری هانتینگتون | |
|---|---|

تصویر میکروسکپی از نورون خاردار میانی(رنگ زرد) همراه توده مشتمل(نقطه با رنگ نارنجی) که روند بیماری را نشان میدهند٬ نگاره با پهنه ۳۶۰ میکرومتر
|
|
| آیسیدی-۱۰ | G10, F02.2 |
| آیسیدی-۹ | 333.4, 294.1 |
| اُمیم | 143100 |
| دادگان بیماریها | 6060 |
| مدلاین پلاس | 000770 |
| ایمدیسین | article/1150165 article/792600 article/289706 |
| پیشنت پلاس | بیماری هانتینگتون |
| سمپ | D006816 |
بیماری هانتینگتون (به انگلیسی: Huntington's disease) در نکوداشت جورج هانتینگتون چنین نام گرفته است است. از علائم بیماری هانتینگتون (HD) کاهش شدید کنترل عضلانی، اختلال هیجانی و تداخلات آسیبشناختی (پاتولوژیک) در یاخته های مغز میباشد. این بیماری در اثرجهش در ژن کد کننده پروتئین هانتینگتین ایجاد میشود. آزمایشهای انجام شده بر موشهایی که دستکاری ژنتیکی شده بودند منجر به شناسایی این پروتئین شد.یک بیماری نورودژنراتیو پیشرونده با توارث اتوزومال غالب، با بروز در سنین بزرگسالی، این بیماری با تریاد سهگانهی حرکات غیرطبیعی کره،اختلالات شناختی،واختلالات روانی شناخته میشود.
ژن و پروتئین هانتینگتین
هانیتنگتون، در اثر افزایش توالی تکراری سه نوکلئوتیدی CAG درژن HD ایجاد میشود. مشخص شده است که ژن HD پروتیئنی بنام هانتینگتین را کد میکند. هانتینگتین در سپتوپلاسم سلولهای عصبی و متصل با غشا ها، وزیکولها و اسکلت سلولی وجود دارد. افزایش توالی CAG باعث ایجاد یک توالی پلی گلوتامین در پروتیئن هانتینگتین میشود. این توالی باعث اتصال پروتئینهای هانتنیگتین و پروتئینهای دیگر بهم میشود که منجربه تجمع اجسامی رشته مانند در سلولهای عصبی مغز میشود. پروتئین هانتینگین در انواع مختلفی از سلولها بیان میشود ولی فقط در سلولهای عصبی مغز باعث ایجاد اجسام رشتهای میشودکه علت این امر این است که برای تجمع یافتن پروتئینهای هانتینگنین، برهمکنش با پروتئینهای دیگری هم لازم میباشد که این پروتئینها به طور اختصاصی فقط در سلولهای عصبی مغز بیان میشوند.
بیماریهای دارای تکرار مشابه پلی گلوتامین
پژوهندگان میگویند یافتههای آنان نه تنها روشنگر عوامل دخیل در پاتولوژی HD است، بلکه نگاهی جدید به دیگر بیماریهای دارای تکرار مشابه پلی گلوتامین را که در آن ژنهای جهش یافته، پروتئینهایی را با زنجیرههای طویل غیرطبیعی از اسید آمینه گلوتامین تولید میکنند، دارد. به گفته پژوهشگران یافتههای آنان نشان میدهد تداخلات غیرطبیعی در ساختار پروتئینها در بیماریهای آلزایمر و پارکینسون نیز نقش دارد. همه این اختلالات به وسیله نورودژنراسیون انتخابی ایجاد شده توسط پروتئینهای بیماری مشخص میشوند، اما سازوکارهای (مکانیسم های) ملکولی و سلولی در این رابطه خیلی شناخته شده نیستند.
منابع
ویکیپدیا انگلیسی: Huntington's disease
ادامه مطلب
| هاری | |
|---|---|

سگی مبتلا به ویروس هاری
|
|
| آیسیدی-۱۰ | A82 |
| دادگان بیماریها | ۱۱۱۴۸ |
| ایمدیسین | med/۱۳۷۴ eerg/۴۹۳ ped/۱۹۷۴ |
| پیشنت پلاس | هاری |
| سمپ | D011818 |
هاری بیماری ویروسی است که موجب التهاب مغزی حاد میشود. ویروسی از خانواده رابدو ویریده این بیماری را ایجاد میکند. این ویروس در تمام حیوانات خونگرم از جمله انسان میتواند ایجاد بیماری کند. ویروس از بزاق حیوان مبتلا به هاری و محل گازگرفتگی وارد بدن شده در ماهیچهها به سمت اعصاب انتهایی میرود و شروع به تکثیر مینماید.
مرگ در صورت ابتلاء به هاری تقریباً قطعی است و در طول تاریخ تنها ۶ انسان از هاری جان سالم بهدر بردهاند. نجات یک دختر ۱۵ ساله از هاری در ویسکانسین، ایالات متحده آمریکا در سال ۲۰۰۴ اولین مورد گزارش شده از غلبه دستگاه ایمنی انسان بر این بیماری بدون استفاده از درمانهای خاص ضدهاری بود.[۱]
رئیس سازمان جهانی بهداشت حیوانات میگوید: «تا ۷۰ هزار کودک هستند که هر سال به طور دردناکی میمیرند و رسانهها آن را پوشش نمیدهند اما وقتی بیماری مرس ۲۰۰ آدم پیر را میکشد به آن توجه میشود.»[۲]
در گزارشی که «اتحاد جهانی علیه هاری» در سال ۲۰۱۵ منتشر کرده نشان میدهد سالانه حدود ۵۹،۰۰۰ نفر در جهان با ابتلاء به این بیماری عفونی در اثر گازگرفتگی سگ جان خود را از دست میدهند.[۳]
محتویات
شیوع
در سال ۲۰۱۰ حدود ۲۶ هزار نفر بر اثر این بیماری جان باختند. درحالیکه در سال ۱۹۹۰ این رقم بیش از دو برابر یعنی ۵۵ هزار نفر (۳۱ هزار نفر در آسیا و ۲۴ هزار نفر در آفریقا) بود.[۴] در سال ۲۰۱۵ اعلام شد که بیش از ۵۹ هزار نفر در اثر این بیماری کشته شدهاند.[۳]
بیشتر کشورهای توسعهیافته جهان، بیماری هاری را در میان سگها ریشهکن کردهاند. اما این بیماری هنوز در کشورهای در حال توسعه در میان سگهای خانگی وجود دارد. گزارش «اتحاد جهانی علیه هاری» میگوید روزانه حدود ۱۶۰ نفر در اثر این بیماری جان میدهند که اکثریت قریب به اتفاق این موارد در آسیا (۶۰ درصد) و آفریقا (۳۶ درصد) رخ میدهد. هند به تنهایی ۳۵ درصد از مرگ و میر ناشی از هاری را به خود اختصاص داده که بیشتر از هر کشور دیگری است. در گزارش "اتحاد جهانی علیه هاری" ایران جزو کشورهایی معرفی شده که مرگ و میر ناشی از هاری در آن سالانه بین ۲۰ تا ۹۰ نفر است. اما آمار و ارقام ارائهشده از سوی مقامهای بهداشتی ایران نشان میدهد تعداد ابتلا و مرگ و میر ناشی از هاری انگشتشمار است و به گفته آنها این بیماری در ایران تقریبا ریشهکن شده است.[۳]
در کل دنیا بیش از ۹۹ درصد موارد هاری در انسان از طریق سگ منتقل میشود اما در قاره آمریکا اکثر موارد هاری در انسانها از طریق خفاشها منتقل میشوند و انتقال از طریق سگ فقط کمتر از ۵ درصد کل موارد هاری را شامل میشود. بیماری هاری در حدود ۱۵۰ کشور دنیا وجود دارد. در بیشتر نقاط اروپا و استرالیا ویروس هاری فقط در خفاشها وجود دارد. در برخی جزایر هم این ویروس اصلاً وجود ندارد.
حدود ۴۰ درصد جانباختگان هاری زیر سن پانزده سالگی دچار گازگرفتگی میشوند. مبتلایان اغلب کودکانی هستند که شاید بدون ترس یا آگاهی به طرف سگهای آلوده رفته باشند. از آنجا که بسیاری از کودکان پس از گاز گرفته شدن قادر به توضیح حادثه برای والدین نیستند، این نگرانی برای سازمانهای بهداشتی وجود دارد که آمار واقعی مرگ بسیار بالاتر از آمار رسمی باشد.[۲]
در ایران
در گزارش «اتحاد جهانی علیه هاری» که در سال ۲۰۱۵ منتشر شد مرگ و میر سالانهٔ ناشی از هاری در ایران بین ۲۰ تا ۹۰ نفر اعلام شد. در این گزارش سرانه ابتلاء به هاری در یکصدهزار نفر جمعیت در ایران بین ۰٬۰۳۸ تا ۰٬۱۹ عنوان شده است. همچنین آمار و ارقام ارائهشده از سوی مقامهای بهداشتی ایران نشان میدهد تعداد ابتلاء و مرگ و میر ناشی از هاری انگشتشمار است و به گفته آنها این بیماری در ایران تقریباً ریشهکن شده است. به گفته رئیس مرکز مدیریت بیماریهای واگیر وزارت بهداشت، سالانه میلیاردها ریال صرف پیشگیری از بیماری هاری در ایران میشود و «کمتر بیماری واگیر در کشور وجود دارد که به اندازه این بیماری برای آن هزینه شود».[۳]
در سوئیس
بیشتر موارد ابتلا به هاری در کشور سوئیس مربوط به گازگرفتگی توسط روباه بود. اما دانشمندان با کار گذاشتن ویروس ضدهاری در سر مرغهای مرده و رها کردن آنها در کوههای آلپ و سپس خوردن آن مرغها توسط روباهها این بیماری را ریشهکن کردند.
عامل
عامل بیماری هاری نوعی ویروس RNA دار و نوروتروپ است، یعنی تمایل به سیستم عصبی دارد و وقتی به سیستم عصبی مرکزی حمله نماید تقریباً همیشه موجب مرگ میزبان میگردد.
ویروس هاری در حرارت ۵۰ درجه سانتی گراد در مدت ۱۵ دقیقه و در حرارت ۶۰ درجه در مدت ۳۵ ثانیه و در حرارت ۱۰۰ درجه سانتیگراد در مدت چند ثانیه از بین میرود؛ بنابراین برای ضدعفونی وسایل آلوده کافی است چند دقیقه آنها را جوشاند یا با فنل و الکل شستشو داد.
مخازن بیماری
کلیه حیوانات خونگرم پستاندار چه وحشی و چه اهلی به این بیماری حساس میباشند. البته در پرندگان ابتلاء به این بیماری فقط بهطور مصنوعی در آزمایشگاه گزارش شدهاست.
پرندگان، ماهیها، خزندگان و دوزیستان مبتلا نخواهند شد. در بیشتر مواقع هاری در حیوانات وحشی و عمدتاً در اسکانکها، راکونها، خفاش، کایوت و روباهها رایج است. همچنین در بین حیوانات اهلی، گاوهای شیرده در تعداد قابل ملاحظهای مبتلا میشوند و با شیوع کمتر در اسب، بز، گوسفند، خوک و راسو تشخیص داده میشود.
همچنین در حیوانات خانگی بیشتر در گربهها و سگها شایع است. اما در سالهای اخیر، درمیان حیوانات خانگی، گربهها بیشترین آلودگی را به این ویروس داشتهاند و آن به این خاطر است که صاحبان گربههایی که با محیط بیرون در ارتباط هستند آنها را در برابر هاری واکسینه نمیکنند. با وحود آن که در جهان ۹۹ درصد موارد هاری از سگها منتقل میشوند اما در ایالات متحده آمریکا که سگها را در برابر هاری واکسینه میکنند این مقدار کمتر از ۵ درصد است و بیشتر موارد هاری در آمریکا از طریق خفاشها است.
راههای سرایت بیماری
مهمترین راه انتقال هاری به انسان گاز گرفته شدن توسط حیوان هار است؛ بنابراین لمس و نوازش، ضربه زدن، لیس زدن پوست سالم، بوسیدن و یا هر روش دیگر، امکان انتقال هاری وجود نخواهد داشت. حتی اگر حیوانی شما را گاز گرفت، تنها در صورتی احتمال ابتلاء به هاری وجود دارد که حیوان حامل ویروس هاری باشد و ویروس به سیستم عصبی و بزاق حیوان وارد شده باشد؛ بنابراین هر گاز گرفتگی به معنی انتقال بیماری هاری نیست با این حال اقدامات درمانی و پیشگیرانه پس از گاز گرفته شدن ضروری است. (حیوان هار حداکثر ۱۰ روز زنده خواهد ماند.)[۵]
پیشگیری
افرادی که به دلیل شغلی (مانند کارکنان آزمایشگاه تشخیص هاری، دامپزشکان، شکارچیان، مأمورین حفاظت محیط زیست، جنگلبانان، کارکنان کشتارگاه، کسانی که در نیروهای مسلح تعلیم و تربیت سگ را به عهده دارند، کسانی که برای مطالعه به غارها میروند و به طور کلی کسانی که به نحوی ممکن است مورد گازگرفتگی حیوانات ذکر شده قرار گیرند) با حیوانات در تماس هستند باید علیه بیماری هاری واکسینه شوند. برای پیشگیری از هاری در این افراد واکسن در چهار نوبت تزریق میگردد که در نوبت دوم، سوم و چهارم به ترتیب ۷ روز، ۲۸ روز و یک سال بعد از نوبت اول تزریق میگردد و این افراد هر ۳ سال باید یک نوبت واکسن به عنوان یادآوری دریافت نمایند. (البته بعد از اندازهگیری آنتی بادی در خون)
درمان
کسی که توسط حیوانی مشکوک به هاری گاز گرفته شود باید فوراً محل گارگرفتگی را با آب و صابون به مدت حداقل ۱۵ دقیقه شستشو دهد و سریعاً به یک مرکز مقابله با هاری مراجعه کند تا با واکسیناسوین هاری درمان شود. شستوشوی زخم مربوط به گازگرفتگی حیوان و بخیه نکردن و بازبودن زخم بسیار مهم است و اساس پیشگیری و درمان هاری است. سپس میتوان از مواد ضدعفونی کننده مثل بتادین برای زخم استفاده نمود چون ویروس هاری به نور و جریان هوا حساس است در نتیجه زخم نباید بخیه زده شود و حتی الامکان روی زخم باز باشد.
به صورت معمول واکسیناسیون تا ۶ روز پس از گازگرفتگی و قبل از بروز علائم بیماری هاری میتواند ۱۰۰ درصد بیماری را از بین ببرد. اما پس از بروز علائم، درمان، دیگر امکانپذیر نیست و بیمار —با وجود مراقبتهای کامل— طی یک یا دو هفته جان خود را از دست خواهد داد.[۶]
علایم اولیه هاری عبارتاند از سرفه، خستگی، تب، سردرد، بدن درد، سوزش در محل گاز گرفتگی، کاهش اشتها، احساس تهوع، درد عضلانی، گلو درد. همچنین فرد مبتلا در طول این دوره ممکن است به صدا و نور بسیار حساس شود. پس از بروز این مراحل بهبودی فرد مبتلا تقریباً ناممکن است.
مرحله نهایی بیماری هاری، دوره حاد عصبی نام دارد. در طول این دوره، ویروس هاری سیستم عصبی مرکزی فرد را آلوده میکند. علایم نهایی هاری عبارت است از: اضطراب، رفتارهای خشونت آمیز، توهم و افسردگی، ترس از آب (ترس از آب به دلیل بیرون آمدن کف از دهان فرد بیمار)، مشکل در صحبت کردن و تکلم، ناتوانی در بلع، فلج شدن فک، حرکت غیر طبیعی عضله دیافراگم، دو بینی، ایست قلبی، مشکلات تنفسی، در نهایت مرگ بیمار تا حداکثر پس از دو هفته.
طبق اعلام انستیتو پاستور ایران اگر فردی دچار گازگرفتگی شود و یا پنجه حیوان ایجاد خراش در بدن وی نماید باید با مراکز پیشگیری و درمان هاری در سطح کشور مشاوره نموده و تحت درمان قرار گیرد واکسیناسیون علیه هاری در پنج نوبت انجام میشود که نوبت اول در روز حادثه یا روز مراجعه، نوبت دوم ۳ روز بعد، نوبت سوم ۷ روز بعد، نوبت چهارم ۱۴ روز بعد و نوبت پنجم ۳۰ روز بعد تزریق میگردد. سرم ضد هاری نیز در مواردی که مرکز پیشگیری و درمان هاری لازم بداند تزریق میگردد.
بهبودیافتگان
در طول تاریخ تنها ۶ انسان از هاری جان سالم بهدر بردهاند. نجات یک دختر ۱۵ ساله از هاری در ویسکانسین، ایالات متحده آمریکا در سال ۲۰۰۴ اولین مورد گزارش شده از غلبه دستگاه ایمنی انسان بر این بیماری بدون استفاده از درمانهای خاص ضدهاری بود.[۷]
در ۱۲ ژوئن ۲۰۱۱ پرشس رینولدز (Precious Reynolds) دختر ۸ سالهٔ اهل شهرستان هومبولت، کالیفرنیا توانست سومین مورد بهبودیافته در ایالات متحده باشد که بدون دریافت درمانهای پزشکی به ویروس هاری مقاومت نشان دهد.
کشورهایی که هاری را ریشهکن کردند
بسیاری از کشورها هاری را ریشهکن کردند یا در حال انجام این کار هستند. در زیر فهرست کشورهایی که در سال ۲۰۰۹ هیچگونه مورد هاری نداشتهاند آمدهاست:
- آفریقا: کیپ ورد، لیبی، موریس، مراسم، سائوتومه و پرنسیپ، و سیشل
- آمریکا: برمودا، سنت پیر و میکلون، آنتیگوا و باربودا، آروبا، باهاما، باربادوس، جزایر کیمن، دومینیکا، جزیره گوادلوپ، جامائیکا، مارتینیک، مونتسرات، آنتیل هلند، سنت کیتس (سنت کریستوفر) و نویس، سنت لوسیا، سنت مارتین، سنت وینسنت و گرنادین، ترکس و کایکوس، و جزایر ویرجین (بریتانیا و ایالات متحده)
-
آسیا و خاورمیانه: هنگ کنگ، ژاپن، کویت، لبنان، مالزی، قطر، سنگاپور، امارات متحده عربی
- تایوان در سال ۲۰۱۳ پس از آن که سه مورد سرنواری مبتلا یه هاری در آن یافت شد از فهرست خارج شد.
- اروپا: اتریش، بلژیک، قبرس، جمهوری چک، دانمارک، فنلاند، جبل الطارق، یونان، ایسلند، ایرلند، جزیره من، لوکزامبورگ، هلند، نروژ، پرتغال، اسپانیا (به جز سئوتا و ملیلیه)، سوئد، سوئیس، و انگلستان
- اقیانوسیه: استرالیا، جزایر کوک، فیجی، پلینزی فرانسه، گوام، هاوایی، کیریباتی، میکرونزی، کالدونیای جدید، نیوزیلند، جزایر شمالی ماریانا، پالائو، پاپوآ گینه نو، ساموآ، و وانواتو
منابع
- Recovery of a Patient from Clinical Rabies - Wisconsin, 2004 Morbidity and Mortality Weekly Report
- مکگرات، مت. «هاری قربانی زیاد میگیرد 'اما بودجه مقابله نمیرسد'». بیبیسی فارسی، ۶ خرداد ۱۳۹۳. بازبینیشده در ۲۸ مه ۲۰۱۴.
- «هاری 'سالانه دهها هزار قربانی میگیرد'». بیبیسی فارسی، ۲۸ فروردین ۹۴.
- Rabies WHO
- http://www.asreelm.com/rabies/
- «هاری». دفتر آموزش و ارتقای سلامت. بازبینیشده در ۱۹ آبان ۱۳۹۱.
- Recovery of a Patient from Clinical Rabies - Wisconsin, 2004 Morbidity and Mortality Weekly Report
پیوند به بیرون
ادامه مطلب
Attri S, Sharma N, Jahagirdar S, Thapa BR Prasad R. Erythrocyte metabolism and antioxidant status of patients with Wilson disease with hemolytic anemia. Pediatr Res ۲۰۰۶ ; ۵۹(۴ Pt ۱): ۵۹۳-۷.
-
بیماری ویلسون 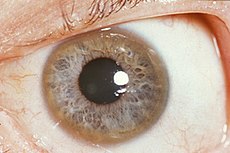 A Kayser-Fleischer ring (the brown ring on the edge of the iris) is common in Wilson's disease, especially when neurological symptoms are present
A Kayser-Fleischer ring (the brown ring on the edge of the iris) is common in Wilson's disease, especially when neurological symptoms are presentآیسیدی-۱۰ E83.0 آیسیدی-۹ 275.1 اُمیم 277900 دادگان بیماریها 14152 مدلاین پلاس 000785 ایمدیسین med/2413 neuro/570 ped/2441 پیشنت پلاس بیماری ویلسون سمپ D006527 مرور ژن Wilson Disease بیماری ویلسون یک اختلال ارثی اتوزوم مغلوب در متابولیسم مس است که در آن تجمع مس در ارگانها و بافتهای مختلف دیده میشود. شیوع نسبی آن یک در صدهزار تولد تا یک در پانصدهزار تولد است. افزایش تجمع مس احتمالن ناشی از نقص لیزوزومهای کبدی در دفع مس از طریق صفراست که نتیجه ی آن تجمع مس در حد توکسیک در کبد، مغز، کلیه، چشم و سایر بافتها میباشد. ژن معیوب روی بازوی بلند کروموزوم شماره ۱۳ قرار دارد.[۱].
محتویات
مس و سرولوپلاسمین
حدود ۹۵ ٪ از مس موجود در خون با پروتئینی به نام سرولوپلاسمین همراه است و بقیه آن به صورت مس آزاد وجود دارد. سرولوپلاسمین پروتئینی از نوع آلفا دو گلوبین و یک گلیکوپروتئین است که ۷٫۵ درصد آن کربوهیدرات بوده و وزن ملکولی ان حدود ۱۵۱۰۰۰ دالتون میباشد. هر مولکول سرولوپلاسمین شامل ۸ اتم مس است. مقدار سرلوپلاسمین در سرم خون در زنان حدود mg/dl ۴۰/۹±۶/۸ و در مردان حدود mg/dl ۳۶/۰±۵/۶ است. هرچند مقدار طبیعی مس در خون، در منابع مختلف متفاوت ذکر شده است ولی به طورکلی میتوان آن را حدود ۱۰۰-۲۰۰ μg/dl در نظر گرفت.[۲]
نشانهها
نشانه های تیپیک بیماری ویلسون تریاد اختلالات عصبی، حلقه kayser-fleischer (حلقه کایزر فلاشر) و سیروز کبدی همراه با پایین بودن مس و سرولوپلاسمین سرم است. باید بیماری ویلسون را در تمام کودکانی که بیماری کبدی دارند در نظر داشت بخصوص چنانچه بیش از یک کودک در خانواده، مبتلا به بیماری کبدی باشند. رسوب مس در مغز منجر به تظاهرات عصبی شبه پارکینسون میشود (اختلال عصبی) بیماری ویلسون باید در هر فرد بالاتر از ۵ سال که دچار بیماری کبدی میباشد در تشخیص افتراقی مطرح شود. تشخیص سریع و درمان آن نجات دهنده میباشد.
کم خونی همولیتیک شدید یک تظاهر و عارضه ناشایع بیماری ویلسون است ولی گزارش هایی از همولیز نیز، به عنوان اولین تظاهر بیماری ویلسون داده شده است.[۳]
مس آزاد شده رادیکال آزاد اکسیژن ایجاد میکند که غشای گلبول قرمز را سوراخ کرده، باعث اختلال آنزیمهای گلیکولیتیک مانند هگزوکیناز میشود. فعالیت آنزیمهای آنتی اکسیدان مانند گلوکز ۶ فسفات دهیدروژناز، گلوتاتیون ردوکتاز، کاتالاز و سوپراکسیداز دیسموتاز متوقف میشود. این مجموعه سبب آسیب اکسیداتیو گلبول قرمز و رسوب احتمالی اجسام هاینز در آن شده، سبب تغییر شکل گلبول قرمز میشود که در نهایت لیزگلبول قرمز اتفاق میافتد.[۴]
درمان
موثرترین دارو در درمان بیماری ویلسون دی پنی سیلامین (پنی سیلامین) است. همراه آن باید ویتامین B۶ و روی (جهت کاهش جذب رودهای مس) نیز تجویز شود. درمان برای تمام عمر ادامه مییابد و باید وابستگان و فرزندان خانواده با slit lamp، تستهای کبدی و اندازهگیری سرولوپلاسمین بررسی گردند.
منابع
- Thomas GR, Forbes JR, Roberts EA, Walshe JM, Cox DW. The Wilson disease gene spectrum of mutations and their consequences Nat Genet ۱۹۹۵;۹(۲):۲۱۰-۷.
- Raphael SS. Lynches Medical Laboratory Technology. Philadelphia: WB Saunders: ۱۹۸۳٫۲۶۷.
- Segel GB. Hemolytic anemias secndary to extracellular factors, Nelson Textbook of Pediatrics. ۱۷th Edi. Philadelphia: WBSauders;۲۰۰۶.p.۱۶۴۰
ادامه مطلب
| دادهها در دیگر منابع | |
|---|---|

Non-segmental vitiligo of the hand.
|
|
| آیسیدی-۱۰ | L80 |
| آیسیدی-۹ | 709.01 |
| اُمیم | 193200 |
| دادگان بیماریها | 13965 |
| مدلاین پلاس | 000831 |
| ایمدیسین | derm/453 |
| پیشنت پلاس | پیسی |
| سمپ | D014820 |
پیسی، بَرَص، لک و پیس یا ویتیلیگو (Vitiligo) یک اختلال تولید رنگدانه است که در آن ملانوسیتها (سلولهایی که رنگدانه تولید میکنند) در قسمتهایی از پوست، غشاهای مخاطی و شبکیه تخریب شدهاند. در نتیجه لکههای سفید پوست درنواحی مختلف بدن ظاهر میشوند. مویی که در نواحی مبتلا به پیسی رشد میکند معمولاً سفید میشود.
علّت بیماری پیسی شناخته نشدهاست، اما پزشکان چندین نظریه متفاوت مطرح کردهاند. یک تئوری این است که افراد پادتنهایی (آنتیبادیهایی) تولید میکنند که ملانوسیتهای بدن خودشان را تخریب میکند. تئوری دیگر این است که ملانوسیتها خود به خود تخریب میشوند. درنهایت بعضی افراد گزارش کردهاند که یک رخداد منفرد از قبیل آفتاب سوختگی یا فشار روحی باعث بروز پیسی شدهاست ولی مورد اخیر از نظر علمی ثابت نشدهاست.
محتویات
درصد افراد مبتلا به پیسی
حدود یک تا دو درصد جمعیت دنیا یا (۵۰-۴۰ میلیون نفر)، به بیماری پیسی مبتلا هستند. ۹۵٪ افراد قبل از ۴۰ سالگی علائم را نشان دادهاند. بیماری تمام نژادها و هر دو جنس را یکسان تحت تأثیر قرار میدهد. بهنظر میرسد پیسی در افراد مبتلا به بیماریهای اتوایمیون شایعتر است . این بیماریهای اتوایمیون عبارتاند از: پرکاری غده تیروئید، نارسایی قشر غده فوق کلیه، آلوپسی آره آتا و آنمی پرنسیوز.
پیسی میتواند بیماری ارثی باشد یعنی در بین افراد فامیل بروز کند کودکانی که والدینشان مبتلا به این بیماری هستند بیشتر احتمال ابتلا به پیسی دارند. با این حال بیشتر کودکانی که یکی از والدینشان مبتلا به پیسی باشند به بیماری مبتلا نمیشوند و بیشتر افراد مبتلا به پیسی سابقهای از این بیماری را در فامیل ندارند.
علائم بیماری پیسی
معمولاً افراد مبتلا به پیسی اول از همه به رنگدانهدار شدن (پیگمانتاسیون) به حالت لکههای سفید روی پوستشان توجه میکنند. این لکهها بیشتر از همه در مناطق در معرض نور از قبیل دستها پاها بازوها، صورت و لبها شایع هستند. دیگر نقاط شایع لکههای سفید عبارتاند از زیر بغل و کشاله ران، اطراف دهان و چشم، پرههای بینی، ناف و نواحی تناسلی.
پیسی معمولاً به یکی از سه الگوی زیر ظاهر میشود:
- در یک الگو (الگوی کانونی) ناحیه بدون رنگدانه به یک یا تعداد معدودی ناحیه محدود میشود. بعضی افراد نواحی بدون رنگدانه را در یک سمت بدن خود دارند (الگوی سگمنتال). اما در بیشتر افراد مبتلا به پیسی نواحی فاقد رنگدانه در قسمتهای مختلف بدن بوجود میآید (الگوی ژنرالیزه). علاوه بر لکههای سفید روی پوست، ممکن است افراد مبتلا به برص سفید شدن زودرس موهای سر، ابروها و ریش را داشته باشند. افراد با پوست تیره ممکن است متوجه فقدان رنگ در ناحیهای در داخل دهانشان بشوند.
- در برخی افراد لکههای فاقد رنگ گسترش نمییابد ولی این اختلال معمولاً پیشروندهاست و به مرور زمان این لکههای سفید به دیگر نواحی بدن گسترش مییابند .
- در بعضی افراد پیسی به آهستگی طی چند سال گسترش مییابد و در برخی دیگر انتشار سریعاً رخ میدهد . برخی افراد گزارش کردهاند که بهدنبال دورههایی از استرس فیزیکی یا روحی، به تعداد لکههای فاقد رنگدانه اضافه شدهاست.
درمان
متاسفانه بسیاری از موارد اين بيماری قابل درمان نیستند. 70 تا 75% بیماران به درمانهای دارويی، نور درمانی و ليزر درمانی پاسخ میدهند .
هدف اصلي در درمانهاي رايج ويتيليگو، بهبود وضعيت ظاهری پوست است و روند درمان نياز به زمان طولانی دارد كه معمولا 6 تا 18 ماه به طول می انجامد، انتخاب نوع درمان به تعداد، محل و گستردگی ضايعات بستگی دارد.
استروئيد موضعی ميتواند در برگرداندن رنگ پوست به لكههاي سفيد كمك كند، بخصوص اگر اين درمان در مراحل اوليه بيماري شروع شود. درمان بايد حداقل تا 3 ماه ادامه يابد تا بهبود قابل ملاحظه ایجاد شود.
با وجود آن كه استفاده از ليزر و نور درمانی (فتوتراپی) ميتواند عوارضی را برای شخص به همراه داشته باشد (بخصوص برروی پوست نواحی سالم)، در مواردی كه بيماری شكل گستردهای دارد، انتخاب ديگري براي درمان لكههاي پوستی باقي نميماند.
یک روش دیگر در موارد مقاوم به درمان عبارت است از بيرنگ كردن باقيمانده پوست بدن تا با لكههاي سفيد همرنگ شود. اين روش درماني براي بيماراني كه حداقل 50% پوست آنها گرفتار است، توصيه ميشود. به علاوه روشهاي ديگري هم به صورت موقت ميتوانند در اين بيماران موثر باشند مانند استفاده از پوشانندههای پوست با مواد آرايشی يا خالكوبي كردن منطقه درگير تا همرنگ پوست شود.
براي حداقل يك سوم بيماراني كه به هيچ كدام از اين روشها، پاسخ درمانی مثبت نميدهند، راهي جز سلول درمانی (استفاده از سلولهای ملانوسیت سالم) باقي نميماند. البته این روش هنوز در مراحل تحقیقاتی است و هنوز کاملا رایج نیست.
نگارخانه
منابع
- ویکیپدیای انگلیسی
ادامه مطلب